Clear Sky Science · tr
NDUFA4L2, PANoptosis'i inhibe ederek HNSCC’nin ilerlemesini ve kemoterapi duyarlılığını düzenler
Bu araştırma neden önemli
Kemoterapi, baş ve boyun kanseri olan birçok kişi için bir can simididir, ancak tümörler genellikle ilaçları etkisiz kılmayı öğrenir. Bu çalışma, tek bir mitokondriyal protein olan NDUFA4L2’nin baş ve boyun skuamöz hücreli karsinomunun yaygın olarak kullanılan sisplatin ilacından kaçmasına nasıl yardımcı olduğunu ortaya koyuyor ve bu proteini kapatmanın kanser hücrelerini daha etkili öldürebileceğini ve bağışıklık sistemini harekete geçirebileceğini gösteriyor. Çalışma, kanser hücrelerinin şekeri yakma ve ölme yollarını hedefleyerek ilaç duyarlılığını geri kazandırmanın yeni yollarına işaret ediyor.
İnatçı bir kanser ve etkisizleşen bir ilaç
Baş ve boyun skuamöz hücreli karsinom (HNSCC), dünyada en yaygın kanserler arasında yer alır ve genellikle sisplatin ile tedavi edilir. Ancak birçok tümör zamanla direnç geliştirir ve hastaların seçenekleri sınırlanır. Yazarlar, düşük oksijen koşullarında açılan ve hücrelerin yakıt kullanımını değiştiren hücre enerji fabrikası (mitokondri) proteinlerinden NDUFA4L2’ye odaklandı. Halkalı tek hücre veri setlerini analiz ederek ve hasta tümör örneklerini inceleyerek, NDUFA4L2’nin kötü prognozla ilişkili belirgin bir tümör hücresi alt grubunda yüksek düzeyde aktif olduğunu buldular. Kemoterapiye artık yanıt vermeyen hastaların tümörleri özellikle yüksek miktarda bu protein içeriyordu; bu da proteinin direncin merkezinde olduğunu düşündürüyor.
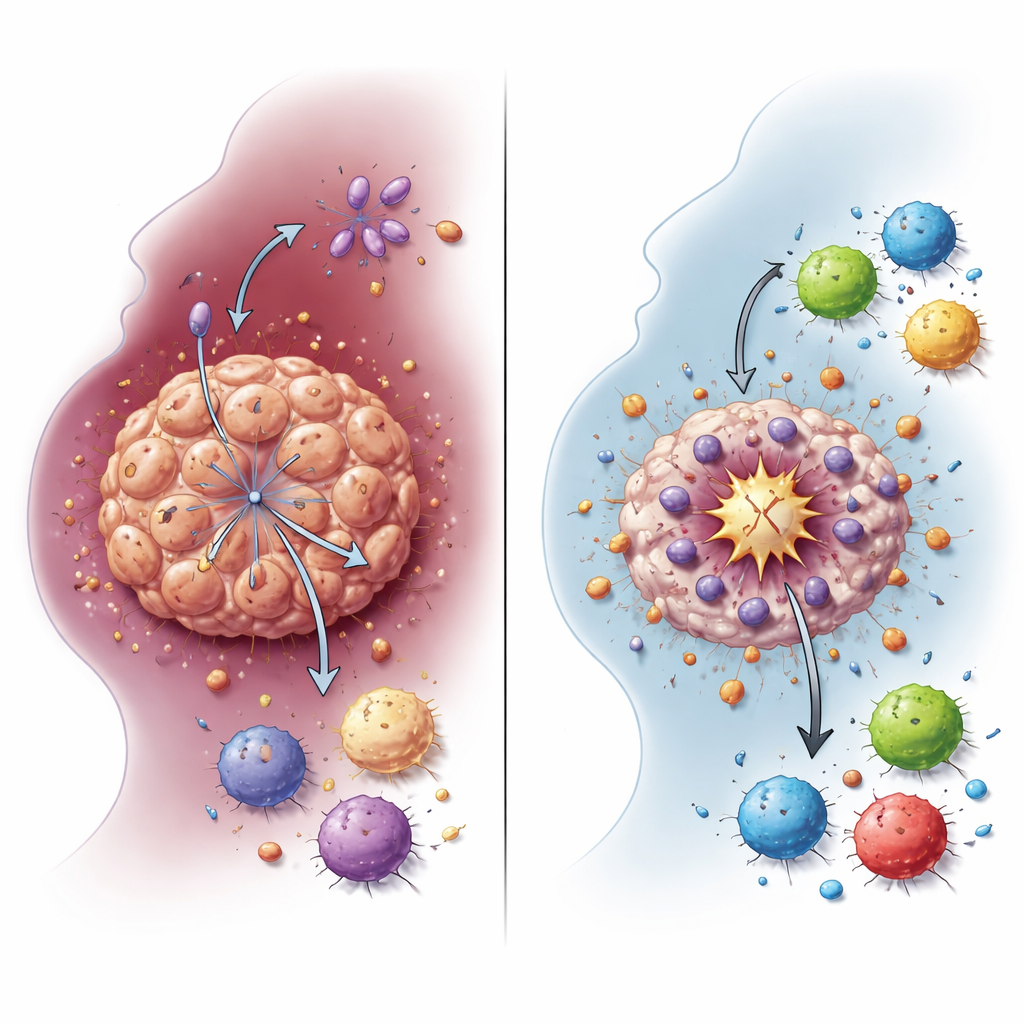
Yakıt değişiminin tümör hücrelerini nasıl koruduğu
Kanser hücreleri sıklıkla oksijen mevcut olsa bile yüksek miktarda laktat üreten glikoliz adı verilen kısa yol şeker yakımına dayanır. Ekip, NDUFA4L2’nin HNSCC hücrelerinde bu glikolitik durumu desteklediğini gösterdi. NDUFA4L2 hücre hatlarından ve hasta örneklerinden büyütülen üç boyutlu mini tümörlerden kaldırıldığında, laktat seviyeleri keskin şekilde düştü. Gen etkinliği desenleri glikoliz ve laktat metabolizmasından uzaklaştı; böylece NDUFA4L2 doğrudan kanserin değişmiş enerji kullanımıyla ilişkilendirildi. Bu yakıt değişimi sadece kanser büyümesinin bir yan ürünü değil: sisplatinden kaçmaya ve özellikle etkili bir hücre ölümü biçiminden korunmaya yardımcı olan bir kalkan olduğu anlaşıldı.
Kanser hücrelerini üçlü ölüm programına zorlamak
Hücreler; apoptoz, nekroptoz ve piroptoz dahil olmak üzere çeşitli düzenlenmiş yollarla ölebilir. Son zamanlarda araştırmacılar, bu üçünün önemli bileşenlerini birleştiren entegre bir “hepsi bir arada” ölüm programı olan PANoptosis’i tanımladı. Bu çalışmada NDUFA4L2’nin yok edilmesi HNSCC hücrelerini sisplatine karşı çok daha hassas hale getirdi. Mikroskop altında tedavi edilen hücreler karakteristik balonlaşma ve parçalanma gösterdi ve biyokimyasal testler apoptoz, nekroptoz ve piroptoz belirteçlerinin eşzamanlı aktivasyonunu doğruladı. Önemli olarak, herhangi bir tek yolun bloke edilmesi hücreleri yalnızca kısmen kurtardı; bu da tam PANoptosis programının devreye girdiğini gösteriyor. Dil tümörü fare modellerinde NDUFA4L2’nin kaldırılması ve sisplatin verilmesi tümörleri küçülttü, yaşam süresini uzattı ve bu birleşik ölüm yanıtının belirteçlerini artırdı.
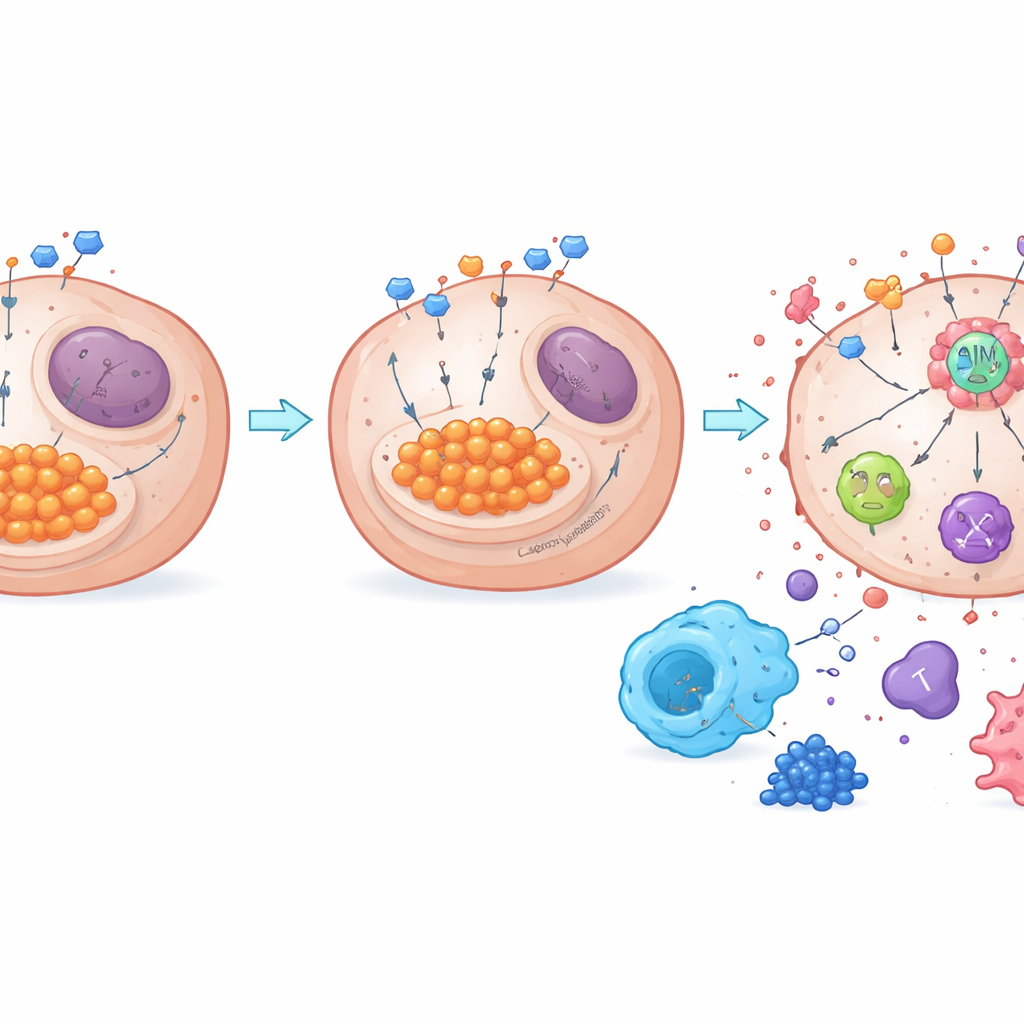
Şeker atığından bağışıklık uyanışına
Çalışma ayrıca metabolizmanın AIM2 adlı anahtar bir ölüm düzenleyici sensörle nasıl bağlandığını ortaya koyuyor. Glikoliz yüksek olduğunda, fazla laktat proteinleri laktile etme olarak bilinen kimyasal bir değişiklikle modifiye edebilir. Yazarlar, NDUFA4L2’nin laktat seviyelerini yüksek tuttuğunu ve AIM2’nin laktile olmasını teşvik ettiğini; bunun da bu sensörü baskılanmış bir durumda tuttuğunu keşfettiler. NDUFA4L2’nın kaldırılması laktatı azalttı, AIM2 laktilasyonunu düşürdü ve PANoptosis’i tetikleyen AIM2 tabanlı bir ölüm kompleksinin oluşumunu güçlendirdi. AIM2 deneysel olarak azaltıldığında, NDUFA4L2 kaybı ile sisplatinin güçlü öldürücü etkisi büyük ölçüde azaldı; bu da AIM2’nin merkezi rolünü doğruladı. Hem fare tümörlerinde hem de insan örneklerinde yüksek NDUFA4L2 ve laktilasyon, daha immünsüpresif makrofajlarla ve daha az kanserle savaşan T hücresiyle ilişkiliyken, glikolizi veya NDUFA4L2’yi engellemek, dengeyi daha aktif bir bağışıklık ortamına doğru kaydırdı.
Gelecekteki tedaviler için ne anlama geliyor
Bir gözlemci için bu çalışma, bazı baş ve boyun kanserlerinin şekeri kullanma biçimlerini yeniden kablajlayarak ve yerleşik bir kendini yok etme anahtarını susturarak kemoterapiden nasıl kaçtığını gösteriyor. NDUFA4L2’yi azaltarak veya glikolizi engelleyerek araştırmacılar laktatı düşürebildiler, AIM2 ölüm sensörünü yeniden etkinleştirebildiler, saldırgan bir üç modlu hücre ölümü programını tetikleyebildiler ve sisplatinin hücrelerde, organoidlerde ve farelerde daha iyi çalışmasını sağladılar. Aynı zamanda tümör çevresi bağışıklık saldırılarına daha açık hale geldi. Bu bulgular, NDUFA4L2’ye veya onun kontrol ettiği metabolik ve laktilasyon yollarına yönelik ilaçların bir gün standart kemoterapi ile birleştirilerek direncin aşılmasına ve baş ve boyun kanseri hastalarının sonuçlarının iyileştirilmesine katkıda bulunabileceğini öne sürüyor.
Atıf: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Anahtar kelimeler: baş ve boyun kanseri, kemoterapi direnci, kanser metabolizması, programlanmış hücre ölümü, tümör mikroçevresi