Clear Sky Science · nl
NDUFA4L2 reguleert de progressie en chemogevoeligheid van HNSCC door PANoptose te remmen
Waarom dit onderzoek ertoe doet
Chemotherapie is voor veel mensen met hoofd‑en‑halskankers een levenslijn, maar tumorcellen vinden vaak manieren om de medicijnen te omzeilen. Deze studie onthult hoe een enkel mitochondriaal eiwit, NDUFA4L2, helpt bij plaveiselcelcarcinoom van hoofd en hals (HNSCC) om het veelgebruikte middel cisplatine te ontwijken, en laat zien dat het uitschakelen van dit eiwit zowel kankercellen effectiever kan doden als het immuunsysteem kan activeren. Het werk wijst op nieuwe wegen om geneesmiddelengevoeligheid te herstellen door in te grijpen in de manier waarop kankercellen suiker verbranden en afsterven.
Een hardnekkige kanker en een falend middel
Plaveiselcelcarcinoom van hoofd en hals (HNSCC) behoort tot de meest voorkomende kankers wereldwijd en wordt vaak met cisplatine behandeld. Veel tumoren worden echter resistent, waardoor patiënten beperkte opties overhouden. De auteurs richtten zich op NDUFA4L2, een eiwit in de energiecentrales van de cel (mitochondriën) dat wordt aangezet bij lage zuurstof en invloed heeft op hoe cellen hun brandstof gebruiken. Door openbare single‑cell datasets te analyseren en patiënttumoren te onderzoeken, vonden ze dat NDUFA4L2 sterk actief is in een specifieke subgroep tumorcellen die geassocieerd is met slechtere overleving. Tumoren van patiënten bij wie de kanker niet langer op chemotherapie reageerde, vertoonden bijzonder hoge niveaus van dit eiwit, wat suggereert dat het een centrale rol speelt bij resistentie.
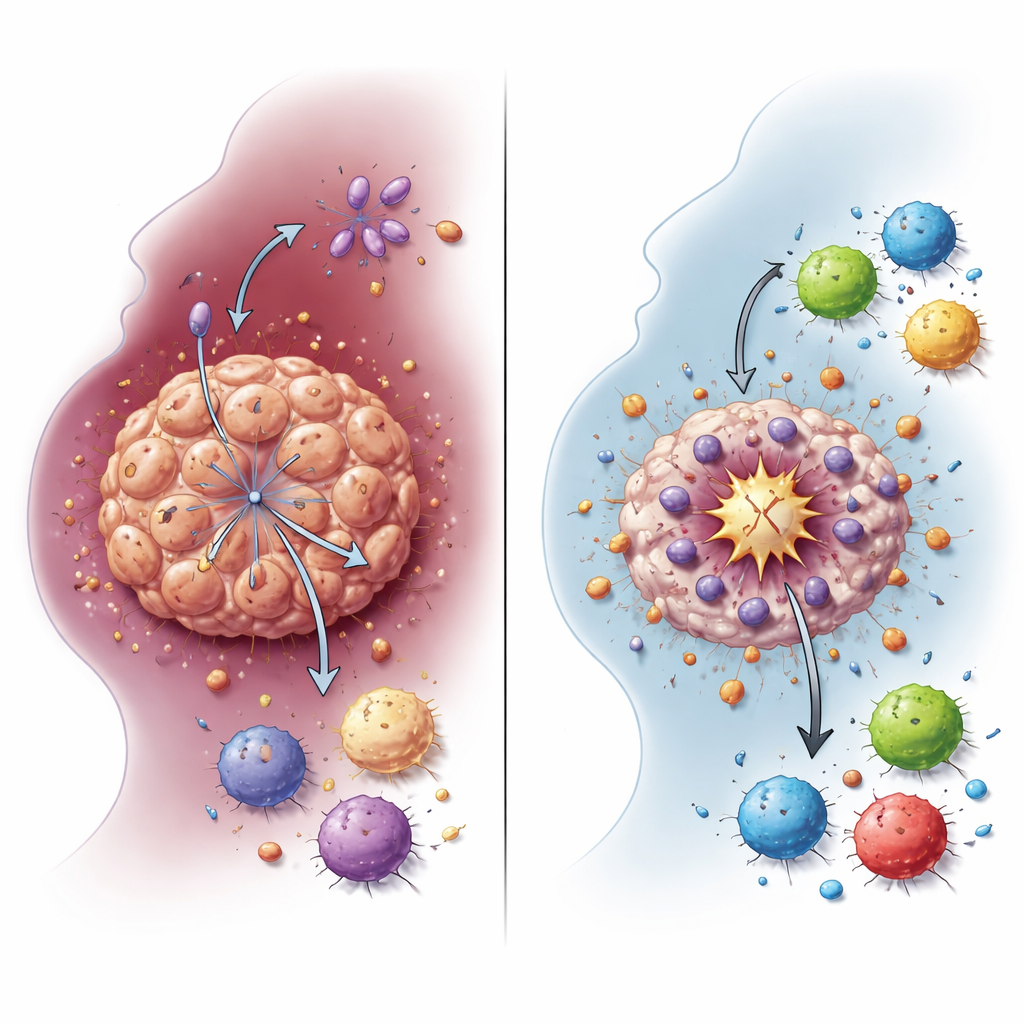
Hoe een brandstofschakel beschermt tumorcellen
Kankercellen vertrouwen vaak op een verkorte manier van suikerverbranding, glycolyse genoemd, die grote hoeveelheden lactaat produceert ook wanneer zuurstof beschikbaar is. Het team toonde aan dat NDUFA4L2 deze glycolytische toestand in HNSCC‑cellen ondersteunt. Wanneer NDUFA4L2 uit celkweken en uit driedimensionale mini‑tumoren gemaakt van patiëntmonsters werd verwijderd, daalden de lactaatniveaus scherp. Genexpressiepatronen verschooften weg van glycolyse en lactaatmetabolisme, waarmee NDUFA4L2 rechtstreeks gerelateerd werd aan het veranderde energiegebruik van de tumor. Deze brandstofschakel is niet slechts een bijproduct van kankergroei: het blijkt een schild te zijn dat tumorcellen helpt cisplatine te overleven en een bijzonder krachtige vorm van celdood te vermijden.
Gevangen nemen van kankercellen in een driedubbel doodprogramma
Cellen kunnen via verschillende gereguleerde routes sterven, waaronder apoptose, necroptose en pyroptose. Onlangs beschreven onderzoekers PANoptose, een geïntegreerd "alles‑in‑één" doodsprogramma dat sleutelonderdelen van alle drie combineert. In deze studie maakte het uitzetten van NDUFA4L2 HNSCC‑cellen veel gevoeliger voor cisplatine. Onder de microscoop toonden behandelde cellen karakteristieke opzwellingen en ruptuur, en biochemische testen bevestigden gelijktijdige activatie van merkers voor apoptose, necroptose en pyroptose. Belangrijk is dat het blokkeren van één enkele route slechts gedeeltelijk bescherming bood, wat aangeeft dat het volledige PANoptose‑programma werd geactiveerd. In muismodellen van tongtumoren zorgde het verwijderen van NDUFA4L2 gecombineerd met cisplatine voor krimp van tumoren, verlengde overleving en verhoging van merkers van deze gecombineerde doodsreactie.
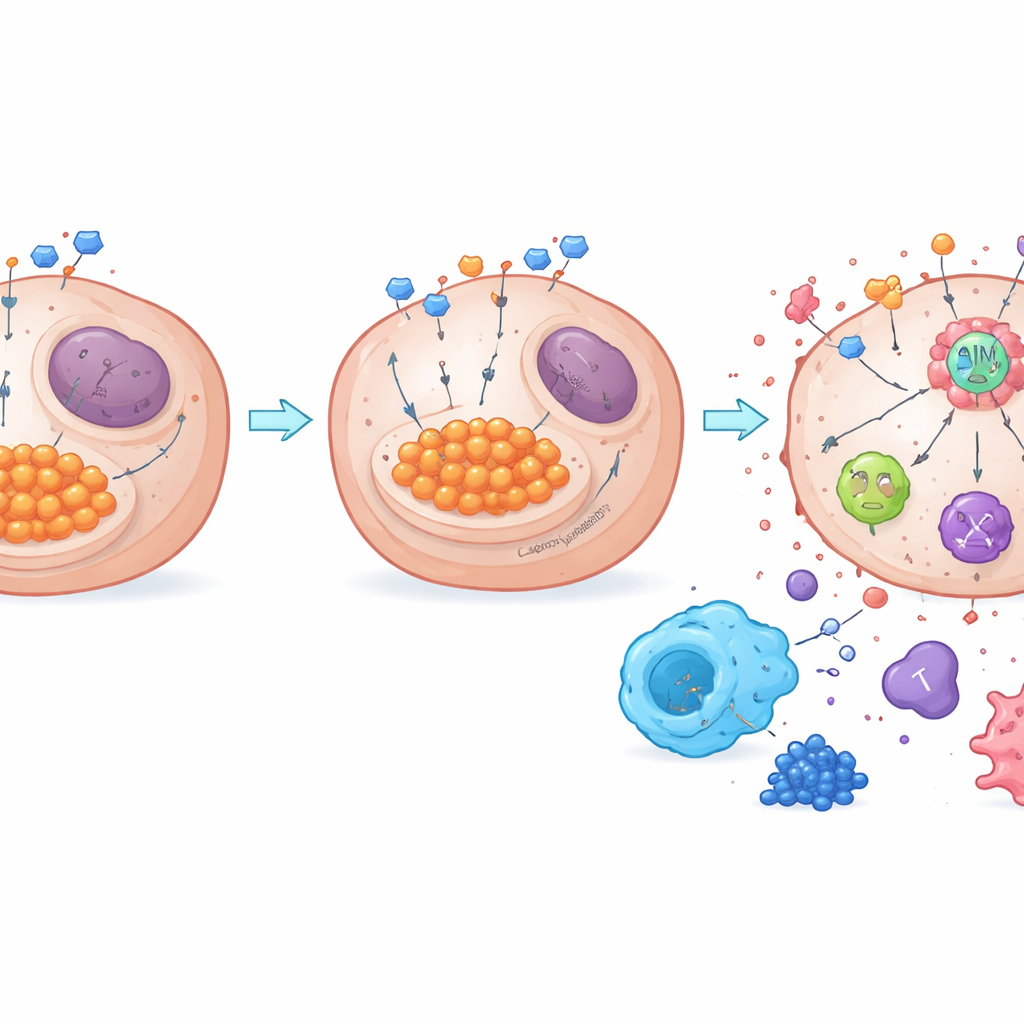
Van suikerverspilling naar immuunactivatie
Het werk laat ook zien hoe metabolisme verbonden is met een belangrijke doodsregulerende sensor genaamd AIM2. Wanneer glycolyse hoog is, kan overtollig lactaat eiwitten chemisch modificeren in een proces dat lactylatie wordt genoemd. De auteurs ontdekten dat NDUFA4L2 lactaatniveaus hoog houdt en de lactylatie van AIM2 bevordert, wat deze sensor in een onderdrukte staat lijkt te houden. Het verwijderen van NDUFA4L2 verlaagde lactaat, verminderde AIM2‑lactylatie en versterkte de assemblage van een AIM2‑gebaseerd doodscomplex dat PANoptose activeert. Wanneer AIM2 experimenteel werd geremd, verdween het krachtige dodeffect van NDUFA4L2‑verlies plus cisplatine grotendeels, waarmee de centrale rol van AIM2 werd bevestigd. In zowel muistumoren als menselijke monsters werden hoge NDUFA4L2‑levels en lactylatie gekoppeld aan meer immuunsuppressieve macrofagen en minder kankerdodende T‑cellen, terwijl het blokkeren van glycolyse of NDUFA4L2 het evenwicht verschoof naar een meer actieve immuunomgeving.
Wat dit betekent voor toekomstige behandelingen
Voor een niet‑specialist toont deze studie dat bepaalde hoofd‑en‑halskankers chemotherapie overleven door hun suikergebruik te herbedraden en een ingebouwde zelfvernietigingsschakel te dempen. Door NDUFA4L2 te verminderen of glycolyse te remmen, konden de onderzoekers lactaat verlagen, de AIM2‑doodsensor heractiveren, een agressief driedubbel celdoodprogramma in gang zetten en cisplatine effectiever maken in cellen, organoïden en muizen. Tegelijk werd de tumoromgeving ontvankelijker voor immuunaanvallen. Deze bevindingen suggereren dat geneesmiddelen gericht op NDUFA4L2, of op de metabolische en lactylatiepaden die het reguleert, mogelijk in de toekomst gecombineerd kunnen worden met standaardchemotherapie om resistentie te overwinnen en de uitkomsten voor patiënten met hoofd‑en‑halskanker te verbeteren.
Bronvermelding: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Trefwoorden: hoofdhalskanker, chemotherapie-resistentie, kankermetabolisme, geprogrammeerde celdood, tumormicro-omgeving