Clear Sky Science · zh
设计、合成及抗菌评估:一系列基于环丙沙星的新化合物,作为可能的双靶向DNA旋转酶/拓扑异构酶IV抑制剂
这对日常感染为何重要
抗生素耐药正使曾经常见且易治的感染变得更难治疗且成本更高。环丙沙星是用于泌尿道、肠道和肺部感染的常用抗生素,但它对某些细菌的效力正在下降。本研究探索了一种巧妙的改造方法,以升级环丙沙星的分子设计,使其能够同时更强烈地作用于两个关键靶点,从而可能减缓耐药性的演进并改善对顽固感染的治疗效果。
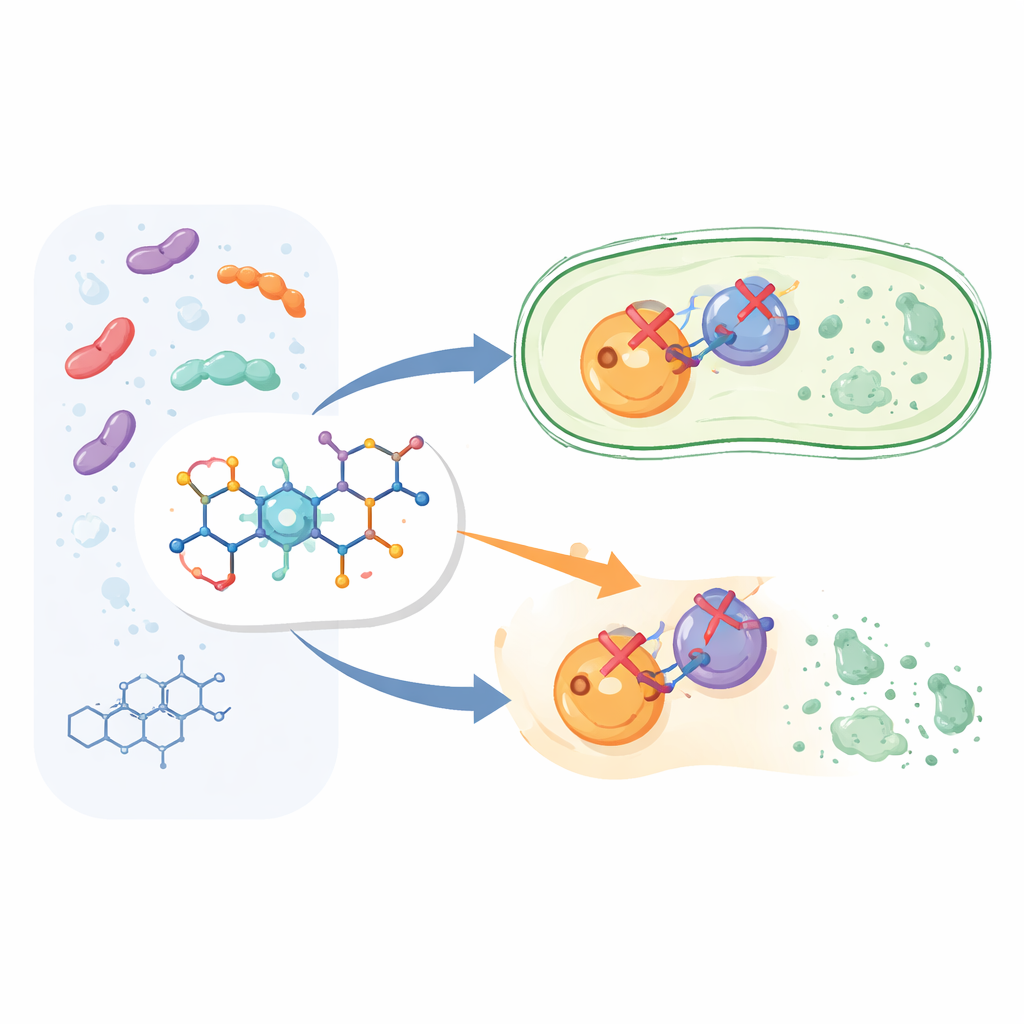
构建一种更聪明的熟悉药物
研究者没有从零开始开发全新药物,而是改造了环丙沙星的骨架——它属于广泛使用的氟喹诺酮家族。他们保留了已知具有杀菌作用的环丙沙星核心结构,并在分子的特定位点接入了一个称为芳基吡啶酮的附加化学片段。由此产生了十二种新化合物,标记为6a到6l。设想是这个额外的“握把”能让药物更牢固且更灵活地与细菌靶点结合,相较于标准环丙沙星具有更强的作用方式。
同时靶向细菌的两条生命线
细菌在生长和分裂时依赖两种密切相关的酶——DNA旋转酶和拓扑异构酶IV——来管理其DNA。环丙沙星已能干扰这些酶,但抑制效果并不均等。新合成的化合物被设计为能同时强力阻断这两种靶点,从而使细菌仅通过在单一酶上产生突变来逃逸的难度增大。在以大肠杆菌蛋白为对象的酶学测试中,大多数新分子在抑制DNA旋转酶和拓扑异构酶IV方面达到了有用的水平。其中一种称为6g的化合物尤为突出:它对DNA旋转酶的抑制略优于环丙沙星,对拓扑异构酶IV的抑制则约高出七倍,使其成为该系列中最强效的“双重作用”分子。
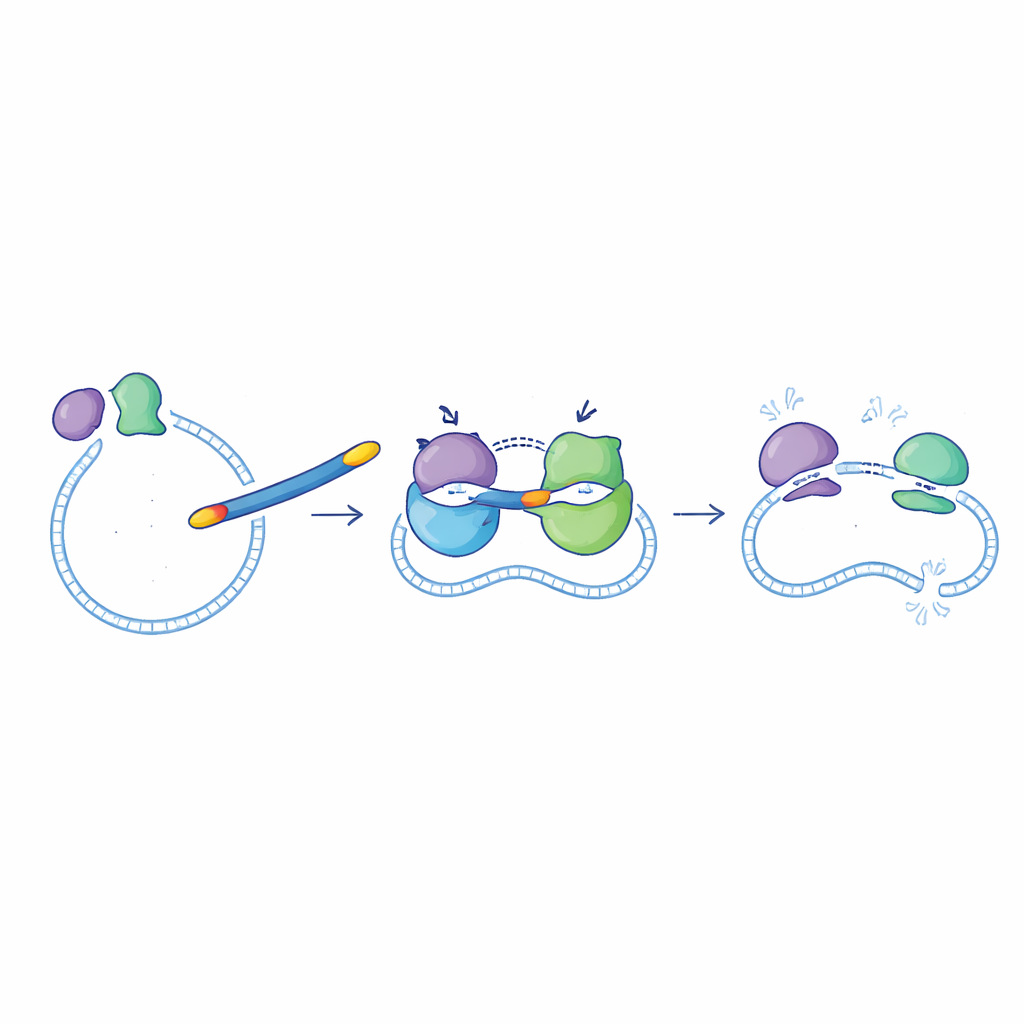
将新分子置于细菌实测中
团队接着检验酶学上的改进是否能转化为对实验室培养细菌的更好抑制效果。挑选出的表现优异者,包括6d、6f、6g、6i和6l,在两种革兰阴性菌(大肠杆菌和铜绿假单胞菌)与两种革兰阳性菌(金黄色葡萄球菌和地衣芽孢杆菌)上进行了测试。总体而言,这些新化合物在革兰阴性菌上效果最佳——在这些菌种中穿透外膜的能力尤为关键。化合物6g再次成为领先者:其对大肠杆菌和铜绿假单胞菌的最低有效浓度与环丙沙星处于相近范围,并且对金黄色葡萄球菌仍具有合理活性,尽管在该菌上其效力低于原始药物。
对抗细菌群体并评估安全性
除了自由浮动的细胞外,细菌常以一层黏性共生体——生物膜形式隐藏,这使感染更顽固且更难根除。研究者发现6g能强烈抑制大肠杆菌生物膜,在阻止生长所需浓度下将生物膜减少96%,并在更低剂量下仍表现出显著活性。对一株正常的人乳腺细胞系所做的早期安全性检测显示,6g在远高于抗菌所需浓度的水平下并不表现明显毒性,这对后续开发是一个鼓舞的迹象,但距离完整的安全评估仍有很大差距。
窥视分子“握手”机制
为理解6g为何表现出色,团队利用计算建模研究该分子如何嵌入DNA旋转酶和拓扑异构酶IV的结合口袋。模拟显示6g形成了密集的相互作用网络——包括氢键、与带电氨基酸的接触以及与蛋白表面的紧密配合——这些相互作用比环丙沙星更强且更持久。对蛋白-药物复合体随时间运动的额外计算表明,6g有助于将酶结构保持在一种稳定、被“锁定”的状态,这与其强效的酶抑制行为一致。对吸收和代谢的其他分析显示其亲脂-亲水平衡和对肝酶的干扰在可接受范围内,但也提示该化合物在未经进一步优化的情况下可能不适合简单的口服给药。
这对未来抗生素可能意味着什么
综合来看,结果突出了化合物6g作为下一代抗生素有前景的起点。它被设计为同时关闭两个必需的细菌酶,显示出强效活性——尤其针对难治的革兰阴性菌——并能破坏保护性生物膜,同时在初步人体细胞测试中未见明显毒性。与此同时,其较大的分子量和预测的吸收有限意味着6g更应被视为一个先导骨架而非已完成的药物。通过进一步微调以改善其进入体内与进入细菌的能力,这种双重作用策略或可帮助延长类环丙沙星药物的有效期,并为抗耐药性感染提供新的治疗选择。
引用: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
关键词: 抗生素耐药, 环丙沙星衍生物, DNA旋转酶抑制剂, 拓扑异构酶IV, 革兰阴性细菌