Clear Sky Science · de
Design, Synthese und antibakterielle Bewertung einer neuen Reihe ciprofloxacinbasierter Verbindungen als mögliche doppelte Hemmer von DNA-Gyrase/Topoisomerase IV
Warum das bei Alltagsinfektionen wichtig ist
Antibiotikaresistenz macht einst routinemäßige Infektionen schwerer und teurer zu behandeln. Ciprofloxacin, ein Arbeitspferd unter den Antibiotika, das bei Harnwegs-, Darm- und Lungenerkrankungen eingesetzt wird, verliert gegenüber einigen Bakterien an Wirksamkeit. Diese Studie untersucht einen durchdachten Ansatz zur Verbesserung des Ciprofloxacin-Designs, sodass es Bakterien gleichzeitig an zwei entscheidenden Schwachstellen stärker treffen kann, was möglicherweise den Vormarsch der Resistenz verlangsamt und die Behandlung hartnäckiger Infektionen verbessert.
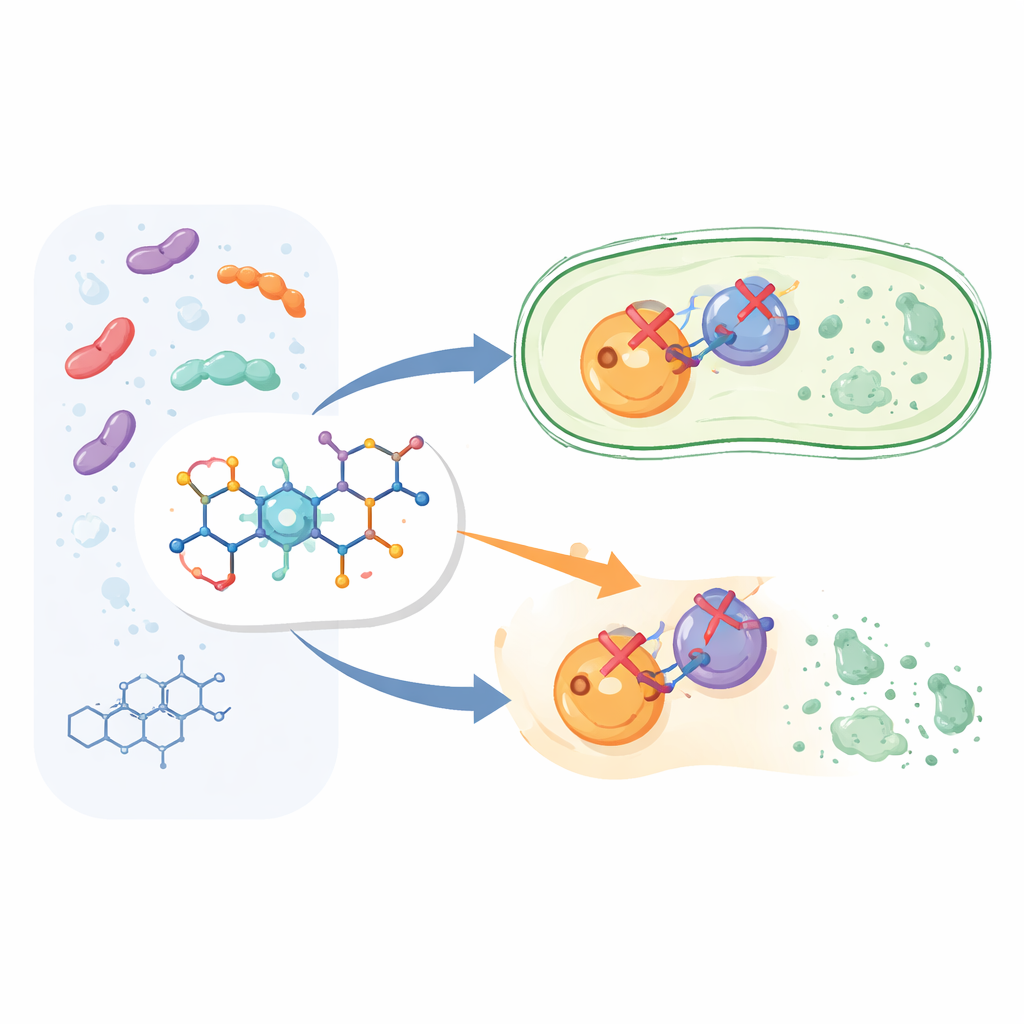
Eine schlauere Variante eines vertrauten Medikaments entwickeln
Statt ein völlig neues Medikament von Grund auf zu entwickeln, veränderten die Forscher die Struktur von Ciprofloxacin, einem Mitglied der weit verbreiteten Fluorchinolon-Familie. Sie behielten den Kern von Ciprofloxacin bei, der für die bakterizide Wirkung bekannt ist, und befestigten an einer definierten Position des Moleküls ein zusätzliches chemisches Fragment, ein Aryl-Pyridon. So entstanden zwölf neue Verbindungen, bezeichnet als 6a bis 6l. Die Idee war, dass dieser zusätzliche „Griff“ dem Wirkstoff helfen würde, seine bakteriellen Zielstrukturen stärker und vielseitiger zu fixieren als Standard-Ciprofloxacin.
Zwei bakterielle Lebensadern gleichzeitig ins Visier
Bakterien sind auf zwei eng verwandte Enzyme angewiesen, DNA-Gyrase und Topoisomerase IV, um ihre DNA beim Wachstum und bei der Zellteilung zu verwalten. Ciprofloxacin stört diese Enzyme bereits, allerdings nicht mit gleicher Effizienz. Die neuen Verbindungen wurden so entworfen, dass sie beide Ziele gleichzeitig stark blockieren, was es Bakterien erschweren sollte, allein durch Mutationen eines Enzyms zu entkommen. In Enzymtests mit Proteinen aus Escherichia coli inhibierten die meisten neuen Moleküle DNA-Gyrase und Topoisomerase IV in nützlichen Konzentrationen. Ein Stoff, genannt 6g, stach hervor: Er hemmte die DNA-Gyrase etwas besser als Ciprofloxacin und blockierte Topoisomerase IV etwa siebenmal stärker, wodurch er das stärkste „Dual‑Action“-Molekül der Reihe war.
Die neuen Moleküle gegen Bakterien testen
Anschließend prüfte das Team, ob die verbesserten Enzymwerte sich in einer stärkeren Wirkung gegen im Labor gezüchtete Bakterien niederschlagen. Ausgewählte Spitzenkandidaten, darunter 6d, 6f, 6g, 6i und 6l, wurden gegen zwei gramnegative Spezies (E. coli und Pseudomonas aeruginosa) und zwei grampositive Spezies (Staphylococcus aureus und Bacillus subtilis) getestet. Insgesamt zeigten diese neuen Verbindungen die beste Wirksamkeit gegen gramnegative Bakterien, bei denen die Fähigkeit, die Außenmembran zu durchdringen, besonders wichtig ist. Verbindungsstoff 6g erwies sich erneut als Spitzenreiter: Seine minimalen Wirkdosen gegen E. coli und P. aeruginosa lagen im gleichen Bereich wie die von Ciprofloxacin, und er blieb gegen S. aureus mäßig aktiv, wenn auch weniger potent als das Originalmedikament.
Gegen bakterielle Gemeinschaften kämpfen und Sicherheit prüfen
Abgesehen von frei schwebenden Zellen verstecken sich Bakterien häufig in schleimigen Gemeinschaften, sogenannten Biofilmen, die Infektionen hartnäckiger und schwerer zu beseitigen machen. Die Forscher fanden heraus, dass 6g E. coli-Biofilme stark unterdrückt: Er reduzierte sie um 96 Prozent bei der gleichen Konzentration, die auch das Wachstum stoppte, und zeigte bei niedrigeren Dosen weiterhin bemerkenswerte Aktivität. Erste Sicherheitstests in einer normalen menschlichen Brustzelllinie deuteten darauf hin, dass 6g bei weit über den antibakteriell wirksamen Konzentrationen nicht toxisch ist — ein ermutigendes Zeichen für die weitere Entwicklung, obwohl dies keineswegs eine vollständige Sicherheitsbewertung ersetzt.
Einblick in den molekularen Händedruck
Um zu verstehen, warum 6g so gut abschneidet, nutzte das Team Computermodelle, um zu untersuchen, wie das Molekül in die Taschen von DNA-Gyrase und Topoisomerase IV passt. Simulationen zeigten, dass 6g ein dichtes Netzwerk von Wechselwirkungen ausbildet — Wasserstoffbrücken, Kontakt mit geladenen Aminosäuren und enges Anlagern an die Proteinoberfläche — die stärker und beständiger sind als bei Ciprofloxacin. Zusätzliche Berechnungen zur Dynamik der Protein–Wirkstoff-Komplexe deuteten darauf hin, dass 6g dazu beiträgt, die Enzymstrukturen in einem stabilen, „verriegelten“ Zustand zu halten, was mit seiner starken Enzymhemmwirkung übereinstimmt. Weitere Analysen zu Absorption und Metabolismus wiesen auf ein akzeptables Fett–Wasser-Gleichgewicht und begrenzte Interferenzen mit Leberenzymen hin, deuteten aber auch an, dass die Verbindung ohne weitere Optimierung möglicherweise nicht ideal für eine einfache orale Verabreichung ist.
Was das für künftige Antibiotika bedeuten könnte
Insgesamt heben die Ergebnisse die Verbindung 6g als vielversprechenden Ausgangspunkt für Antibiotika der nächsten Generation hervor. Sie ist so konstruiert, zwei essentielle bakterielle Enzyme gleichzeitig lahmzulegen, zeigt starke Aktivität — insbesondere gegen widerstandsfähige gramnegative Arten — und stört schützende Biofilme, während sie in einem ersten Test an menschlichen Zellen nicht toxisch erscheint. Gleichzeitig sprechen ihre große Molekülgröße und die mäßig vorhergesagte Resorption dafür, 6g eher als Leitgerüst denn als fertiges Medikament zu betrachten. Mit weiterer Feinabstimmung, um die Aufnahme ins Organismus und in Bakterien zu verbessern, könnte dieser Doppelwirkungsansatz helfen, die Nutzungsdauer ciprofloxacinähnlicher Mittel zu verlängern und neue Optionen gegen resistente Infektionen zu bieten.
Zitation: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Schlüsselwörter: Antibiotikaresistenz, Ciprofloxacin-Derivate, DNA-Gyrase-Hemmer, Topoisomerase IV, Gramnegative Bakterien