Clear Sky Science · ar
تصميم وتخليق وتقييم نشاط مضاد للبكتيريا لسلسلة جديدة من مركبات مشتقة من سيبروفلوكساسين كمثبطات محتملة مزدوجة لهلجنة DNA/توبويزوميراز IV
لماذا هذا مهم للعدوى اليومية
تجعل مقاومة المضادات الحيوية العدوى التي كانت روتينية سابقًا أكثر صعوبة وتكلفة في العلاج. يفقد السيبروفلوكساسين، وهو مضاد حيوي أساسي يستخدم لعلاج التهابات المسالك البولية والأمعاء والرئتين، فعاليته ضد بعض البكتيريا. تستكشف هذه الدراسة طريقة ذكية لتحسين تصميم السيبروفلوكساسين بحيث يستهدف البكتيريا بقوة أكبر في نقطتي ضعف حيويتين في آن واحد، مما قد يبطئ تقدم المقاومة ويحسن علاج العدوى العنيدة.
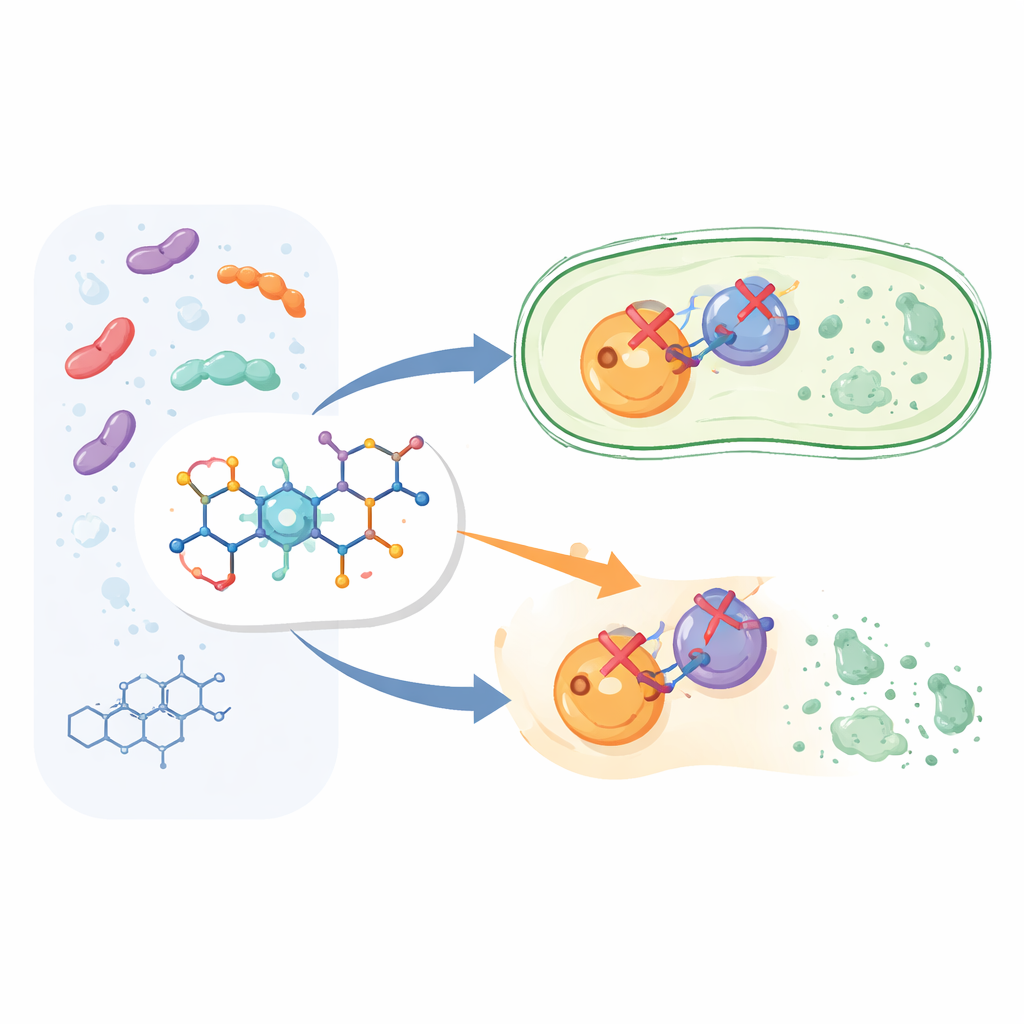
بناء نسخة أذكى من دواء مألوف
بدلاً من البدء بتصميم دواء جديد من الصفر، عدّل الباحثون بنية السيبروفلوكساسين، وهو عضو في عائلة الفلوروكينولونات واسعة الاستخدام. احتفظوا بالهيكل الأساسي للسيبروفلوكساسين المعروف بقدرته على قتل البكتيريا، ثم أضافوا قطعة كيميائية إضافية تسمى أريل بيريدون في موضع محدد من الجزيء. أنتج هذا اثني عشر مركبًا جديدًا، عُنِيت بالأرقام 6a إلى 6l. الفكرة كانت أن هذه «المقبضة» الإضافية ستساعد الدواء على الالتصاق بأهدافه البكتيرية بقوة أكبر وبطريقة أكثر تنوعًا من السيبروفلوكساسين القياسي.
استهداف خيطين حيويين للبكتيريا في آن واحد
تعتمد البكتيريا على إنزيمين مرتبطين ارتباطًا وثيقًا، هما حلزون DNA (DNA gyrase) وتوبويزوميراز IV، لإدارة حمضها النووي أثناء النمو والانقسام. يتداخل السيبروفلوكساسين بالفعل مع هذين الإنزيمين، لكن ليس بنفس الدرجة. صُممت المركبات الجديدة لتكون مثبطات قوية لكلا الهدفين في الوقت نفسه، مما يصعّب على البكتيريا الهروب عبر طفرات في إنزيم واحد فقط. في اختبارات الإنزيم باستخدام بروتينات إيشرشيا كولاي، قام معظم الجزيئات الجديدة بتثبيط حلزون DNA وتوبويزوميراز IV بمستويات مفيدة. برز مركب واحد، يُدعى 6g: فقد منع حلزون DNA أفضل قليلاً من السيبروفلوكساسين وغطى توبويزوميراز IV بقوة أكبر بنحو سبع مرات، مما جعله أقوى جزيء «ذو نشاط مزدوج» في المجموعة.
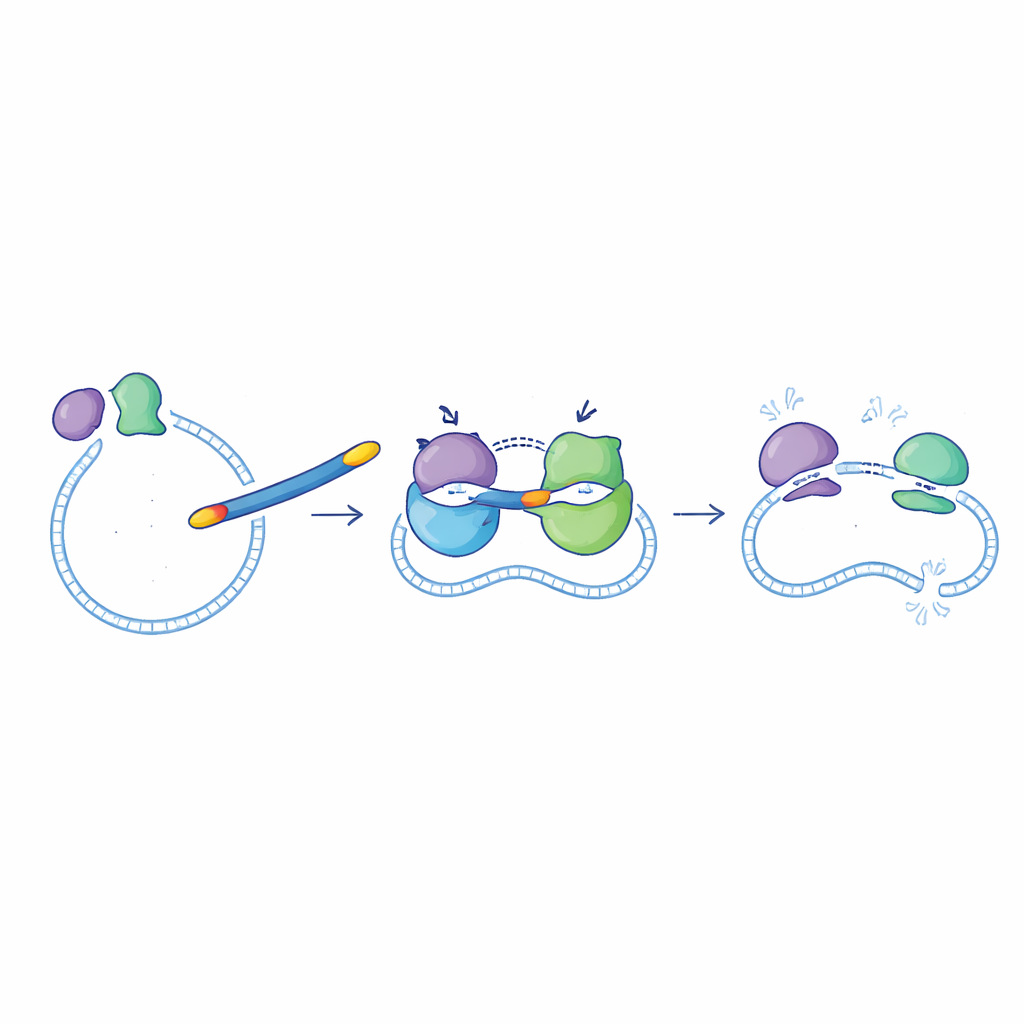
اختبار الجزيئات الجديدة ضد البكتيريا
ثم تحقق الفريق مما إذا كانت تحسينات الإنزيم تتحول إلى أداء أفضل ضد البكتيريا الحقيقية المزروعة في المختبر. اُختبر أبرز الأداءين، بما في ذلك 6d و6f و6g و6i و6l، ضد نوعين سالبي الغرام (E. coli وPseudomonas aeruginosa) ونوعين موجبي الغرام (Staphylococcus aureus وBacillus subtilis). عمومًا، عملت هذه المركبات الجديدة بشكل أفضل ضد البكتيريا سالبة الغرام، حيث تكون قدرتها على عبور الغشاء الخارجي مهمة بشكل خاص. برز المركب 6g مرة أخرى كالأفضل: كانت جرعاته الفعالة الدنيا ضد E. coli وP. aeruginosa في نفس مدى السيبروفلوكساسين، وبقي نشطًا بشكل معقول ضد S. aureus، وإن كان أقل فعالية هناك مقارنةً بالدواء الأصلي.
مكافحة المجتمعات البكتيرية وفحص السلامة
بعيدًا عن الخلايا الطافية الحرة، تختبئ البكتيريا غالبًا في مجتمعات مخاطية تُسمى الأغشية الحيوية (biofilms)، التي تجعل العدوى أكثر استمرارًا وصعوبة في الإزالة. وجد الباحثون أن 6g خفّض أغشية E. coli الحيوية بشدة، مقتطعًا منها 96 بالمئة عند نفس التركيز المطلوب لإيقاف النمو، وما زال يُظهر نشاطًا ملحوظًا عند جرعات أقل. أشارت فحوصات السلامة الأولية على سلالة خلوية بشرية طبيعية من نسيج الثدي إلى أن 6g ليس سامًا عند مستويات أعلى بكثير من تلك اللازمة للتأثير على البكتيريا، وهي علامة مشجعة للتطوير المستقبلي، وإن كانت بعيدة عن تقييم سلامة كامل.
النظر داخل المصافحة الجزيئية
لفهم سبب أداء 6g الجيد، استخدم الفريق النمذجة الحاسوبية لفحص كيفية انسجام الجزيء داخل جيوب حلزون DNA وتوبويزوميراز IV. أظهرت المحاكيات أن 6g يشكل شبكة كثيفة من التفاعلات—روابط هيدروجينية، اتصال مع أحماض أمينية مشحونة، وتراصف محكم مع سطح البروتين—تتسم بأنها أقوى وأكثر ثباتًا من تلك الخاصة بالسيبروفلوكساسين. أشارت حسابات إضافية لحركة مركبات البروتين–الدواء عبر الزمن إلى أن 6g يساعد في تثبيت هياكل الإنزيم في حالة محكمة ومقفلة، وهو ما يتوافق مع سلوكه القوي كمثبط للإنزيم. أما تحليلات الامتصاص والأيض فقد لفتت إلى توازن دهني–مائي مقبول وتداخل محدود مع إنزيمات الكبد، لكنها أيضاً ألمحت إلى أن المركب قد لا يكون مثاليًا للجرعات الفموية البسيطة دون مزيد من التحسين.
ماذا قد يعني هذا للمضادات الحيوية المستقبلية
تسلط النتائج بضعةً مجتمعةً الضوء على المركب 6g كنقطة انطلاق واعدة للمضادات الحيوية من الجيل القادم. فهو مُصمم لإيقاف إنزيمين بكتيريين أساسيين في آن واحد، ويظهر نشاطًا قويًا—لا سيما ضد أنواع سالبة الغرام المقاومة—ويعيق الأغشية الحيوية الواقية، وكل ذلك مع ظهوره غير سام في اختبار خلوي بشري أولي. في المقابل، فإن حجمه الكبير وتوقعات امتصاص متواضعة تجعله أنسب لأن يُنظر إليه كساس للقياس (lead scaffold) أكثر من كونه دواء نهائي. مع تحسينات إضافية لتعزيز طريقة دخوله إلى الجسم والبكتيريا، قد تساعد هذه المقاربة ذات العمل المزدوج في إطالة العمر المفيد لأدوية شبيهة بالسيبروفلوكساسين وتقديم خيارات جديدة ضد العدوى المقاومة.
الاستشهاد: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
الكلمات المفتاحية: مقاومة المضادات الحيوية, مشتقات السيبروفلوكساسين, مثبطات حلزون DNA (DNA gyrase), توبويزوميراز IV, بكتيريا سالبة الغرام