Clear Sky Science · ru
Дизайн, синтез и оценка антибактериальной активности новой серии соединений на основе ципрофлоксацина как потенциальных двойных ингибиторов ДНК-гиразы/топоизомеразы IV
Почему это важно для повседневных инфекций
Резистентность к антибиотикам делает когда-то рутинные инфекции сложнее и дороже в лечении. Ципрофлоксацин, широко используемый антибиотик при инфекциях мочевых путей, кишечника и легких, теряет эффективность против некоторых бактерий. В этом исследовании изучается хитрый способ улучшить конструкцию ципрофлоксацина так, чтобы он поражал бактерии одновременно по двум жизненно важным уязвимым местам, что потенциально может замедлить распространение резистентности и улучшить лечение упорных инфекций.
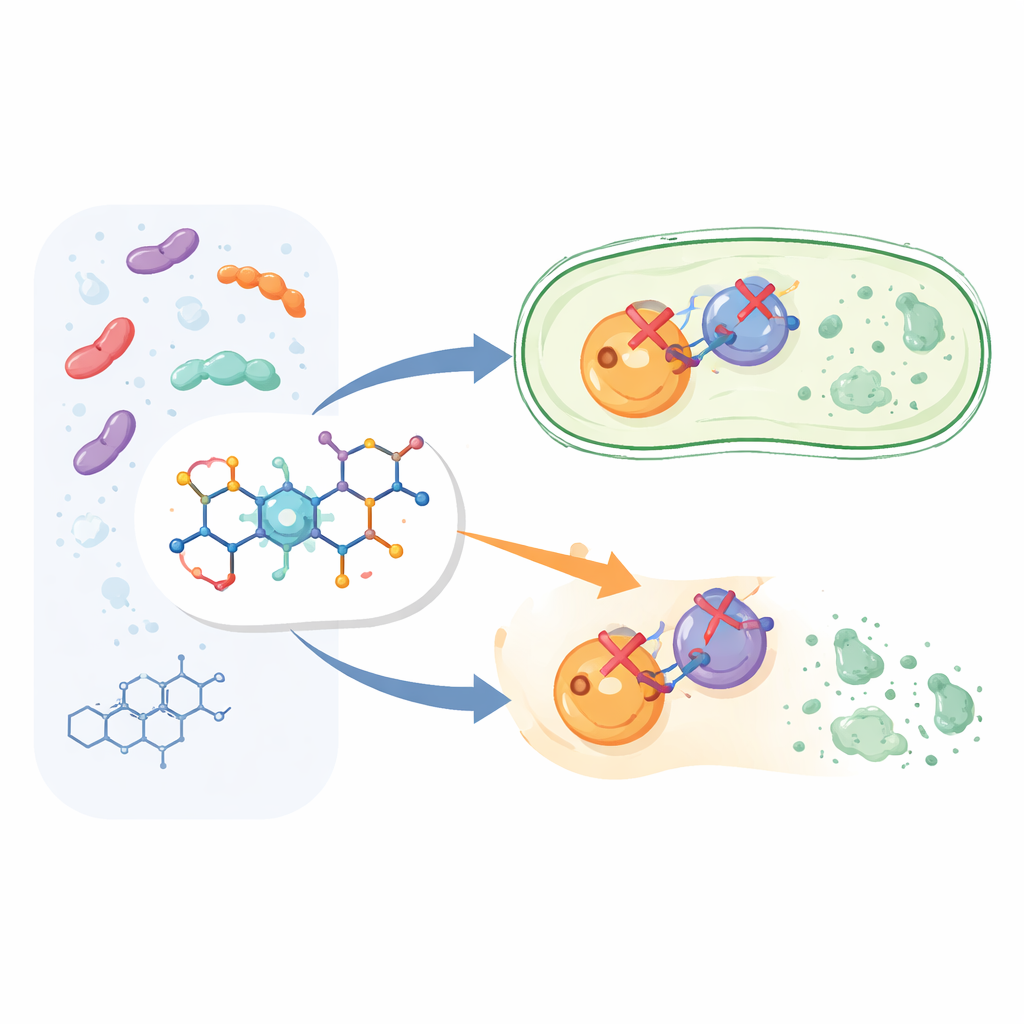
Создание более умной версии знакомого препарата
Вместо того чтобы начинать совершенно новый препарат с нуля, исследователи модифицировали структуру ципрофлоксацина, представителя широко используемого семейства фторхинолонов. Они сохранили ядро ципрофлоксацина, известное своей бактерицидной активностью, и прикрепили дополнительную химическую фрагмент — арилпиридон — в определенном положении молекулы. Это дало двенадцать новых соединений, обозначенных как 6a–6l. Идея заключалась в том, что эта дополнительная «ручка» поможет препарату прочнее и более универсально сцепляться с бактериальными мишенями по сравнению со стандартным ципрофлоксацином.
Атака по двум бактериальным «линиям жизни» одновременно
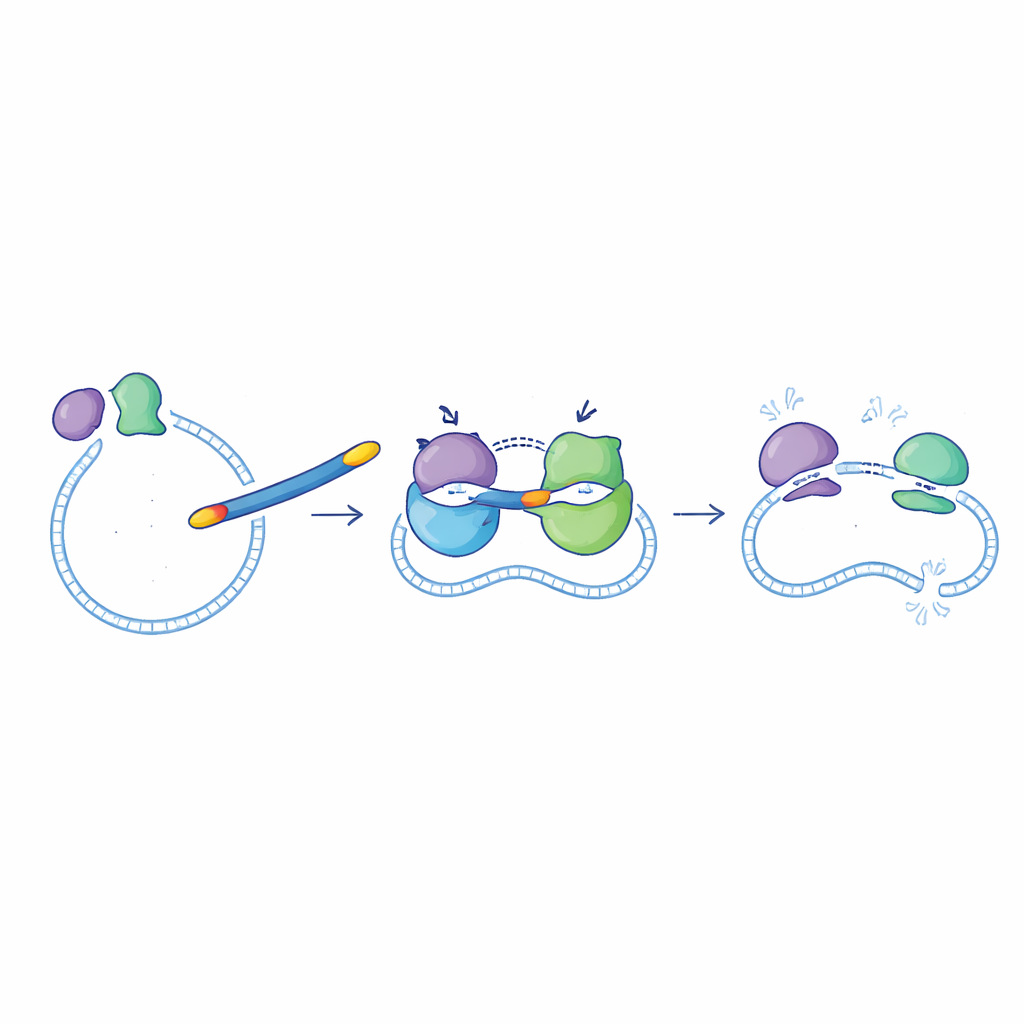
Бактерии полагаются на два тесно родственных фермента — ДНК-гиразу и топоизомеразу IV — чтобы управлять своей ДНК в процессе роста и деления. Ципрофлоксацин уже вмешивается в работу этих ферментов, но не одинаково эффективно. Новые соединения были разработаны как сильные блокаторы обеих мишеней одновременно, что должно усложнить бактериям путь к ускользанию путем мутации только одного фермента. В ферментных тестах с белками Escherichia coli большинство новых молекул ингибировали ДНК-гиразу и топоизомеразу IV на полезных уровнях. Одно соединение, обозначенное как 6g, выделилось: оно немного сильнее блокировало ДНК-гиразу по сравнению с ципрофлоксацином и подавляло активность топоизомеразы IV примерно в семь раз сильнее, что сделало его самым мощным «двойным» молекулой в наборе.
Испытание новых молекул на бактериях
Затем команда проверила, перенеслись ли улучшения в ферментных тестах на реальные бактерии, выращенные в лаборатории. Отобранные лидеры, включая 6d, 6f, 6g, 6i и 6l, тестировали против двух грамотрицательных видов (E. coli и Pseudomonas aeruginosa) и двух грамположительных видов (Staphylococcus aureus и Bacillus subtilis). В целом эти новые соединения оказались наиболее эффективны против грамотрицательных бактерий, где их способность пересекать наружную мембрану особенно важна. Соединение 6g снова проявило себя как лидер: минимальные эффективные концентрации против E. coli и P. aeruginosa были в том же диапазоне, что и у ципрофлоксацина, и оно сохраняло разумную активность против S. aureus, хотя там было менее мощным, чем исходный препарат.
Борьба с бактериальными сообществами и проверка безопасности
Помимо плавающих в среде клеток, бактерии часто укрываются в слизистых сообществах — биопленках, которые делают инфекции более стойкими и трудными для устранения. Исследователи обнаружили, что 6g сильно подавлял биопленки E. coli, сокращая их на 96 процентов при той же концентрации, что и для остановки роста, и сохранял заметную активность при более низких дозах. Ранние проверки безопасности в нормальной линии человеческих молочных клеток показали, что 6g не токсичен при уровнях, значительно превышающих те, которые необходимы для воздействия на бактерии — обнадеживающий признак для дальнейшей разработки, хотя это далеко не полный анализ безопасности.
Взгляд на молекулярное «пожатие руки»
Чтобы понять, почему 6g работает так хорошо, команда использовала компьютерное моделирование, чтобы изучить, как молекула входит в карманы ДНК-гиразы и топоизомеразы IV. Симуляции показали, что 6g формирует плотную сеть взаимодействий — водородных связей, контактов с заряженными аминокислотами и плотного упакования вдоль поверхности белка — которые сильнее и более устойчивы, чем у ципрофлоксацина. Дополнительные расчеты движения комплексов белок–препарат во времени показали, что 6g способствует удержанию структуры ферментов в стабильном, «заблокированном» состоянии, что согласуется с его мощным ингибирующим эффектом. Другие анализы абсорбции и метаболизма указывали на приемлемый баланс жиро/водорастворимости и ограниченное вмешательство в печеночные ферменты, но также намекали на то, что соединение может быть не идеальным для простой пероральной дозировки без дальнейшей оптимизации.
Что это может значить для будущих антибиотиков
В сумме результаты выделяют соединение 6g как перспективную отправную точку для антибиотиков следующего поколения. Оно сконструировано для одновременного подавления двух незаменимых бактериальных ферментов, демонстрирует сильную активность — особенно против стойких грамотрицательных видов — и нарушает защитные биопленки, при этом в начальном тесте на человеческих клетках не проявляет токсичности. Вместе с тем его крупный размер и умеренные прогнозируемые показатели всасывания означают, что 6g следует рассматривать скорее как лид-скелет, чем как готовый лекарственный препарат. При дальнейшей доработке, направленной на улучшение проникновения в организм и в бактерии, этот подход двойного действия может помочь продлить полезную жизнь лекарств, подобных ципрофлоксацину, и предложить новые варианты против резистентных инфекций.
Цитирование: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Ключевые слова: резистентность к антибиотикам, производные ципрофлоксацина, ингибиторы ДНК-гиразы, топоизомераза IV, грамотрицательные бактерии