Clear Sky Science · it
Progettazione, sintesi e valutazione antibatterica di una nuova serie di composti a base di ciprofloxacina come possibili inibitori duali della DNA girasi/topoisomerasi IV
Perché questo è importante per le infezioni di tutti i giorni
La resistenza agli antibiotici rende più difficili e costose da trattare infezioni che una volta erano di routine. La ciprofloxacina, un antibiotico molto usato per infezioni urinarie, intestinali e polmonari, sta perdendo efficacia contro alcuni batteri. Questo studio esplora un modo intelligente per aggiornare il progetto della ciprofloxacina in modo che possa colpire i batteri più duramente su due punti deboli vitali contemporaneamente, rallentando potenzialmente la diffusione della resistenza e migliorando il trattamento delle infezioni ostinate.
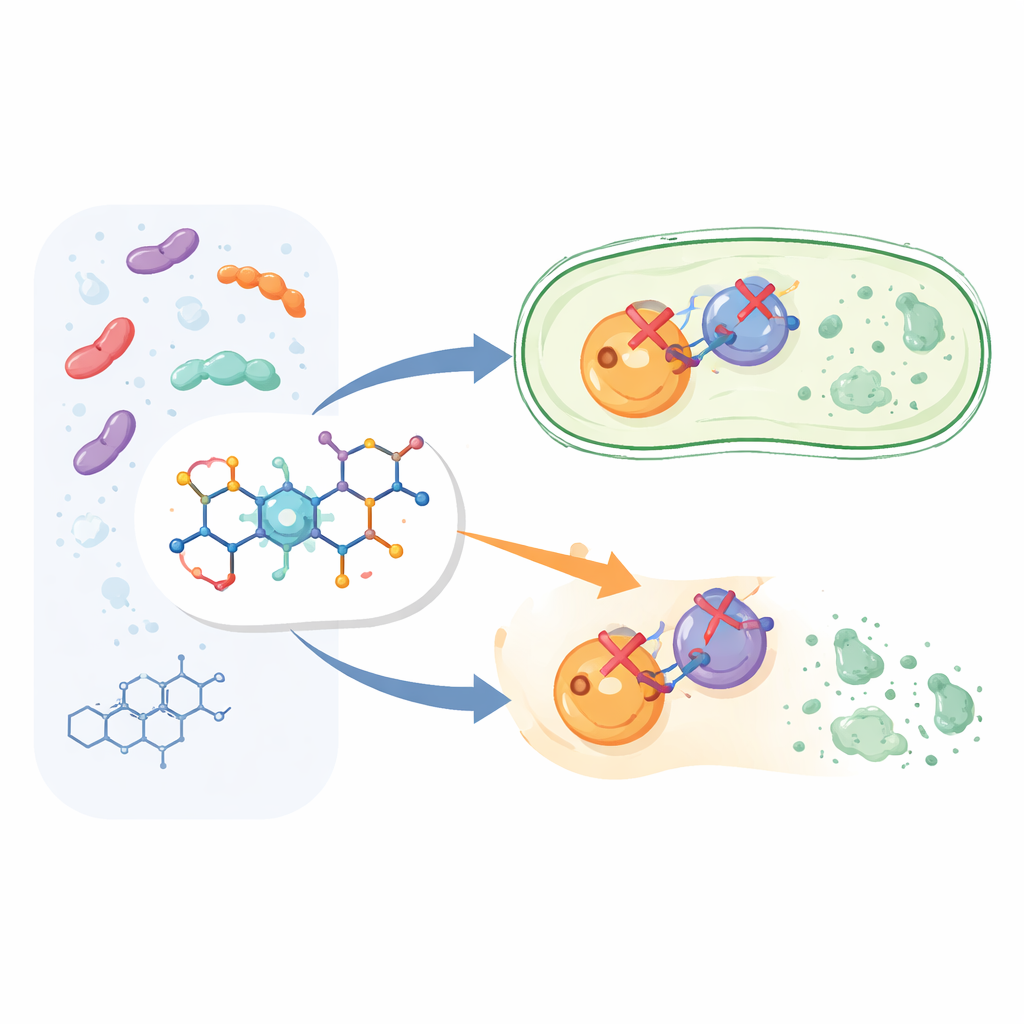
Costruire una versione più intelligente di un farmaco familiare
Invece di partire da zero con un nuovo farmaco, i ricercatori hanno modificato la struttura della ciprofloxacina, membro della famiglia dei fluorochinoloni ampiamente usata. Hanno mantenuto il nucleo della ciprofloxacina noto per uccidere i batteri, quindi hanno aggiunto un frammento chimico aggiuntivo chiamato aril-piridone in una posizione specifica della molecola. Ciò ha prodotto dodici nuovi composti, etichettati 6a fino a 6l. L’idea era che questa «maniglia» extra aiutasse il farmaco ad agganciarsi ai bersagli batterici in modo più forte e più versatile rispetto alla ciprofloxacina standard.
Colpire contemporaneamente due linee di vita batteriche
I batteri dipendono da due enzimi strettamente correlati, la DNA girasi e la topoisomerasi IV, per gestire il loro DNA durante crescita e divisione. La ciprofloxacina interferisce già con questi enzimi, ma non in modo uguale. I nuovi composti sono stati progettati per bloccare entrambi i bersagli con forza allo stesso tempo, rendendo più difficile per i batteri sfuggire mediante la mutazione di un singolo enzima. Nei test enzimatici con proteine di Escherichia coli, la maggior parte delle nuove molecole ha inibito la DNA girasi e la topoisomerasi IV a livelli utili. Un composto, chiamato 6g, si è distinto: ha bloccato la DNA girasi leggermente meglio della ciprofloxacina e ha inibito la topoisomerasi IV circa sette volte più efficacemente, rendendolo la molecola «doppia azione» più potente del gruppo.
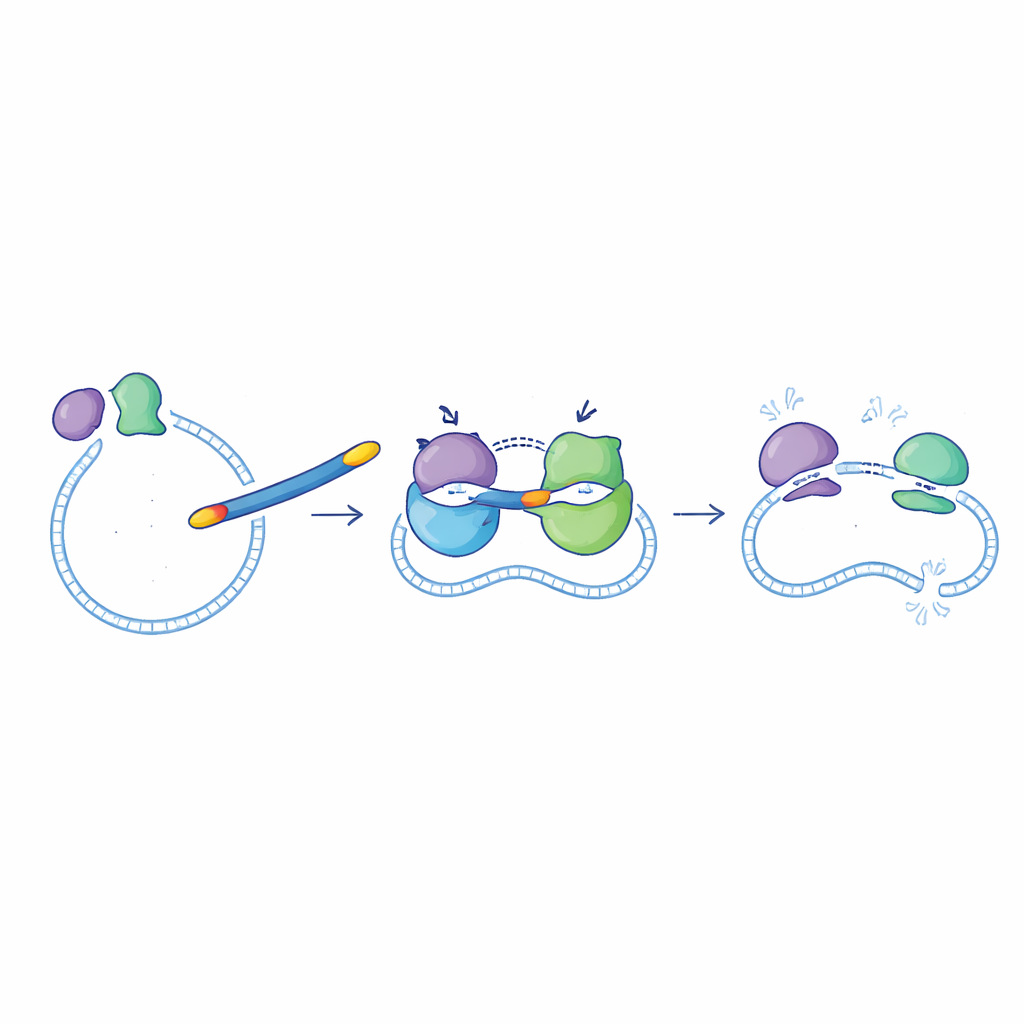
Mettere alla prova le nuove molecole contro i batteri
Il team ha poi verificato se i miglioramenti enzimatici si traducessero in una migliore attività contro batteri coltivati in laboratorio. I migliori candidati selezionati, tra cui 6d, 6f, 6g, 6i e 6l, sono stati testati contro due specie Gram-negative (E. coli e Pseudomonas aeruginosa) e due specie Gram-positive (Staphylococcus aureus e Bacillus subtilis). Complessivamente, questi nuovi composti hanno funzionato meglio contro i Gram-negativi, dove la capacità di attraversare la membrana esterna è particolarmente importante. Anche in questo caso il composto 6g è emerso come il leader: le sue dosi minime efficaci contro E. coli e P. aeruginosa erano della stessa entità della ciprofloxacina, ed è rimasto ragionevolmente attivo contro S. aureus, sebbene meno potente rispetto al farmaco originale.
Combattere le comunità batteriche e sondare la sicurezza
Oltre alle cellule libere, i batteri spesso si nascondono in comunità vischiose chiamate biofilm, che rendono le infezioni più persistenti e difficili da eradicare. I ricercatori hanno scoperto che 6g sopprime fortemente i biofilm di E. coli, riducendoli del 96 percento alla stessa concentrazione necessaria per arrestare la crescita, e mostrando ancora una attività notevole a dosi inferiori. I controlli di sicurezza iniziali su una linea cellulare umana normale mammaria hanno suggerito che 6g non è tossico a livelli molto superiori a quelli necessari per colpire i batteri, un segnale incoraggiante per lo sviluppo futuro, sebbene lontano da una valutazione completa della sicurezza.
Esaminare la stretta di mano molecolare
Per capire perché 6g rende così bene, il team ha usato modelli computazionali per esaminare come la molecola si inserisce nelle tasche della DNA girasi e della topoisomerasi IV. Le simulazioni hanno mostrato che 6g forma una fitta rete di interazioni — legami a idrogeno, contatti con amminoacidi caricati e un impacchettamento aderente contro la superficie proteica — che sono più forti e più persistenti rispetto a quelli della ciprofloxacina. Calcoli aggiuntivi sul movimento delle complesse proteina–farmaco nel tempo hanno suggerito che 6g aiuta a mantenere le strutture enzimatiche in uno stato stabile e bloccato, coerente con la sua potente attività inibitoria. Altre analisi su assorbimento e metabolismo indicano un equilibrio lipofilia–idrofilia accettabile e un’interferenza limitata con gli enzimi epatici, ma suggeriscono anche che il composto potrebbe non essere ideale per una semplice somministrazione orale senza ulteriori ottimizzazioni.
Cosa potrebbe significare per i futuri antibiotici
Nel complesso, i risultati evidenziano il composto 6g come un punto di partenza promettente per antibiotici di nuova generazione. È progettato per spegnere due enzimi batterici essenziali contemporaneamente, mostra una forte attività — specialmente contro specie Gram-negative ostiche — e perturba i biofilm protettivi, apparendo al contempo non tossico in un test cellulare umano iniziale. Allo stesso tempo, la sua grandezza e il modesto assorbimento previsto fanno sì che 6g sia meglio considerato come uno scaffold guida piuttosto che come un medicinale finito. Con ulteriori perfezionamenti per migliorare il suo ingresso nell’organismo e nei batteri, questo approccio a doppia azione potrebbe contribuire a prolungare la vita utile dei farmaci simili alla ciprofloxacina e offrire nuove opzioni contro le infezioni resistenti.
Citazione: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Parole chiave: resistenza agli antibiotici, derivati della ciprofloxacina, inibitori della DNA girasi, topoisomerasi IV, batteri Gram-negativi