Clear Sky Science · nl
Ontwerp, synthese en antibacteriële beoordeling van een nieuwe reeks ciprofloxacine-gebaseerde verbindingen als mogelijke dubbele DNA-gyrase/topoisomerase IV-remmers
Waarom dit belangrijk is voor alledaagse infecties
Antibioticaresistentie maakt infecties die ooit routinematig waren moeilijker en duurder te behandelen. Ciprofloxacine, een veelgebruikt antibioticum voor urine-, darm- en longinfecties, verliest effectiviteit tegen sommige bacteriën. Deze studie onderzoekt een slimme manier om het ontwerp van ciprofloxacine te verbeteren, zodat het bacteriën tegelijk op twee cruciale zwakke plekken kan treffen, wat mogelijk de opkomst van resistentie vertraagt en de behandeling van hardnekkige infecties verbetert.
Een slimmer variant van een bekend geneesmiddel bouwen
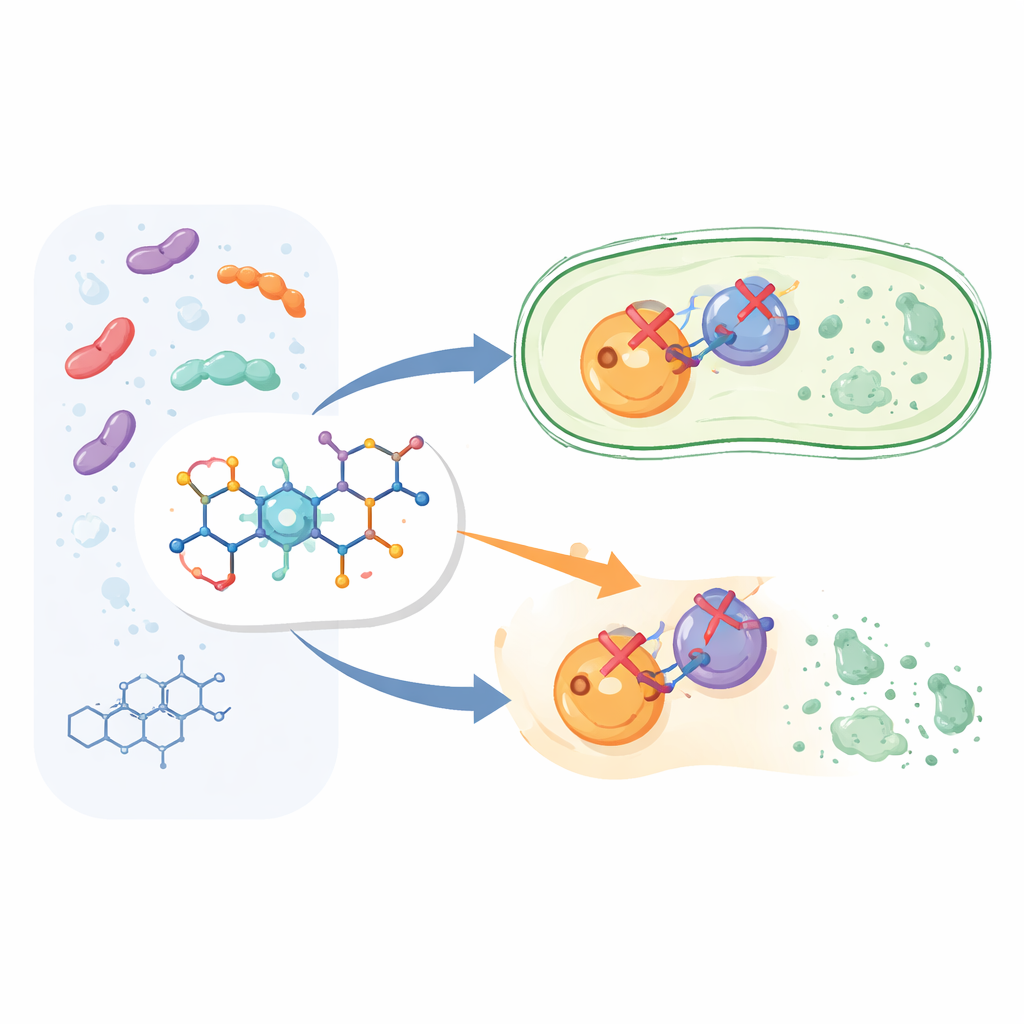
In plaats van een geheel nieuw geneesmiddel vanaf nul te ontwikkelen, pasten de onderzoekers de structuur van ciprofloxacine aan, een lid van de veelgebruikte klasse fluoroquinolonen. Ze behielden de kern van ciprofloxacine die bekendstaat om bacteriën te doden, en voegden een extra chemische fragment, een arylpyridon, toe op een specifieke positie van het molecuul. Dit leidde tot twaalf nieuwe verbindingen, aangeduid als 6a tot en met 6l. Het idee was dat dit extra “handvat” het middel zou helpen zijn bacteriële doelwitten steviger en op meer veelzijdige wijze vast te grijpen dan standaard ciprofloxacine.
Tegelijk twee bacteriële levenslijnen blokkeren
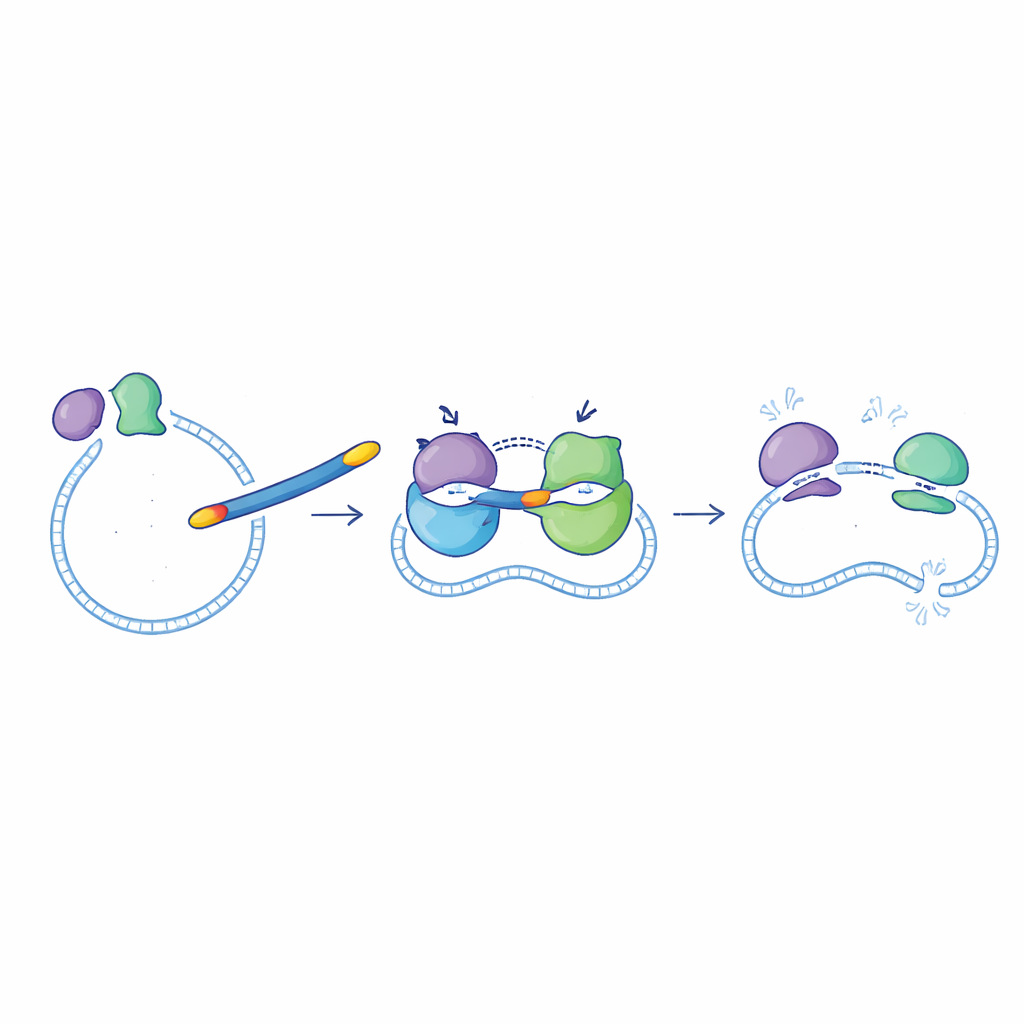
Bacteriën vertrouwen op twee nauw verwante enzymen, DNA-gyrase en topoisomerase IV, om hun DNA te beheren tijdens groei en celdeling. Ciprofloxacine verstoort deze enzymen al, maar niet altijd even effectief. De nieuwe verbindingen zijn ontworpen als sterke blokkers van beide doelwitten tegelijk, waardoor het voor bacteriën moeilijker wordt om te ontsnappen door slechts één enzym te muteren. In enzymtests met eiwitten uit Escherichia coli remden de meeste nieuwe moleculen DNA-gyrase en topoisomerase IV op nuttige niveaus. Eén verbinding, 6g genoemd, stak er met kop en schouders bovenuit: zij remde DNA-gyrase iets beter dan ciprofloxacine en remde topoisomerase IV ongeveer zeven keer sterker, waardoor het de krachtigste “dubbelwerkende” molecule in de reeks was.
De nieuwe moleculen testen tegen bacteriën
Vervolgens controleerde het team of de verbeteringen op enzymniveau zich vertaalden naar betere prestaties tegen echte in het laboratorium gekweekte bacteriën. Uitgekozen koplopers, waaronder 6d, 6f, 6g, 6i en 6l, werden getest tegen twee gramnegatieve soorten (E. coli en Pseudomonas aeruginosa) en twee grampositieve soorten (Staphylococcus aureus en Bacillus subtilis). Over het algemeen werkten deze nieuwe verbindingen het beste tegen gramnegatieve bacteriën, waarbij hun vermogen om de buitenmembraan te passeren bijzonder belangrijk is. Verbinding 6g bleek opnieuw de koploper: de minimale effectieve doses tegen E. coli en P. aeruginosa lagen in hetzelfde bereik als ciprofloxacine, en het bleef redelijk actief tegen S. aureus, hoewel het daar minder potent was dan het oorspronkelijke middel.
Bestrijden van bacteriële gemeenschappen en veiligheidsonderzoek
Bacteriën zitten naast vrij zwevende cellen vaak verstopt in slijmachtige gemeenschappen die biofilms heten, waardoor infecties persistent zijn en moeilijker uit te roeien. De onderzoekers vonden dat 6g E. coli-biofilms sterk onderdrukte, met een reductie van 96 procent bij dezelfde concentratie die nodig was om groei te stoppen, en dat het nog steeds noemenswaardige activiteit toonde bij lagere doses. Vroege veiligheidstests in een normale menselijke borstcelijn suggereerden dat 6g niet toxisch is bij niveaus die veel hoger liggen dan die nodig zijn om bacteriën te beïnvloeden, een bemoedigend teken voor verdere ontwikkeling, maar verre van een volledige veiligheidsbeoordeling.
Inzoomen op de moleculaire handdruk
Om te begrijpen waarom 6g zo goed presteert, gebruikte het team computermodellering om te onderzoeken hoe het molecuul in de pocket van DNA-gyrase en topoisomerase IV past. Simulaties toonden aan dat 6g een dicht netwerk van interacties vormt — waterstofbruggen, contact met geladen aminozuren en nauw contact met het eiwitoppervlak — die sterker en blijvender zijn dan die van ciprofloxacine. Aanvullende berekeningen van hoe de eiwit–middelcomplexen in de tijd bewegen, suggereerden dat 6g helpt de enzymstructuren in een stabiele, vergrendelde toestand te houden, wat consistent is met zijn krachtige enzymremmende werking. Andere analyses van absorptie en metabolisme wezen op een acceptabele vet–water-balans en beperkte interferentie met leverenzymen, maar wezen ook op dat de verbinding zonder verdere optimalisatie mogelijk niet ideaal is voor eenvoudige orale toediening.
Wat dit kan betekenen voor toekomstige antibiotica
Gezamenlijk wijzen de resultaten op verbinding 6g als een veelbelovend uitgangspunt voor volgende generaties antibiotica. Het is ontworpen om twee essentiële bacteriële enzymen tegelijk uit te schakelen, toont sterke activiteit — vooral tegen hardnekkige gramnegatieve soorten — en verstoort beschermende biofilms, terwijl het in een eerste menselijke celtest niet toxisch lijkt. Tegelijkertijd maken de grote omvang en de matig voorspelde absorptie dat 6g beter gezien kan worden als een leidend bouwblok dan als een afgewerkt geneesmiddel. Met verdere verfijning om de opname in het lichaam en in bacteriën te verbeteren, kan deze dubbelwerkende benadering helpen de bruikbare levensduur van ciprofloxacine-achtige middelen te verlengen en nieuwe opties bieden tegen resistente infecties.
Bronvermelding: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Trefwoorden: antibioticaresistentie, ciprofloxacine-afgeleiden, DNA-gyraseremmers, topoisomerase IV, gramnegatieve bacteriën