Clear Sky Science · es
Diseño, síntesis y evaluación antibacteriana de una nueva serie de compuestos basados en ciprofloxacino como posibles inhibidores duales de la girasa de ADN/topoisomerasa IV
Por qué esto importa para las infecciones cotidianas
La resistencia a los antibióticos está haciendo que infecciones antes rutinarias sean más difíciles y costosas de tratar. La ciprofloxacino, un antibiótico fundamental usado para infecciones urinarias, intestinales y respiratorias, está perdiendo eficacia frente a algunas bacterias. Este estudio examina una vía ingeniosa para mejorar el diseño de la ciprofloxacino de modo que pueda atacar a las bacterias con mayor contundencia en dos puntos débiles vitales a la vez, lo que podría frenar el avance de la resistencia y mejorar el tratamiento de infecciones rebeldes.
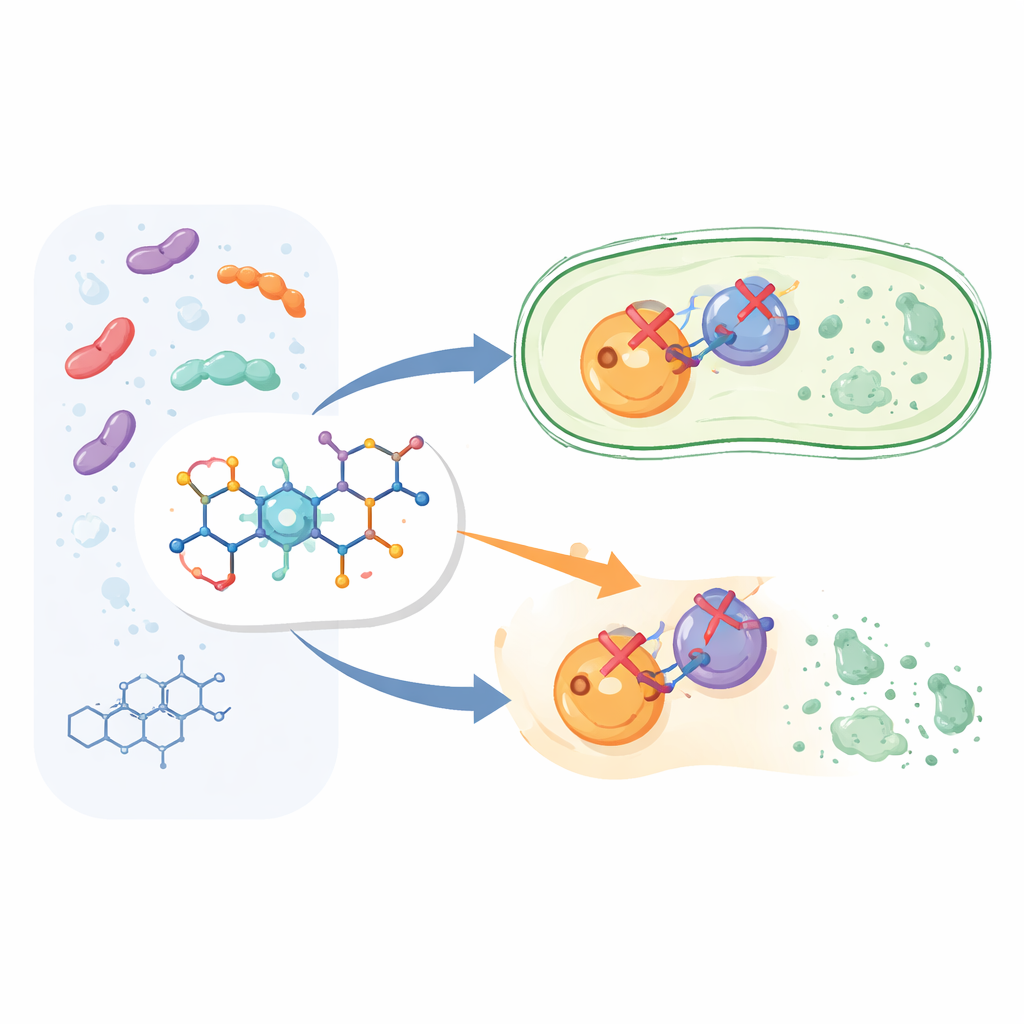
Construyendo una versión más inteligente de un fármaco conocido
En vez de empezar un fármaco completamente nuevo desde cero, los investigadores modificaron la estructura de la ciprofloxacino, miembro de la amplia familia de las fluoroquinolonas. Mantuvieron el núcleo de la ciprofloxacino conocido por matar bacterias y añadieron un fragmento químico adicional llamado aril-piridona en una posición específica de la molécula. Esto produjo doce nuevos compuestos, etiquetados 6a hasta 6l. La idea era que esta «asa» extra ayudaría al fármaco a sujetar sus dianas bacterianas con más fuerza y de forma más versátil que la ciprofloxacino estándar.
Apuntar a dos líneas vitales bacterianas a la vez
Las bacterias dependen de dos enzimas estrechamente relacionadas, la girasa de ADN y la topoisomerasa IV, para manejar su ADN mientras crecen y se dividen. La ciprofloxacino ya interfiere con estas enzimas, pero no por igual. Los nuevos compuestos se diseñaron para bloquear con fuerza ambas dianas al mismo tiempo, lo que debería dificultar que las bacterias escapen al mutar solo una enzima. En ensayos enzimáticos con proteínas de Escherichia coli, la mayor parte de las moléculas nuevas inhibieron la girasa de ADN y la topoisomerasa IV en niveles útiles. Un compuesto, denominado 6g, destacó: bloqueó la girasa de ADN algo mejor que la ciprofloxacino e inhibió la topoisomerasa IV aproximadamente siete veces con mayor potencia, convirtiéndolo en la molécula «de acción dual» más potente del conjunto.
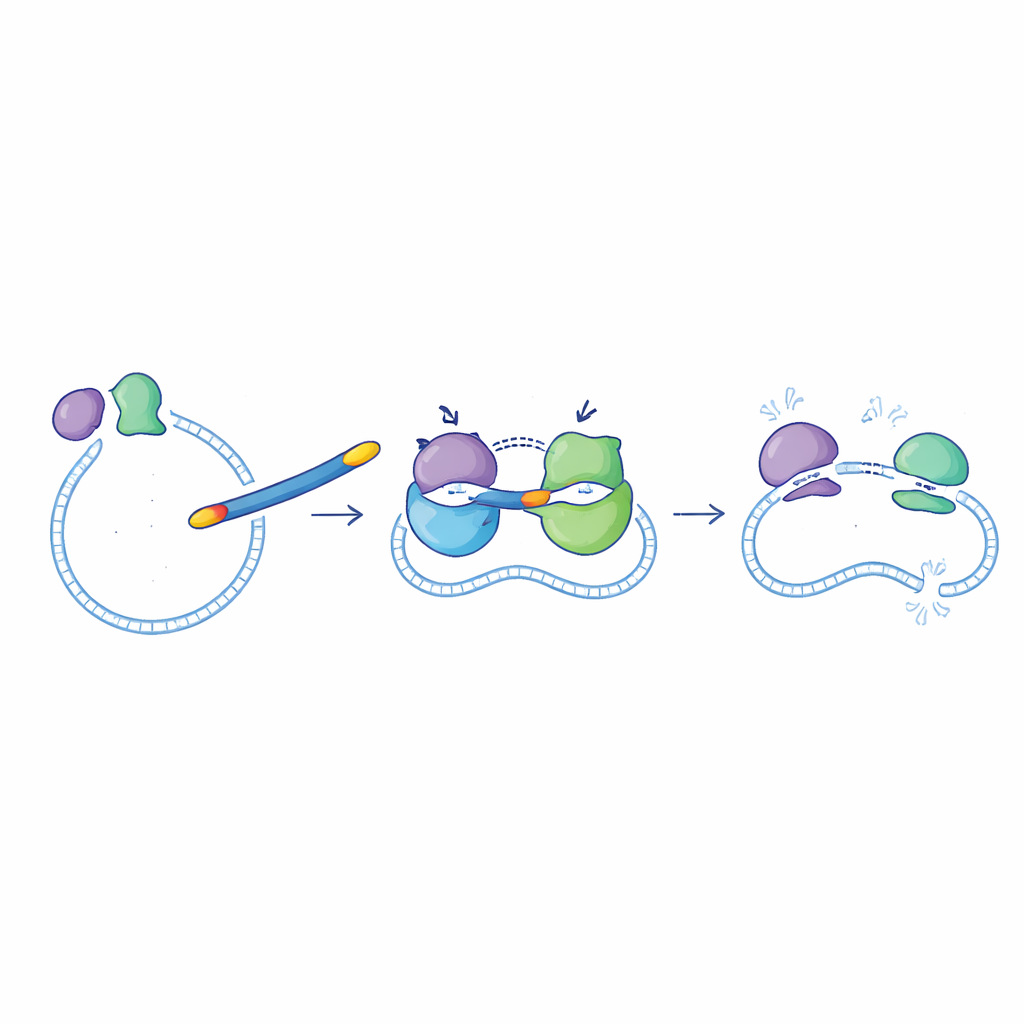
Poniendo a prueba las nuevas moléculas contra bacterias
El equipo comprobó luego si las mejoras observadas enzimáticamente se traducían en mejor rendimiento frente a bacterias reales cultivadas en el laboratorio. Se probaron los mejores candidatos, incluidos 6d, 6f, 6g, 6i y 6l, frente a dos especies Gram-negativas (E. coli y Pseudomonas aeruginosa) y dos Gram-positivas (Staphylococcus aureus y Bacillus subtilis). En general, estos nuevos compuestos funcionaron mejor contra bacterias Gram-negativas, donde su capacidad para cruzar la membrana externa es especialmente importante. El compuesto 6g volvió a emerger como el favorito: sus dosis mínimas efectivas contra E. coli y P. aeruginosa estaban en el mismo rango que la ciprofloxacino, y mantuvo actividad razonable frente a S. aureus, aunque fue menos potente allí que el fármaco original.
Combatir comunidades bacterianas e investigar la seguridad
Más allá de las células libres, las bacterias a menudo se ocultan en comunidades viscosas llamadas biopelículas, que hacen que las infecciones sean más persistentes y difíciles de erradicar. Los investigadores observaron que 6g suprimió fuertemente las biopelículas de E. coli, reduciéndolas en un 96 por ciento a la misma concentración necesaria para detener el crecimiento, y mostrando aún actividad notable a dosis más bajas. Controles iniciales de seguridad en una línea celular humana mamaria normal sugirieron que 6g no es tóxico a niveles mucho más altos que los necesarios para afectar a las bacterias, una señal alentadora para desarrollos futuros, aunque lejos de ser una evaluación de seguridad completa.
Mirando dentro del apretón molecular
Para entender por qué 6g funciona tan bien, el equipo utilizó modelado por ordenador para examinar cómo encaja la molécula en las cavidades de la girasa de ADN y la topoisomerasa IV. Las simulaciones mostraron que 6g forma una densa red de interacciones: enlaces de hidrógeno, contacto con aminoácidos cargados y empaquetamiento compacto contra la superficie de la proteína, que son más fuertes y persistentes que los de la ciprofloxacino. Cálculos adicionales sobre el movimiento de los complejos proteína‑fármaco a lo largo del tiempo sugirieron que 6g ayuda a mantener las estructuras enzimáticas en un estado estable y bloqueado, coherente con su potente bloqueo enzimático. Otros análisis sobre absorción y metabolismo apuntaron a un equilibrio lípido‑agua aceptable y una interferencia limitada con enzimas hepáticas, pero también sugirieron que el compuesto puede no ser ideal para una administración oral simple sin más optimización.
Qué podría significar esto para futuros antibióticos
En conjunto, los resultados destacan al compuesto 6g como un punto de partida prometedor para antibióticos de próxima generación. Está diseñado para bloquear dos enzimas bacterianas esenciales a la vez, muestra fuerte actividad—especialmente contra especies Gram-negativas difíciles—y perturba las biopelículas protectoras, todo ello sin parecer tóxico en una prueba inicial con células humanas. Al mismo tiempo, su gran tamaño y la absorción prevista moderada hacen que 6g deba considerarse más como un armazón líder que como un medicamento acabado. Con un ajuste fino adicional para mejorar cómo entra en el organismo y en las bacterias, este enfoque de acción dual podría ayudar a prolongar la vida útil de fármacos similares a la ciprofloxacino y ofrecer nuevas opciones contra infecciones resistentes.
Cita: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Palabras clave: resistencia a los antibióticos, derivados de ciprofloxacino, inhibidores de la girasa de ADN, topoisomerasa IV, bacterias Gram-negativas