Clear Sky Science · he
עיצוב, סינתזה והערכה אנטיבקטריאלית של סדרה חדשה של תרכובות מבוססות ציפרופלוקסצין כמעכבים כפולים אפשריים של DNA גיראז/טופואיזומראז IV
מדוע זה חשוב לזיהומים יומיומיים
עמידות לאנטיביוטיקה הופכת זיהומים שבעבר היו שגרתיים לקשים ויקרים יותר לטיפול. ציפרופלוקסצין, אנטיביוטיקה נפוצה הניתנת לזיהומי דרכי השתן, מערכת העיכול והריאות, מאבדת מהאפקטיביות שלה מול חלק מהחיידקים. המחקר הזה בוחן דרך חכמה לשדרג את מבנה הציפרופלוקסצין כך שיוכל לפגוע בחיידקים חזק יותר בשני חוליות חיוניות בו־זמנית, מה שעשוי להאט את התפתחות העמידות ולשפר את הטיפול בזיהומים עקשניים.
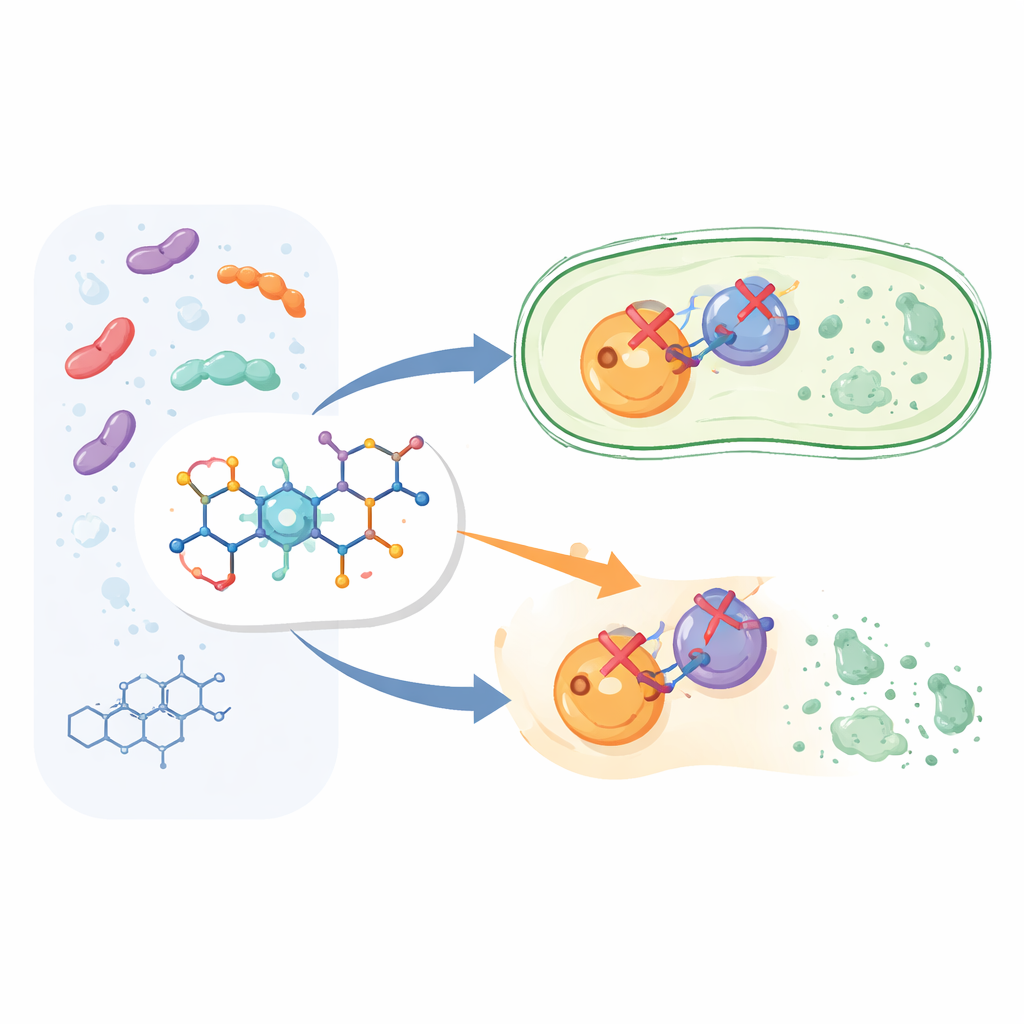
בנייה של גרסה חכמה יותר של תרופה מוכרת
במקום להתחיל תרופה חדשה מאפס, החוקרים שינו את המבנה של ציפרופלוקסצין, חבר במשפחת הפלורוכינולונים הנפוצה. הם שמרו על הליבה של הציפרופלוקסצין המוכרת כפעילה כנגד חיידקים, והוסיפו שבר כימי נוסף בשם אריל פירידון בעמדה מסוימת במולקולה. כך נוצרו שנים־עשר תרכובות חדשות, המסומנות 6a עד 6l. הרעיון היה שה"ידית" הנוספת הזו תעזור לתרופה לאחוז במטרות החיידק בחוזקה רבה יותר ובאופן מגוון יותר מאשר ציפרופלוקסצין הסטנדרטי.
מיקוד בשני קווי החיים של החיידק בו־זמנית
חיידקים מסתמכים על שתי אנזימים קרובים זה לזה, DNA גיראז וטופואיזומראז IV, לניהול ה‑DNA שלהם במהלך גדילה וחלוקה. ציפרופלוקסצין כבר מתערב בפעילות האנזימים הללו, אך לא באותה מידה. התרכובות החדשות עוצבו להיות מעכבים חזקים של שני היעדים בו־זמנית, מה שיפחית את הסיכוי שחיידקים יתחמקו באמצעות מוטציה באנזים אחד בלבד. בניסויים על אנזימים של Escherichia coli, רוב המולקולות החדשות עיכבו את ה‑DNA גיראז ואת טופואיזומראז IV ברמות שימושיות. תרכובת אחת, שכונתה 6g, בלטה: היא חסמה את ה‑DNA גיראז במעט יותר יעילות מציפרופלוקסצין והעכירה את טופואיזומראז IV בערך פי שבעה יותר חזק, מה שהפך אותה למולקולת ה"פעולה הכפולה" החזקה ביותר בערכה.
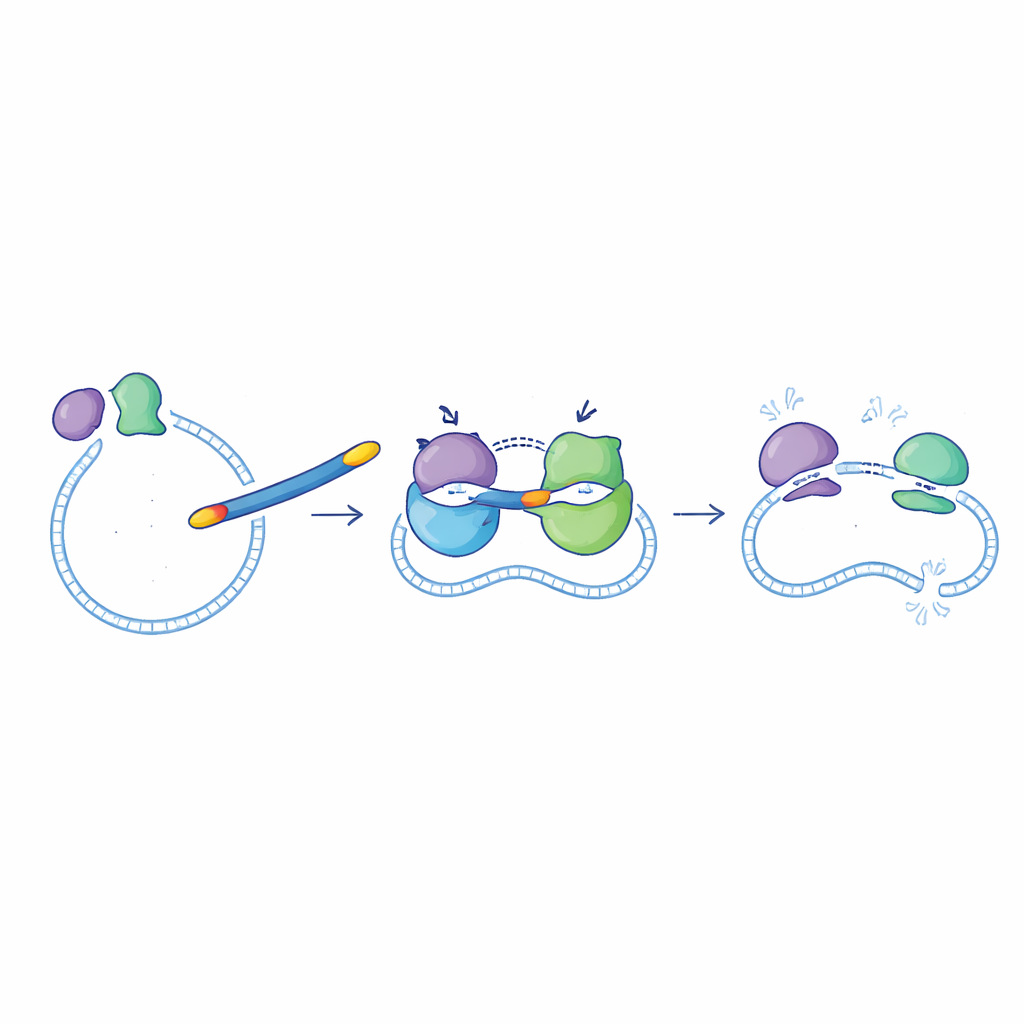
בדיקת המולקולות החדשות נגד חיידקים
הצוות בדק האם השיפורים באנזימים מתורגמים לביצועים טובים יותר נגד חיידקים אמיתיים בגידול מעבדה. מבין המובילים נבחרו 6d, 6f, 6g, 6i ו‑6l ונבדקו מול שני מינים גרם‑שליליים (E. coli ו‑Pseudomonas aeruginosa) ושני מינים גרם‑חיוביים (Staphylococcus aureus ו‑Bacillus subtilis). באופן כללי, התרכובות החדשות הראו פעילות טובה יותר נגד חיידקים גרם‑שליליים, שם יכולת לעבור את הממברנה החיצונית היא קריטית. שוב, 6g נצפה כמובילה: המינונים המינימליים היעילים שלה נגד E. coli ו‑P. aeruginosa היו בטווח דומה לציפרופלוקסצין, והיא נשארה פעילה באופן סביר נגד S. aureus, אם כי בעוצמה נמוכה יותר מהתרופה המקורית.
לחימה בקהילות חיידקיות ובחינת בטיחות ראשונית
מעבר לתאים חופשיים, חיידקים מסתתרים לעיתים בקהילות דביקות הנקראות ביופילמים, שהופכות זיהומים לעמידים וקשים לחיסול. החוקרים מצאו כי 6g דיכאה בחוזקה ביופילמים של E. coli, קיצוצה ב‑96 אחוזים בריכוז שעליו נעצר גדילה, ועדיין הראתה פעילות משמעותית במינונים נמוכים יותר. בדיקות בטיחות ראשוניות בתרבית של תאים נורמליים משד אנושי הראו כי 6g אינה רעילה ברמות גבוהות בהרבה מהן הנדרשות להשפעה על החיידקים — סימן מעודד לפיתוח עתידי, אם כי רחוק מהערכת בטיחות מקיפה.
מבט על הלחיצה המולקולרית
כדי להבין מדוע 6g מתפקדת כל כך טוב, הצוות השתמש במדידות ממוחשבות כדי לבחון כיצד המולקולה מתאימה לכיסים של ה‑DNA גיראז וטופואיזומראז IV. סימולציות הראו ש‑6g יוצר רשת צפופה של אינטראקציות — קשרי מימן, מגע עם חומצות אמינו טעונות ואריזה הדוקה על פני שטח החלבון — שהן חזקות ומתמשכות יותר מאלו של ציפרופלוקסצין. חישובים נוספים של דינמיקת הקומפלקסים חלבון‑תרופה לאורך זמן הציעו ש‑6g מסייעת לייצב את המבנים האנזימטיים במצב "נעול", בהתאמה להתנהגותה החזקה כמעכב אנזים. ניתוחים נוספים של ספיגה ומטבוליזם הצביעו על איזון בין שומניות למים מקובל והתערבות מוגבלת באנזימי כבד, אך גם רמזו שהתרכובת עשויה שלא להתאים לנטילה אורלית פשוטה ללא אופטימיזציה נוספת.
מה זה יכול להצביע לו לגבי אנטיביוטיקות עתידיות
לסיכום, הממצאים מצביעים על תרכובת 6g כנקודת התחלה מבטיחה לדור הבא של אנטיביוטיקות. היא מתוכננת להשבית שתי אנזימים חיידקיים חיוניים בו‑זמנית, מראה פעילות חזקה — במיוחד נגד מינים גרם‑שליליים עמידים — ומפרקת ביופילמים שמגינים על חיידקים, וכל זאת תוך היעדר רעילות מוקדמת בתא אנושי. יחד עם זאת, גודלה הגדול ותחזיות הספיגה הממוצעות מצביעים על כך ש‑6g ראויה להיחשב כשלד מוביל יותר מאשר כתרופה גמורה. עם כיוונון נוסף לשיפור החדירה לגוף ולחיידקים, הגישה הפעולה‑הכפולה הזאת עשויה לסייע להאריך את חיי התרופות בסגנון ציפרופלוקסצין ולהציע אפשרויות חדשות נגד זיהומים עמידים.
ציטוט: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
מילות מפתח: עמידות לאנטיביוטיקה, נגזרות ציפרופלוקסצין, מעכבי DNA גיראז, טופואיזומראז IV, חיידקים גרם-שליליים