Clear Sky Science · pt
Desenho, síntese e avaliação antibacteriana de uma nova série de compostos à base de ciprofloxacino como possíveis inibidores duplos da DNA girase/topoisomerase IV
Por que isso importa para infecções do dia a dia
A resistência a antibióticos está tornando infecções antes rotineiras mais difíceis e caras de tratar. A ciprofloxacino, um antibiótico amplamente utilizado para infecções urinárias, intestinais e pulmonares, está perdendo eficácia contra algumas bactérias. Este estudo explora uma forma engenhosa de aprimorar o desenho da ciprofloxacino para que ela ataque as bactérias com mais força em dois pontos vitais ao mesmo tempo, potencialmente desacelerando a marcha da resistência e melhorando o tratamento de infecções persistentes.
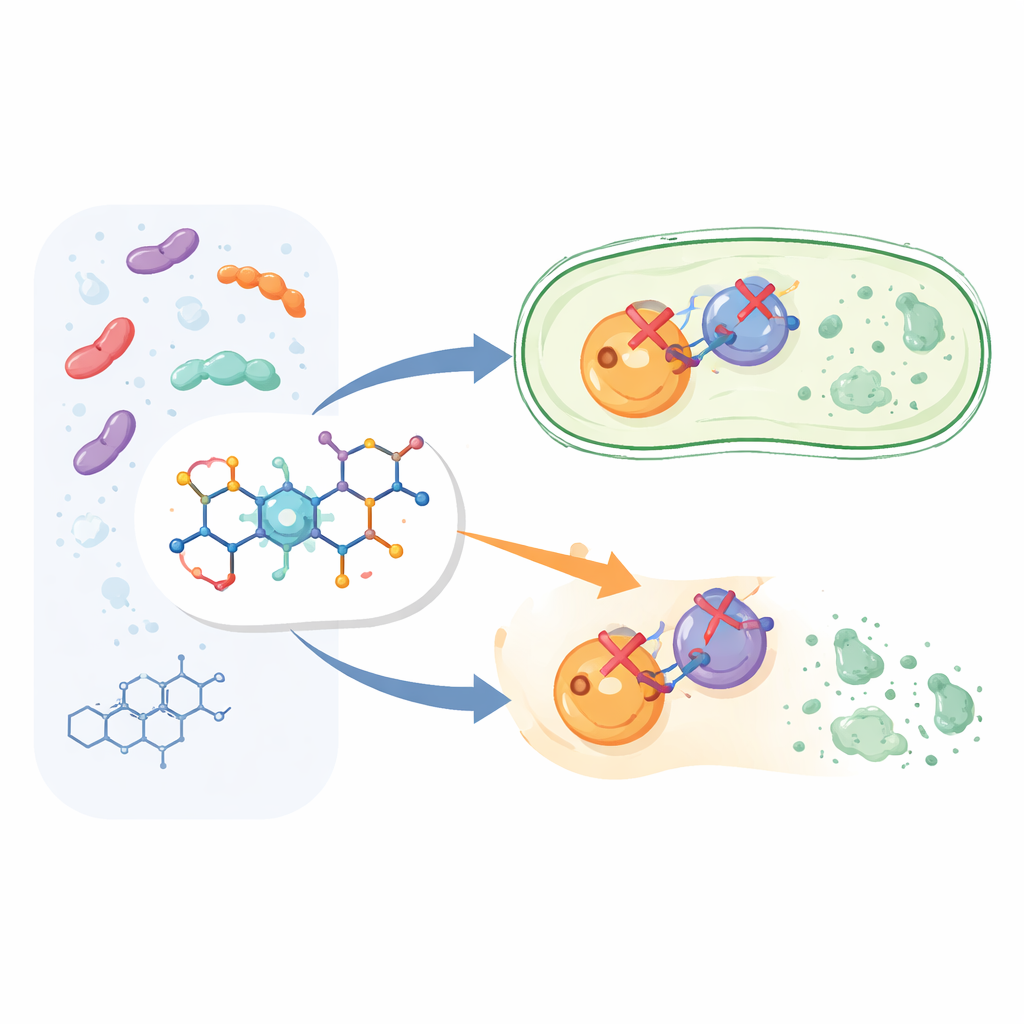
Construindo uma versão mais inteligente de um fármaco conhecido
Em vez de começar um medicamento totalmente novo do zero, os pesquisadores modificaram a estrutura da ciprofloxacino, membro da família amplamente usada das fluoroquinolonas. Mantiveram o núcleo da ciprofloxacino conhecido por matar bactérias e anexaram um fragmento químico adicional chamado aril-piridona em uma posição específica da molécula. Isso produziu doze novos compostos, rotulados de 6a a 6l. A ideia foi que essa “alça” extra ajudaria o fármaco a se prender aos alvos bacterianos com mais firmeza e de modo mais versátil do que a ciprofloxacino padrão.
Alvo duplo nas duas linhas vitais bacterianas
As bactérias dependem de duas enzimas intimamente relacionadas, a DNA girase e a topoisomerase IV, para gerenciar seu DNA durante o crescimento e a divisão. A ciprofloxacino já interfere nessas enzimas, mas não com a mesma eficiência em ambas. Os novos compostos foram projetados para bloquear fortemente os dois alvos ao mesmo tempo, o que deveria dificultar que as bactérias escapem por mutação de apenas uma enzima. Em testes enzimáticos com proteínas de Escherichia coli, a maioria das novas moléculas inibiu a DNA girase e a topoisomerase IV em níveis úteis. Um composto, chamado 6g, destacou-se: bloqueou a DNA girase ligeiramente melhor que a ciprofloxacino e inibiu a topoisomerase IV cerca de sete vezes mais fortemente, tornando-se a molécula “de ação dupla” mais potente do conjunto.
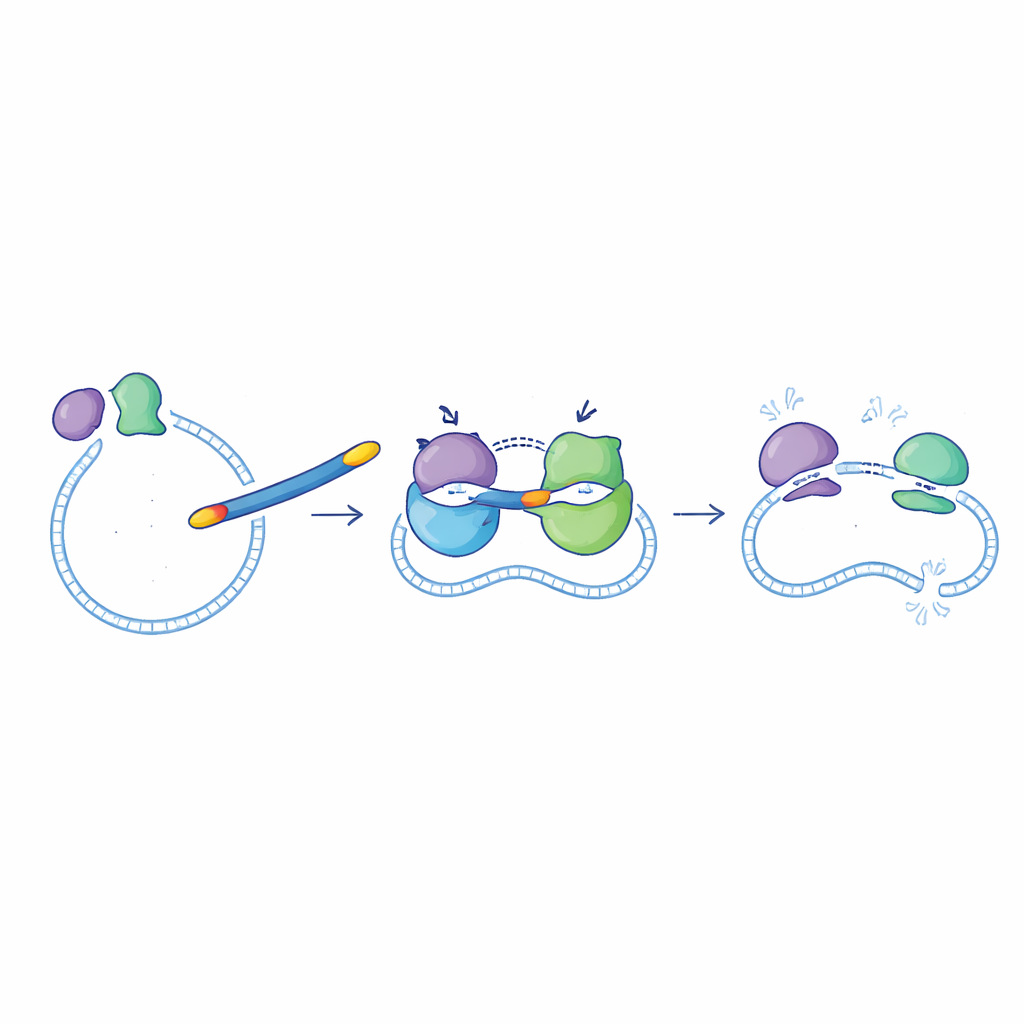
Testando as novas moléculas contra bactérias
A equipe então verificou se as melhorias observadas nas enzimas se traduziriam em melhor desempenho contra bactérias reais cultivadas em laboratório. Desempenhos selecionados, incluindo 6d, 6f, 6g, 6i e 6l, foram testados contra duas espécies Gram-negativas (E. coli e Pseudomonas aeruginosa) e duas Gram-positivas (Staphylococcus aureus e Bacillus subtilis). No geral, esses novos compostos funcionaram melhor contra bactérias Gram-negativas, onde a capacidade de atravessar a membrana externa é especialmente importante. O composto 6g novamente emergiu como o principal: suas doses eficazes mínimas contra E. coli e P. aeruginosa ficaram na mesma faixa que a ciprofloxacino, e ele manteve atividade razoável contra S. aureus, embora com menor potência ali do que o fármaco original.
Combate a comunidades bacterianas e avaliação preliminar de segurança
Além de células livres, as bactérias frequentemente se abrigam em comunidades viscosas chamadas biofilmes, que tornam as infecções mais persistentes e difíceis de erradicar. Os pesquisadores observaram que 6g suprimia fortemente biofilmes de E. coli, reduzindo-os em 96% na mesma concentração necessária para interromper o crescimento, e ainda apresentava atividade notável em doses mais baixas. Testes iniciais de segurança em uma linhagem normal de células mamárias humanas indicaram que 6g não é tóxico em níveis muito superiores aos necessários para afetar as bactérias, um sinal encorajador para desenvolvimento futuro, embora esteja longe de constituir uma avaliação de segurança completa.
Olhando para o aperto molecular
Para entender por que 6g performa tão bem, a equipe usou modelagem computacional para examinar como a molécula se encaixa nos bolsões da DNA girase e da topoisomerase IV. As simulações mostraram que 6g forma uma rede densa de interações — ligações de hidrogênio, contato com aminoácidos carregados e empacotamento ajustado contra a superfície da proteína — que são mais fortes e mais persistentes do que as da ciprofloxacino. Cálculos adicionais de como os complexos proteína–droga se movem ao longo do tempo sugeriram que 6g ajuda a manter as estruturas enzimáticas em um estado estável e travado, consistente com seu potente comportamento de bloqueio enzimático. Outras análises de absorção e metabolismo apontaram para um equilíbrio aceitável entre lipofilicidade e hidrossolubilidade e interferência limitada com enzimas hepáticas, mas também indicaram que o composto pode não ser ideal para administração oral simples sem otimizações adicionais.
O que isso pode significar para antibióticos futuros
Em conjunto, os resultados destacam o composto 6g como um ponto de partida promissor para antibióticos de próxima geração. Ele foi projetado para desativar duas enzimas bacterianas essenciais ao mesmo tempo, mostra forte atividade — especialmente contra espécies Gram-negativas difíceis — e perturba biofilmes protetores, tudo enquanto parece não ser tóxico em um teste inicial com células humanas. Ao mesmo tempo, seu grande tamanho e absorção prevista modesta fazem de 6g mais um esboço líder do que um medicamento pronto. Com aperfeiçoamentos para melhorar sua entrada no organismo e nas bactérias, essa abordagem de ação dupla pode ajudar a estender a vida útil de fármacos do tipo ciprofloxacino e oferecer novas opções contra infecções resistentes.
Citação: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Palavras-chave: resistência a antibióticos, derivados da ciprofloxacino, inibidores da DNA girase, topoisomerase IV, bactérias Gram-negativas