Clear Sky Science · tr
Ciprofloxacin bazlı yeni bir dizi bileşiğin tasarımı, sentezi ve antibakteriyel değerlendirmesi: olası çift DNA giraz/topoizomeraz IV inhibitörleri
Günlük enfeksiyonlar için bunun önemi nedir
Antibiyotik direnci bir zamanlar rutin olan enfeksiyonların tedavisini daha zor ve daha maliyetli hale getiriyor. İdrar, bağırsak ve akciğer enfeksiyonlarında yaygın olarak kullanılan işçi atı bir antibiyotik olan siprofloxacin, bazı bakterilere karşı etkisini kaybediyor. Bu çalışma, siprofloxacinin tasarımını akıllıca yükseltmenin bir yolunu araştırıyor; böylece ilacın bakterilerin iki hayati zayıf noktasına aynı anda daha güçlü şekilde saldırması sağlanarak direncin ilerleyişi yavaşlatılabilir ve inatçı enfeksiyonların tedavisi iyileştirilebilir.
Tanıdık bir ilacın daha akıllı bir versiyonunu inşa etmek
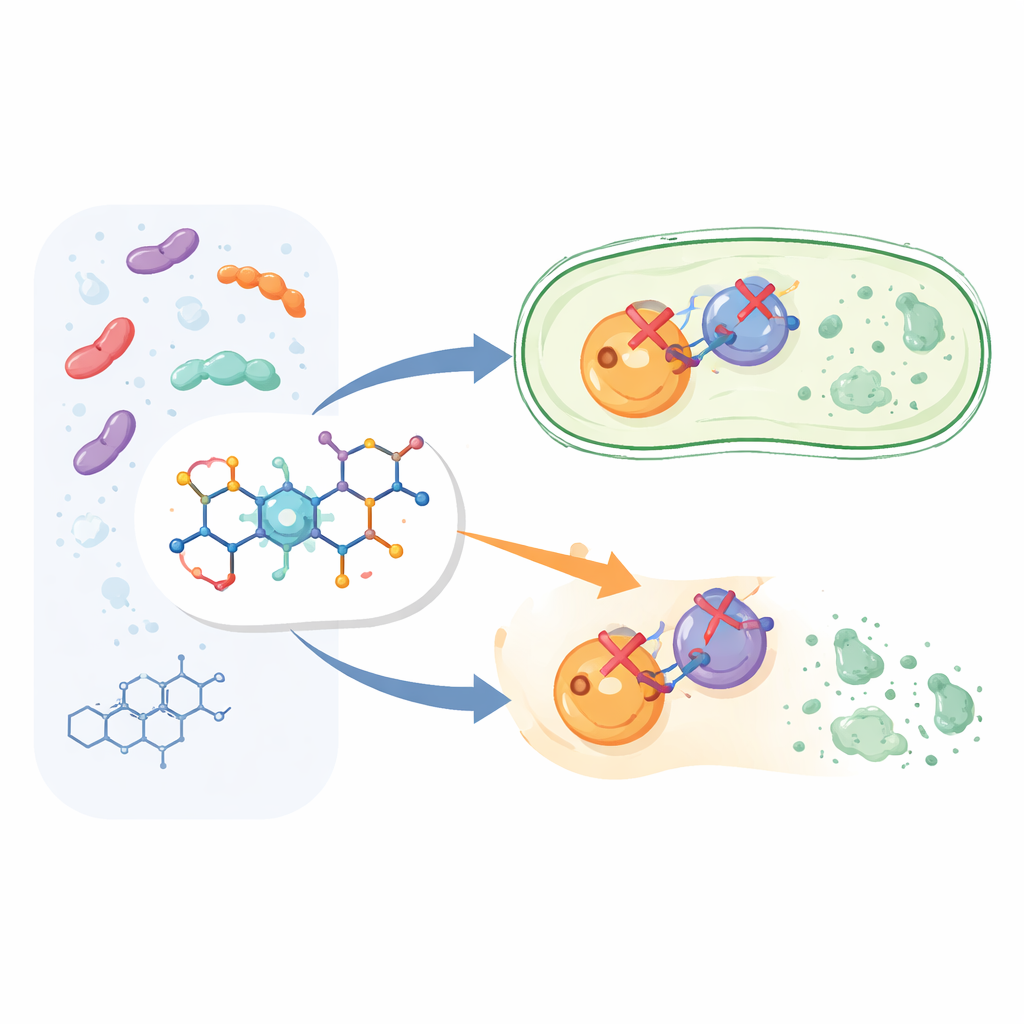
Tamamen yeni bir ilaçla başlamak yerine araştırmacılar, yaygın kullanılan florokinolon ailesinin bir üyesi olan siprofloxacinin yapısını değiştirdiler. Bakterileri öldürdüğü bilinen siprofloxacinin çekirdeğini korudular ve sonra molekülün belirli bir konumuna aril piridon adı verilen ek bir kimyasal parça eklediler. Bu, 6a ile 6l arasında etiketlenen on iki yeni bileşik üretti. Fikir, bu ekstra “tutamağın” ilacın bakteriyel hedeflerine standart siprofloxacin’den daha güçlü ve daha çok yönlü bir şekilde tutunmasına yardımcı olmasıydı.
Aynı anda iki bakteriyel yaşam hattını hedeflemek
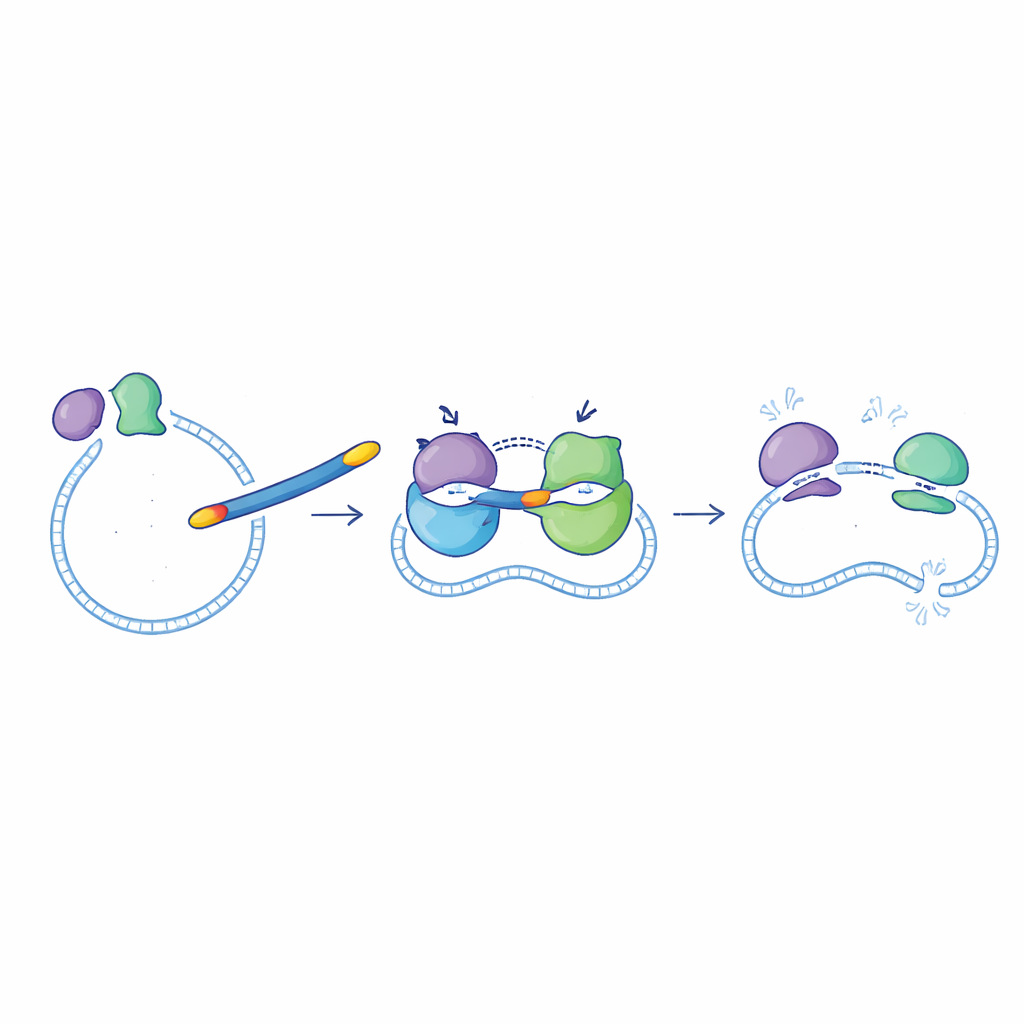
Bakteriler, büyüyüp bölünürken DNA’larını yönetmek için DNA giraz ve topoizomeraz IV adında iki yakından ilişkili enzime güvenirler. Siprofloxacin zaten bu enzimleri engelliyor, ancak her iki hedefi aynı derecede iyi etkilemiyor. Yeni bileşikler aynı anda her iki hedefin de güçlü bloklayıcıları olacak şekilde tasarlandı; bu, bakterilerin yalnızca bir enzimi mutasyona uğratarak kaçmasını zorlaştırmalıdır. Escherichia coli proteinleri kullanılarak yapılan enzim testlerinde, yeni moleküllerin çoğu DNA girazı ve topoizomeraz IV’ü faydalı düzeylerde inhibe etti. 6g adlı bir bileşik öne çıktı: DNA girazı siprofloxacine göre biraz daha iyi engelledi ve topoizomeraz IV’ü yaklaşık yedi kat daha güçlü biçimde inhibe ederek setteki en güçlü “çift etkili” molekül oldu.
Yeni molekülleri bakterilere karşı test etmek
Araştırma ekibi, enzim düzeyindeki iyileşmelerin laboratuvarda yetiştirilen gerçek bakterilere karşı daha iyi performansa dönüşüp dönüşmediğini kontrol etti. 6d, 6f, 6g, 6i ve 6l dahil olmak üzere seçilmiş üst performans gösterenler iki Gram-negatif tür (E. coli ve Pseudomonas aeruginosa) ve iki Gram-pozitif tür (Staphylococcus aureus ve Bacillus subtilis) karşı test edildi. Genel olarak bu yeni bileşikler özellikle dış zarın geçilmesinin önemli olduğu Gram-negatif bakterilere karşı en iyi etkiyi gösterdi. 6g yeniden öncü olarak öne çıktı: E. coli ve P. aeruginosa’ya karşı asgari etkili dozları siprofloxacinin aynı aralığındaydı ve S. aureus’a karşı makul etkinlik gösterse de orada orijinal ilaca göre daha az güçlüydü.
Bakteriyel topluluklarla mücadele ve güvenlik incelemeleri
Serbest yüzen hücrelerin ötesinde, bakteriler sık sık biyofilm adı verilen sümüksü topluluklarda saklanır; bu da enfeksiyonları daha inatçı ve yok etmeyi zorlaştırır. Araştırmacılar 6g’nin E. coli biyofilmlerini güçlü şekilde baskıladığını, büyümeyi durdurmak için gereken aynı konsantrasyonda biyofilmleri %96 oranında azalttığını ve daha düşük dozlarda da dikkat çekici aktivite gösterdiğini buldular. Normal bir insan meme hücresi hattında yapılan erken güvenlik kontrolleri, 6g’nin bakterileri etkilemek için gereken düzeylerden çok daha yüksek konsantrasyonlarda toksik olmadığını gösterdi; bu, gelecekteki geliştirmeler için cesaret verici bir işaret olsa da kapsamlı bir güvenlik değerlendirmesinden çok uzaktır.
Moleküler el sıkışmasını incelemek
6g’nin neden bu kadar iyi performans gösterdiğini anlamak için ekip, molekülün DNA giraz ve topoizomeraz IV ceplerine nasıl sığdığını incelemek üzere bilgisayar modellemesi kullandı. Simülasyonlar 6g’nin hidrojen bağları, yüklü aminoasitlerle temas ve protein yüzeyine sıkı paketlenme gibi yoğun bir etkileşim ağı oluşturduğunu gösterdi; bu etkileşimler siprofloxacininkinden daha güçlü ve daha kalıcıydı. Protein–ilaç komplekslerinin zaman içinde nasıl hareket ettiğine dair ek hesaplamalar, 6g’nin enzim yapılarını kararlı, kilitlenmiş bir durumda tutmaya yardımcı olduğunu öne sürdü; bu da onun güçlü enzim engelleyici davranışıyla tutarlı. Emilim ve metabolizma üzerine yapılan diğer analizler makul yağ–su dengesi ve karaciğer enzimleriyle sınırlı etkileşim gösterse de, bileşiğin ek optimizasyon olmadan basit ağız yoluyla kullanım için ideal olmayabileceğine dair ipuçları verdi.
Gelecek antibiyotikler için bunun anlamı
Bir arada değerlendirildiğinde sonuçlar 6g’yi gelecek nesil antibiyotikler için umut verici bir başlangıç noktası olarak öne çıkarıyor. Bu bileşik iki temel bakteriyel enzimi aynı anda kapatacak şekilde tasarlanmış, özellikle zorlu Gram-negatif türlere karşı güçlü aktivite gösteriyor ve koruyucu biyofilmleri bozuyor; aynı zamanda ilk insan hücresi testinde toksik görünmüyor. Öte yandan büyük boyutu ve tahmini emiliminin sınırlılığı 6g’yi tamamlanmış bir ilaçtan ziyade bir lider iskelet (lead scaffold) olarak görmeyi gerektiriyor. Vücuda ve bakterilere girişini iyileştirmek için daha fazla ince ayar yapıldığında, bu çift etkili yaklaşım siprofloxacin benzeri ilaçların kullanım ömrünü uzatmaya ve dirençli enfeksiyonlara karşı yeni seçenekler sunmaya yardımcı olabilir.
Atıf: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Anahtar kelimeler: antibiyotik direnci, siprofloxacin türevleri, DNA giraz inhibitörleri, topoizomeraz IV, Gram-negatif bakteriler