Clear Sky Science · sv
Design, syntes och antibakteriell bedömning av en ny serie ciprofloxacin-baserade föreningar som möjliga dubbla hämmare av DNA-gyras/topoisomeras IV
Varför detta spelar roll för vardagliga infektioner
Antibiotikaresistens gör tidigare rutinmässiga infektioner svårare och dyrare att behandla. Ciprofloxacin, ett arbetshästantibiotikum som används vid urinvägs-, tarm- och lunginfektioner, tappar effekt mot vissa bakterier. Denna studie undersöker ett smart sätt att uppgradera ciprofloxacins utformning så att det kan angripa bakterier hårdare på två viktiga svaga punkter samtidigt, vilket potentiellt kan bromsa resistensutvecklingen och förbättra behandlingen av svårbehandlade infektioner.
Att bygga en smartare version av ett välkänt läkemedel
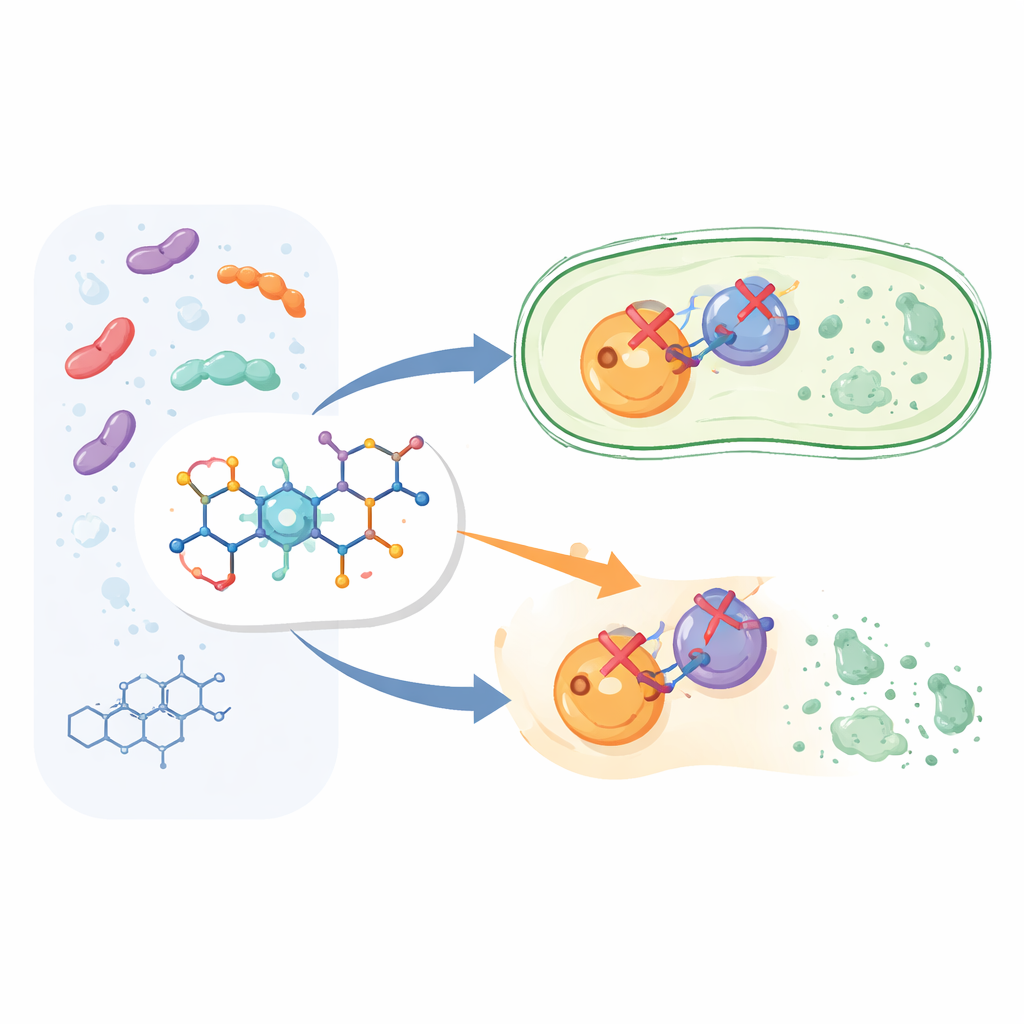
I stället för att börja från grunden med ett helt nytt läkemedel modifierade forskarna strukturen hos ciprofloxacin, en medlem av den mycket använda fluorkinolonfamiljen. De behöll kärnan i ciprofloxacin som är känd för att döda bakterier och fäste sedan en extra kemisk fragment som kallas arylpyridon på en specifik position i molekylen. Detta gav tolv nya föreningar, betecknade 6a till 6l. Idén var att detta extra "handtag" skulle hjälpa läkemedlet att greppa sina bakteriella mål starkare och på ett mer mångsidigt sätt än standardciprofloxacin.
Att rikta in sig på två bakterielivlinor samtidigt
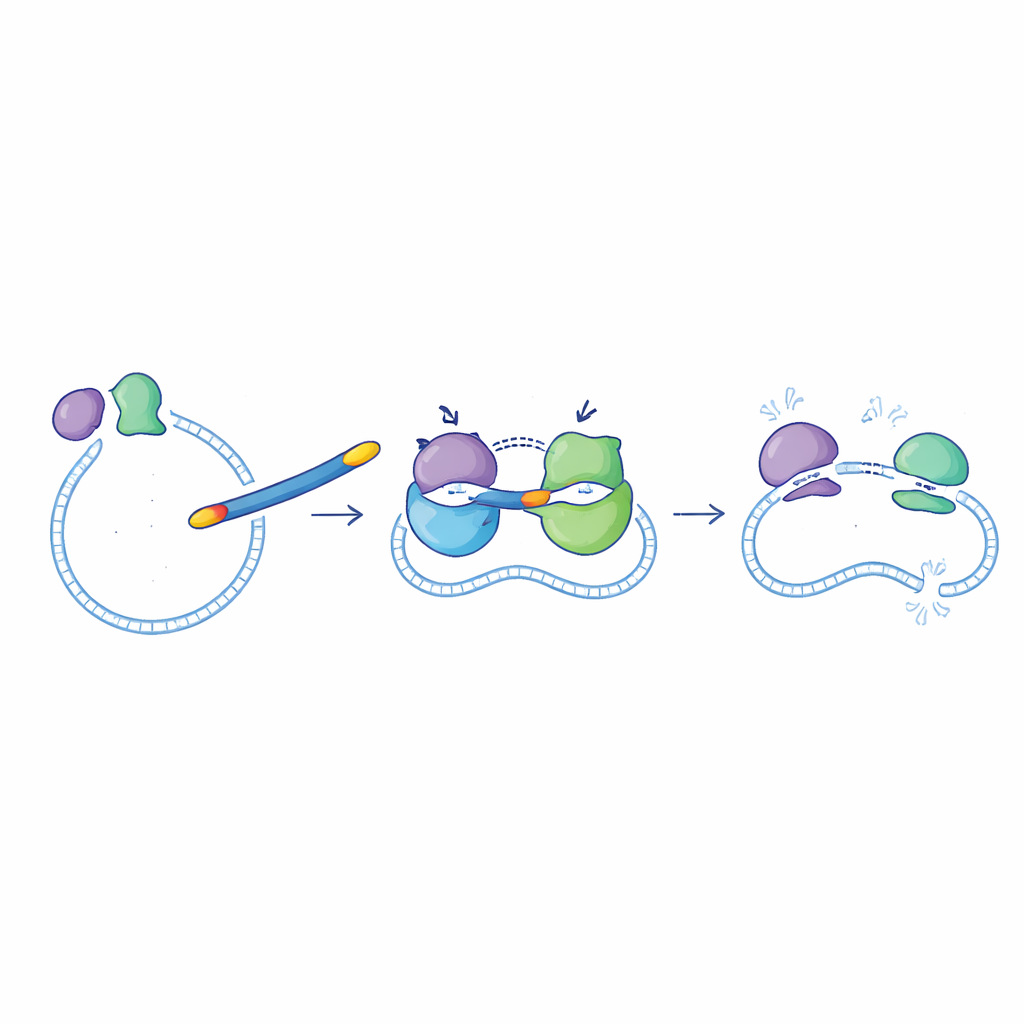
Bakterier förlitar sig på två närbesläktade enzymer, DNA-gyras och topoisomeras IV, för att hantera sitt DNA när de växer och delar sig. Ciprofloxacin stör redan dessa enzymer, men inte lika effektivt för båda. De nya föreningarna designades för att vara starka blockare av båda målen samtidigt, vilket borde göra det svårare för bakterier att undkomma genom att mutera bara ett enzym. I enzymtester med proteiner från Escherichia coli hämmade de flesta av de nya molekylerna DNA-gyras och topoisomeras IV på praktiskt användbara nivåer. En förening, kallad 6g, utmärkte sig: den hämmade DNA-gyras något bättre än ciprofloxacin och hämmande topoisomeras IV ungefär sju gånger starkare, vilket gjorde den till den mest potenta "dubbelverkande" molekylen i serien.
Att testa de nya molekylerna mot bakterier
Teamet kontrollerade sedan om enzymförbättringarna översattes till bättre verkan mot verkliga bakterier odlade i laboratoriet. Utvalda toppkandidater, inklusive 6d, 6f, 6g, 6i och 6l, testades mot två Gramnegativa arter (E. coli och Pseudomonas aeruginosa) och två Grampositiva arter (Staphylococcus aureus och Bacillus subtilis). Överlag fungerade dessa nya föreningar bäst mot Gramnegativa bakterier, där deras förmåga att korsar det yttre membranet är särskilt viktig. Förening 6g framstod återigen som ledande: dess minimala effektiva doser mot E. coli och P. aeruginosa låg i samma intervall som ciprofloxacin, och den var fortsatt rimligt aktiv mot S. aureus även om den var mindre potent där än originalläkemedlet.
Kampen mot bakteriesamhällen och säkerhetsundersökningar
Utöver fritt svävande celler gömmer sig bakterier ofta i slemlika samhällen kallade biofilmer, vilket gör infektioner mer långvariga och svårare att utrota. Forskarna fann att 6g kraftigt undertryckte E. coli-biofilmer och minskade dem med 96 procent vid samma koncentration som behövdes för att stoppa tillväxt, och visade fortfarande märkbar aktivitet vid lägre doser. Tidiga säkerhetskontroller i en normal mänsklig bröstcellinje antydde att 6g inte är toxisk vid nivåer betydligt högre än de som krävs för att påverka bakterier, ett uppmuntrande tecken för fortsatt utveckling, även om det är långt ifrån en fullständig säkerhetsbedömning.
En titt in i det molekylära handslaget
För att förstå varför 6g presterar så väl använde teamet datorbaserad modellering för att undersöka hur molekylen passar in i fickorna på DNA-gyras och topoisomeras IV. Simulationer visade att 6g bildar ett tätt nätverk av interaktioner—vätebindningar, kontakter med laddade aminosyror och tät packning mot proteinytan—som är starkare och mer bestående än ciprofloxacins. Ytterligare beräkningar av hur protein–läkemedelskomplexen rör sig över tid föreslog att 6g hjälper till att hålla enzymstrukturerna i ett stabilt, låst tillstånd, vilket stämmer överens med dess potenta enzymhämmande beteende. Andra analyser av absorption och metabolism pekade på acceptabel balans mellan fett och vatten och begränsad störning av leverenzym, men antydde även att föreningen kanske inte är idealisk för enkel oral dosering utan vidare optimering.
Vad detta kan innebära för framtida antibiotika
Sammantaget lyfter resultaten fram förening 6g som en lovande utgångspunkt för nästa generationens antibiotika. Den är konstruerad för att slå ut två viktiga bakteriella enzymer samtidigt, visar stark aktivitet—särskilt mot svåra Gramnegativa arter—och stör skyddande biofilmer, samtidigt som den verkar icke-toxisk i ett initialt mänskligt celltest. Samtidigt innebär dess stora storlek och måttligt förväntade absorption att 6g bättre ses som ett ledande ramverk än som ett färdigt läkemedel. Med fortsatt finslipning för att förbättra hur den tas upp av kroppen och når bakterier kan denna dubbelverkande strategi bidra till att förlänga livslängden för ciprofloxacin-liknande läkemedel och erbjuda nya alternativ mot resistenta infektioner.
Citering: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Nyckelord: antibiotikaresistens, ciprofloxacin-derivat, DNA-gyrashämmare, topoisomeras IV, Gramnegativa bakterier