Clear Sky Science · fr
Conception, synthèse et évaluation antibactérienne d’une nouvelle série de composés dérivés de la ciprofloxacine comme inhibiteurs potentiels doubles de l’ADN gyrase/topoisomérase IV
Pourquoi cela compte pour les infections quotidiennes
La résistance aux antibiotiques rend des infections autrefois banales plus difficiles et coûteuses à traiter. La ciprofloxacine, un antibiotique de référence utilisé pour les infections urinaires, intestinales et pulmonaires, perd de son efficacité face à certaines bactéries. Cette étude explore une manière ingénieuse d’améliorer la conception de la ciprofloxacine afin qu’elle attaque plus vigoureusement deux points faibles essentiels des bactéries à la fois, ralentissant potentiellement l’apparition de résistances et améliorant le traitement des infections tenaces.
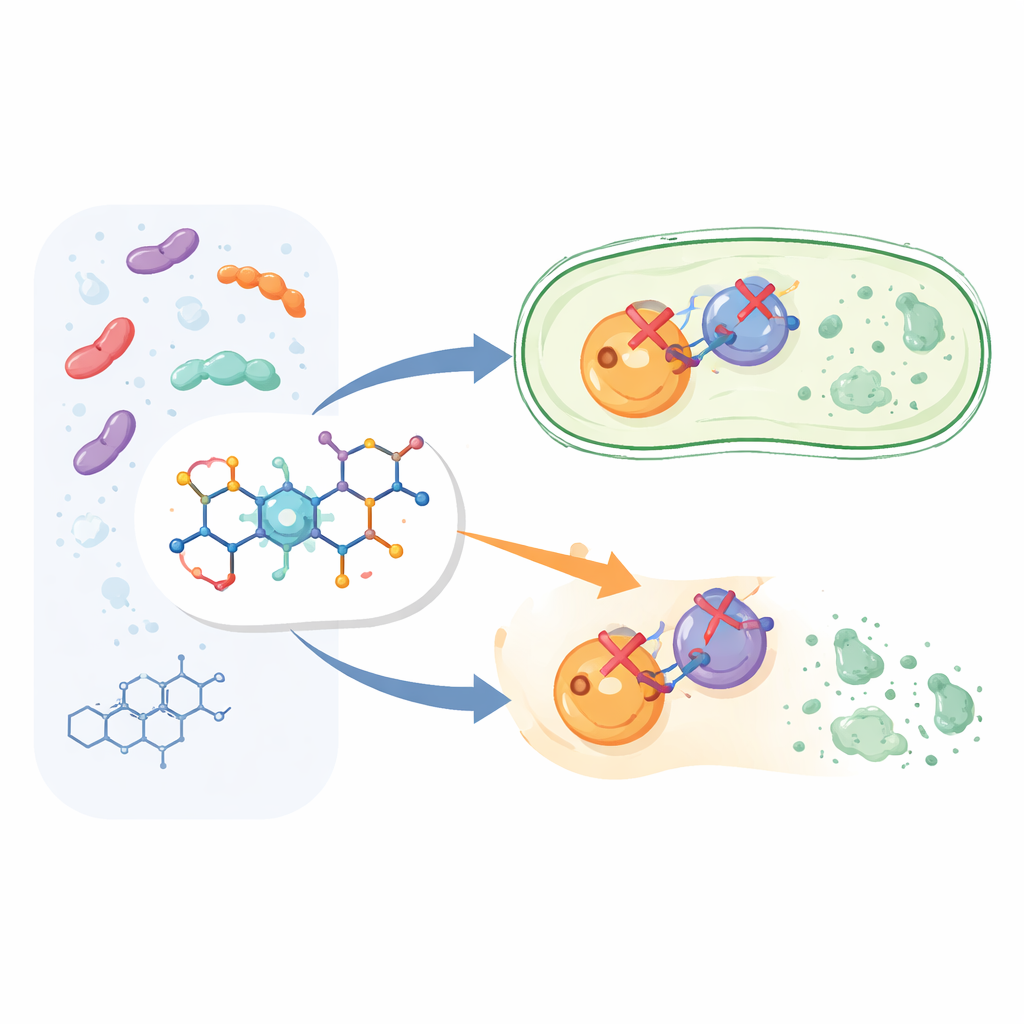
Construire une version plus intelligente d’un médicament familier
Plutôt que de partir d’un tout nouveau médicament, les chercheurs ont modifié la structure de la ciprofloxacine, membre de la famille largement utilisée des fluoroquinolones. Ils ont conservé le noyau de la ciprofloxacine connu pour son activité bactéricide, puis ont ajouté un fragment chimique supplémentaire appelé aryl pyridone à une position spécifique de la molécule. Cela a donné douze nouveaux composés, désignés 6a à 6l. L’idée était que cette « poignée » additionnelle aiderait le médicament à s’accrocher plus fortement et de façon plus polyvalente à ses cibles bactériennes que la ciprofloxacine standard.
Cibler deux lignes de vie bactériennes à la fois
Les bactéries dépendent de deux enzymes étroitement liées, l’ADN gyrase et la topoisomérase IV, pour gérer leur ADN lors de leur croissance et division. La ciprofloxacine interfère déjà avec ces enzymes, mais pas avec la même efficacité sur les deux. Les nouveaux composés ont été conçus pour bloquer fermement les deux cibles simultanément, ce qui devrait rendre plus difficile pour les bactéries d’échapper en mutant une seule enzyme. Dans des tests enzymatiques utilisant des protéines d’Escherichia coli, la plupart des nouvelles molécules ont inhibé l’ADN gyrase et la topoisomérase IV à des niveaux utiles. Un composé, nommé 6g, s’est distingué : il inhibait légèrement mieux l’ADN gyrase que la ciprofloxacine et inhibait la topoisomérase IV environ sept fois plus fortement, faisant de lui la molécule « double action » la plus puissante de la série.
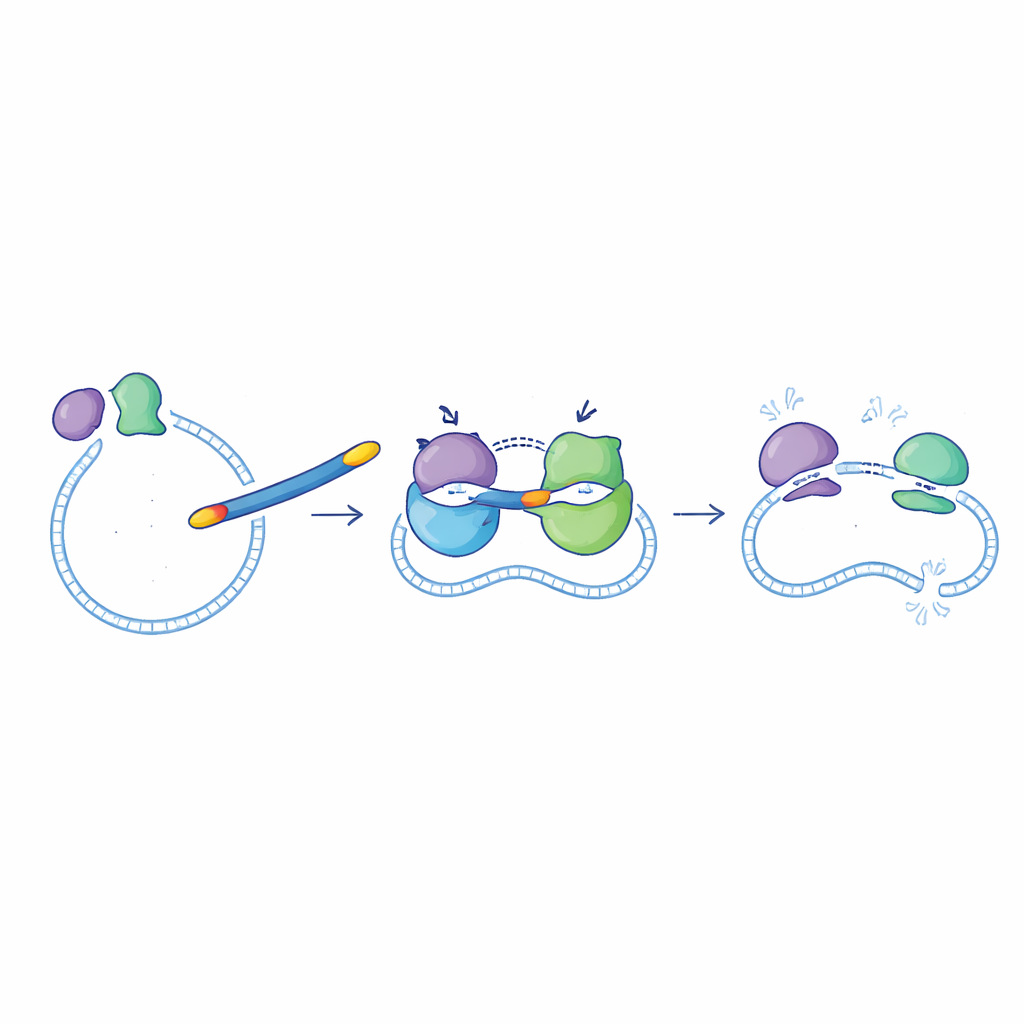
Mettre les nouvelles molécules à l’épreuve contre des bactéries
L’équipe a ensuite vérifié si les améliorations observées in vitro sur les enzymes se traduisaient par de meilleures performances contre de vraies bactéries cultivées en laboratoire. Les meilleurs candidats sélectionnés, notamment 6d, 6f, 6g, 6i et 6l, ont été testés contre deux espèces Gram-négatives (E. coli et Pseudomonas aeruginosa) et deux espèces Gram-positives (Staphylococcus aureus et Bacillus subtilis). Globalement, ces nouveaux composés étaient plus efficaces contre les bactéries Gram-négatives, où leur capacité à traverser la membrane externe est particulièrement importante. Le composé 6g s’est encore imposé comme le leader : ses doses effectives minimales contre E. coli et P. aeruginosa étaient du même ordre de grandeur que celles de la ciprofloxacine, et il restait raisonnablement actif contre S. aureus, bien qu’il y soit moins puissant que le médicament d’origine.
Combattre les communautés bactériennes et évaluer la sécurité
Au-delà des cellules libres, les bactéries se cachent souvent dans des communautés visqueuses appelées biofilms, qui rendent les infections plus persistantes et plus difficiles à éradiquer. Les chercheurs ont trouvé que 6g supprimait fortement les biofilms d’E. coli, les réduisant de 96 % à la même concentration nécessaire pour arrêter la croissance, et montrait encore une activité notable à des doses plus faibles. Des contrôles préliminaires de sécurité dans une lignée cellulaire mammaire humaine normale ont suggéré que 6g n’est pas toxique à des niveaux bien supérieurs à ceux nécessaires pour affecter les bactéries, un signe encourageant pour le développement futur, bien que très loin d’une évaluation complète de la sécurité.
Regarder à l’intérieur de la poignée de main moléculaire
Pour comprendre pourquoi 6g est si performant, l’équipe a utilisé la modélisation informatique pour examiner comment la molécule s’insère dans les sites de l’ADN gyrase et de la topoisomérase IV. Les simulations ont montré que 6g forme un réseau dense d’interactions — liaisons hydrogène, contacts avec des acides aminés chargés et empaquetage serré contre la surface de la protéine — qui sont plus fortes et plus persistantes que celles de la ciprofloxacine. Des calculs supplémentaires sur la dynamique des complexes protéine–médicament ont suggéré que 6g aide à maintenir les structures enzymatiques dans un état stable et verrouillé, en accord avec son fort pouvoir inhibiteur enzymatique. D’autres analyses de l’absorption et du métabolisme ont indiqué un équilibre lipophile–hydrophile acceptable et une interférence limitée avec les enzymes hépatiques, mais ont aussi laissé entendre que le composé pourrait ne pas être idéal pour une administration orale simple sans optimisation supplémentaire.
Ce que cela pourrait signifier pour les antibiotiques futurs
Dans l’ensemble, les résultats mettent en évidence le composé 6g comme point de départ prometteur pour des antibiotiques de nouvelle génération. Il est conçu pour bloquer deux enzymes bactériennes essentielles à la fois, montre une forte activité — en particulier contre des espèces Gram-négatives difficiles — et perturbe les biofilms protecteurs, tout en apparaissant non toxique dans un premier test sur cellules humaines. Parallèlement, sa grande taille et son absorption prédite modeste font de 6g davantage un échafaudage (lead scaffold) qu’un médicament fini. Avec un affinage supplémentaire pour améliorer sa pénétration dans l’organisme et dans les bactéries, cette approche à double action pourrait aider à prolonger la durée d’utilité des médicaments du type ciprofloxacine et offrir de nouvelles options contre les infections résistantes.
Citation: Al-Wahaibi, L.H., Alzahrani, H.A., Bräse, S. et al. Design, synthesis, and antibacterial assessment of a new series of ciprofloxacin-based compounds as possible dual DNA gyrase/topoisomerase IV inhibitors. Sci Rep 16, 13911 (2026). https://doi.org/10.1038/s41598-026-50106-z
Mots-clés: résistance aux antibiotiques, dérivés de la ciprofloxacine, inhibiteurs de l’ADN gyrase, topoisomérase IV, bactéries Gram-négatives