Clear Sky Science · zh
多种细胞内基序的复杂相互作用决定了毒蕈碱受体的G蛋白结合与激活
微小的细胞开关为何对医学至关重要
我们的细胞每时每刻都依赖被称为受体的微小分子开关来感知激素、神经递质和药物。一大类这样的开关,称为G蛋白偶联受体(GPCR),镶嵌在细胞膜上,通过名为G蛋白的伙伴将外部信号传入细胞内部。有些受体仅与一种类型的G蛋白通讯,而另一些则向多种G蛋白广播,最终影响从心率到情绪的诸多生理过程。本研究提出了一个看似简单但对药物设计影响深远的问题:受体内部的哪些特征决定了它与哪些G蛋白对话——以及对话的强度如何?
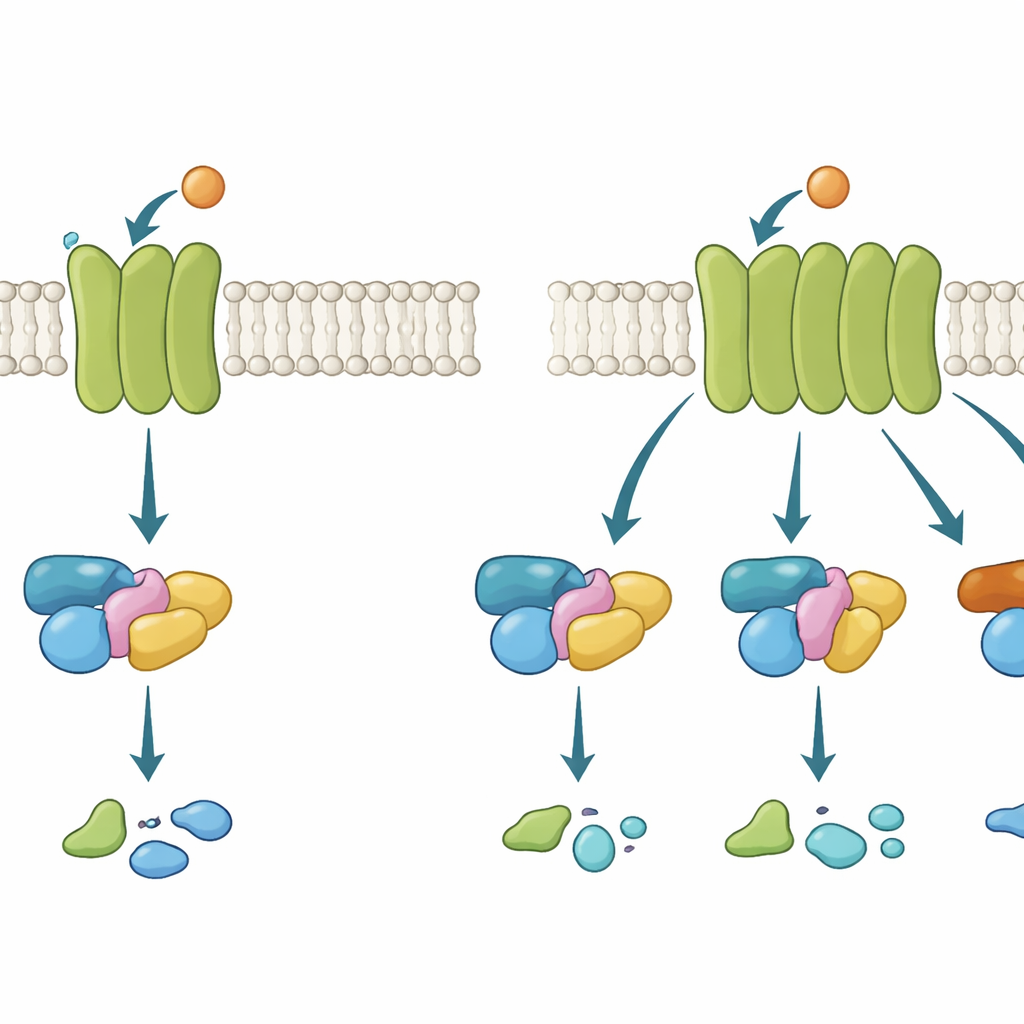
膜上的“手机信号塔”
G蛋白偶联受体有点像镶嵌在细胞外壳中的手机信号塔。当外部的信号分子(例如神经递质乙酰胆碱)结合到受体上时,受体会在内部发生构象变化并招募G蛋白。该G蛋白随后从非活性状态转换为活性状态并传递信息。G蛋白有多个家族,各自触发不同的细胞反应。有些GPCR高度挑剔,仅使用某一家族;另一些则更为多配,能同时招募多种家族。理解是什么使受体具有选择性或灵活性至关重要,因为许多重磅药物正是通过调节这些通路发挥作用。
交换部位以重写信号
研究人员聚焦于大脑与机体中两种密切相关的乙酰胆碱受体:M2受体,通常主要通过Gi/o型G蛋白传递信号;以及M3受体,偏好Gq型G蛋白但也能弱地招募Gi/o。与其寻找单个“万能”氨基酸,团队采取了模块化的方法。他们构建了嵌合受体——通过在M2与M3之间替换整个内部片段来形成杂交体,比如细胞内的短环、两根关键螺旋(称为5和6)的内端、一段短尾螺旋,以及富含正电荷残基的尾部片段。然后他们对每个嵌合体提出两个独立问题:它是否能与某种G蛋白结合?若能,是否能成功激活该G蛋白?
分别观察结合与激活
为追踪这些微观相互作用,团队在活细胞中使用了基于光学的方法。在第一组实验中,他们使用一种称为FRET的技术来检测在缺乏通常能量载体核苷酸GTP的受控条件下,受体与G蛋白结合的稳定性。这可以揭示受体—G蛋白对有多大的结合倾向以及结合持续的时间。在第二组实验中,他们用一种相关的方法BRET以及专门的传感器构建件来测量受体结合的G蛋白是否真正转变为活性状态。通过比较野生型与嵌合受体在两类G蛋白家族(Gi/o和Gq)上的表现,研究者能够区分出哪些结构片段在何种步骤上偏好哪类伙伴。
许多微小改变导致行为的大幅转变
结果表明,没有单一的内部特征可作为G蛋白选择的开/关开关。相反,是多个基序的组合协同起作用,而且这些效应依赖于受体的背景。例如,将更具有灵活性的M3受体的螺旋5和6的内端移植到选择性更强的M2受体中,会将其信号偏向Gq而非Gi/o,在某些情况下将M2转变为主要与Gq偶联的受体。再加入其他环段可以恢复结合并激活两类G蛋白的能力。相反,将M2样的片段插入M3可以使其更偏向Gi/o,或通过尾部的变化把信号几乎完全推向Gq。值得注意的是,某些嵌合体可以结合G蛋白但不激活它,而另一些即便结合过于短暂以致在结合测定中难以检测,仍能触发激活。
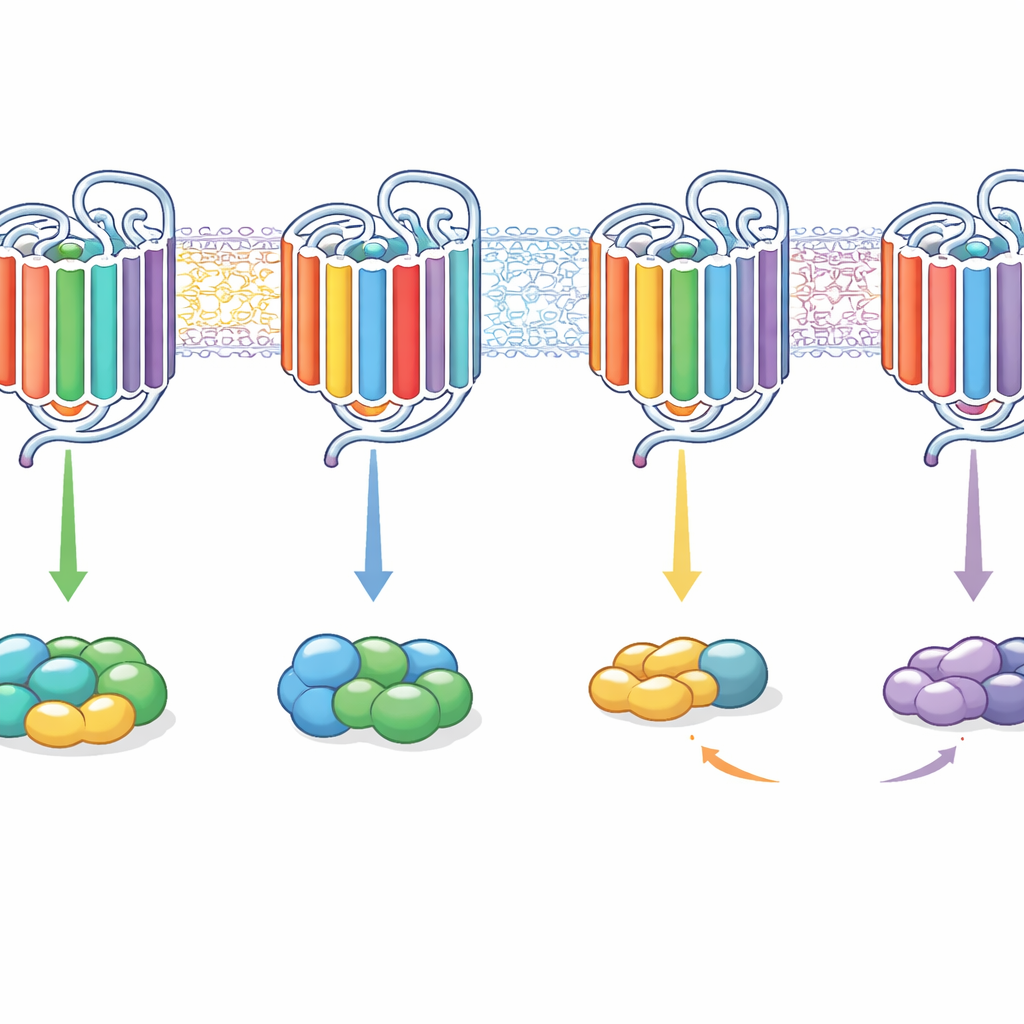
这对未来药物意味着什么
通俗地说,这项工作表明GPCR选择其信号伙伴并非通过单一钥匙孔,而是通过一整套内部部件的“组合锁”。内环、某些螺旋的内端和尾部在受体偏好某一G蛋白家族、偏好多家族或能结合却不真正激活这些G蛋白方面,都是协同起作用的。通过巧妙地重新组合这些片段,作者可以将受体从选择性导向广泛信号传递,亦或逆向操作。对药物发现而言,这表明调节受体使用其各种内部“拨盘”的方式,或可让未来药物将信号引导到有益通路并避开副作用,而无需彻底重新设计受体本身。
引用: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
关键词: G 蛋白偶联受体, 毒蕈碱受体, 信号转导, 受体选择性, 药物靶向