Clear Sky Science · pl
Złożona interakcja różnych wewnątrzkomórkowych motywów determinuje wiązanie białka G i aktywację receptorów muskarynowych
Dlaczego małe przełączniki komórkowe mają znaczenie dla medycyny
Co sekundę nasze komórki polegają na drobnych molekularnych przełącznikach zwanych receptorami, które wyczuwają hormony, neuroprzekaźniki i leki. Główna klasa tych przełączników, znana jako receptory sprzężone z białkiem G, osadza się w błonie komórkowej i przekazuje sygnały do wnętrza za pośrednictwem partnerów zwanych białkami G. Niektóre receptory komunikują się tylko z jednym typem białka G, inne nadają do kilku, kształtując wszystko, od częstości pracy serca po nastrój. W tym badaniu zadano pozornie proste pytanie o dużych implikacjach dla projektowania leków: które cechy wewnątrz receptora decydują, z jakimi białkami G się kontaktuje — i jak silnie?
Maszty telefonii komórkowej na błonie
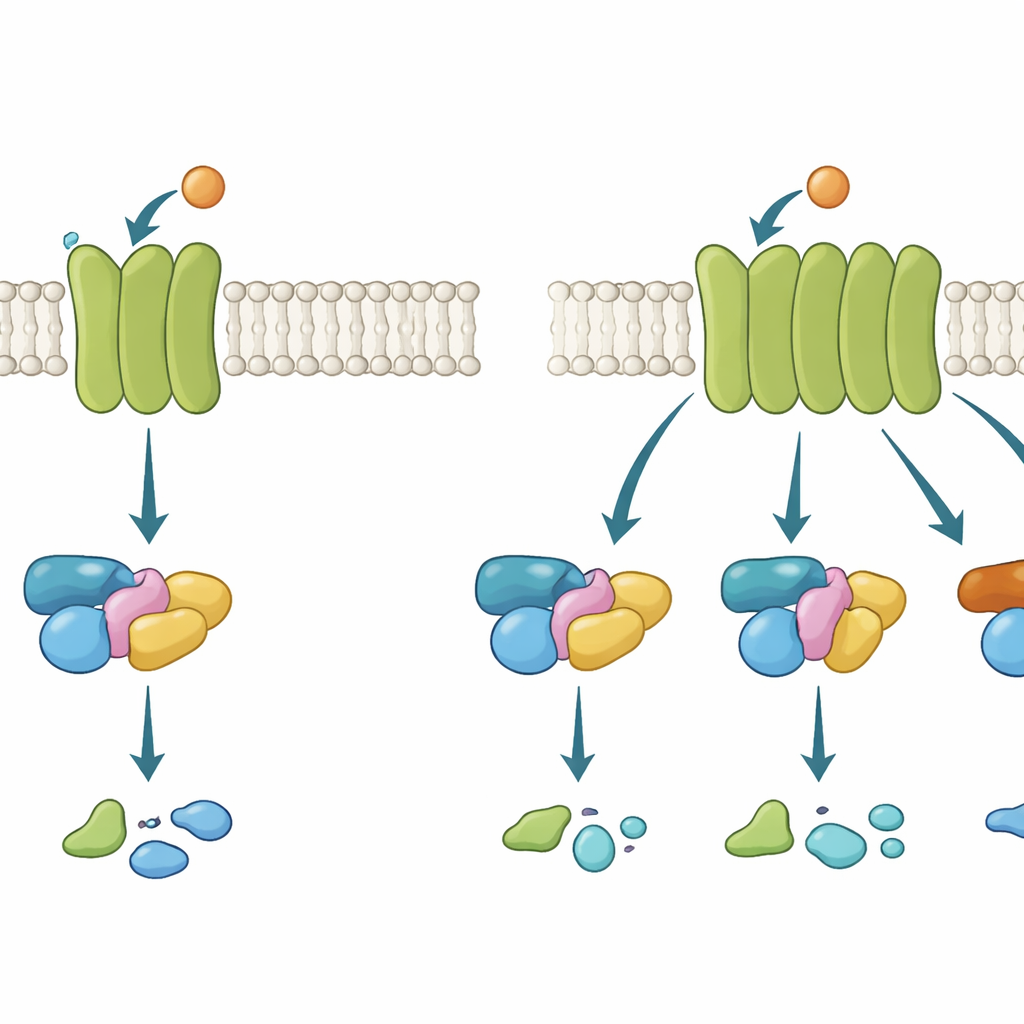
Receptory sprzężone z białkiem G (GPCR) działają trochę jak maszty telefonii komórkowej osadzone w zewnętrznej powłoce komórki. Kiedy cząsteczka sygnałowa, taka jak neuroprzekaźnik acetylocholina, przyłącza się z zewnątrz, receptor zmienia kształt od strony wewnętrznej i rekrutuje białko G. To białko wtedy przechodzi z formy nieaktywnej w aktywną i przekazuje sygnał dalej. Istnieje kilka rodzin białek G, z których każda wywołuje różne odpowiedzi komórkowe. Niektóre GPCR są bardzo wybiórcze i używają tylko jednej rodziny; inne są bardziej „promiskuitywne” i angażują kilka. Zrozumienie, co czyni receptor selektywnym lub elastycznym, ma kluczowe znaczenie, ponieważ wiele przełomowych leków działa przez modulowanie tych ścieżek.
Wymiana części, by przepisać sygnał
Naukowcy skupili się na dwóch blisko spokrewnionych receptorach acetylocholiny w mózgu i organizmie: receptorze M2, który zwykle sygnalizuje głównie przez białko G typu Gi/o, oraz receptorze M3, który preferuje białko G typu Gq, ale może słabiej również angażować Gi/o. Zamiast zakładać istnienie pojedynczych „magicznych” aminokwasów, zespół przyjął podejście modułowe. Zbudowali chimeryczne receptory — hybrydy, w których wymieniali całe wewnątrzkomórkowe segmenty między M2 i M3, takie jak krótkie pętle wewnątrzkomórkowe, wewnętrzne końce dwóch kluczowych helis (oznaczonych jako 5 i 6), krótka helisa ogonowa oraz fragmenty ogona bogate w dodatnio naładowane reszty. Następnie zadali dla każdej chimery dwa osobne pytania: czy wiąże dane białko G oraz, jeśli tak, czy potrafi je skutecznie aktywować?
Obserwowanie wiązania i aktywacji oddzielnie
Aby śledzić te mikroskopijne interakcje, zespół zastosował metody oparte na świetle w żywych komórkach. W pierwszym zestawie eksperymentów użyto techniki zwanej FRET, by wykryć, jak trwale receptor utrzymuje białko G w kontrolowanych warunkach, gdy brak jest zwykłego nukleotydu energetycznego GTP. To ujawnia, jak prawdopodobne i jak długie są kontakty pary receptor–białko G. W drugim zestawie użyto pokrewnej metody, BRET, z wyspecjalizowanymi czujnikami, aby zmierzyć, czy związane białka G rzeczywiście przechodzą w stan aktywny. Porównując, jak receptory typu dzikiego i chimery radziły sobie z dwiema rodzinami białek G — Gi/o i Gq — badacze mogli rozdzielić, które segmenty strukturalne faworyzują którego partnera i na którym etapie.
Wiele drobnych zmian, duże przesunięcia zachowania
Wyniki pokazały, że żaden pojedynczy wewnętrzny element nie działał jak włącznik wyboru białka G. Zamiast tego kombinacje motywów działały razem, a ich efekty zależały od kontekstu receptorowego. Na przykład przeszczepienie wewnętrznych końców helis 5 i 6 z bardziej elastycznego receptora M3 do wybiórczego M2 przesunęło jego sygnalizację głównie na Gq zamiast Gi/o, w niektórych przypadkach zamieniając M2 w receptor w przeważającej mierze sprzężony z Gq. Dodanie kolejnych fragmentów pętli mogło przywrócić zdolność wiązania i aktywacji obu rodzin białek G. Odwrotnie, wstawienie segmentów przypominających M2 do M3 mogło sprawić, że M3 silniej faworyzował Gi/o lub — przy zmianach w ogonie — skłaniał się niemal wyłącznie ku sygnalizacji przez Gq. Co warte podkreślenia, niektóre chimery potrafiły wiązać białko G bez jego aktywacji, podczas gdy inne nadal wywoływały aktywację nawet wtedy, gdy wiązanie było zbyt krótkotrwałe, by je wykryć w teście wiązania.
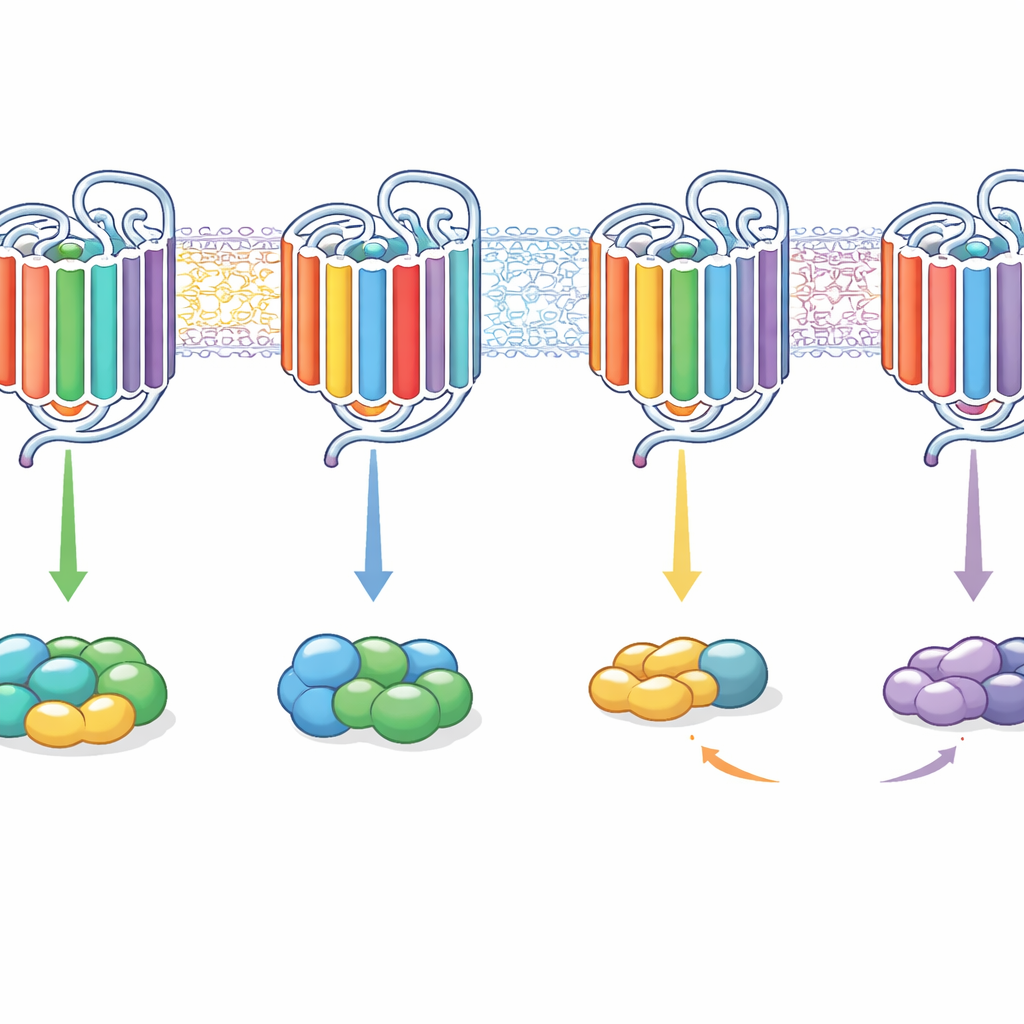
Co to oznacza dla przyszłych leków
Mówiąc potocznie, praca ta pokazuje, że GPCR wybierają swoich partnerów sygnalizacyjnych nie przez pojedynczy zamek, lecz przez cały szyfr złożony z wewnętrznych elementów. Wewnętrzne pętle, wewnętrzne końce niektórych helis i ogon współdziałają, decydując, czy receptor woli jedną rodzinę białek G, kilka z nich, czy może wiązać bez rzeczywistego ich włączania. Poprzez zręczne przestawianie tych segmentów autorzy mogli przeprogramować receptory od selektywnych do szeroko sygnalizujących i z powrotem. Dla odkrywania leków sugeruje to, że strojenie sposobu, w jaki receptor używa swoich wewnętrznych „pokręteł”, może pozwolić przyszłym lekom kierować sygnały ku korzystnym ścieżkom i z dala od skutków ubocznych, bez konieczności całkowitej przebudowy samego receptora.
Cytowanie: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Słowa kluczowe: receptory sprzężone z białkiem G, receptory muskarynowe, transdukcja sygnału, selektywność receptorów, celowanie leków