Clear Sky Science · nl
Een complex samenspel van verschillende intracellulaire motieven bepaalt G-eiwitbinding en activatie van muscarine receptoren
Waarom kleine schakelaars in cellen van belang zijn voor de geneeskunde
Elke seconde vertrouwen onze cellen op kleine moleculaire schakelaars, receptoren genoemd, om hormonen, neurotransmitters en medicijnen waar te nemen. Een belangrijke klasse van deze schakelaars, bekend als G-eiwit–gekoppelde receptoren (GPCR's), zit in het celmembraan en geeft berichten door naar binnen via partners die G-eiwitten heten. Sommige receptoren communiceren met slechts één type G-eiwit, terwijl andere met meerdere typen samenwerken, wat alles beïnvloedt van hartslag tot stemming. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties voor geneesmiddelontwerp: welke kenmerken binnen een receptor bepalen met welke G-eiwitten hij communiceert — en hoe sterk?
Mobiele telefoonmasten op het membraan
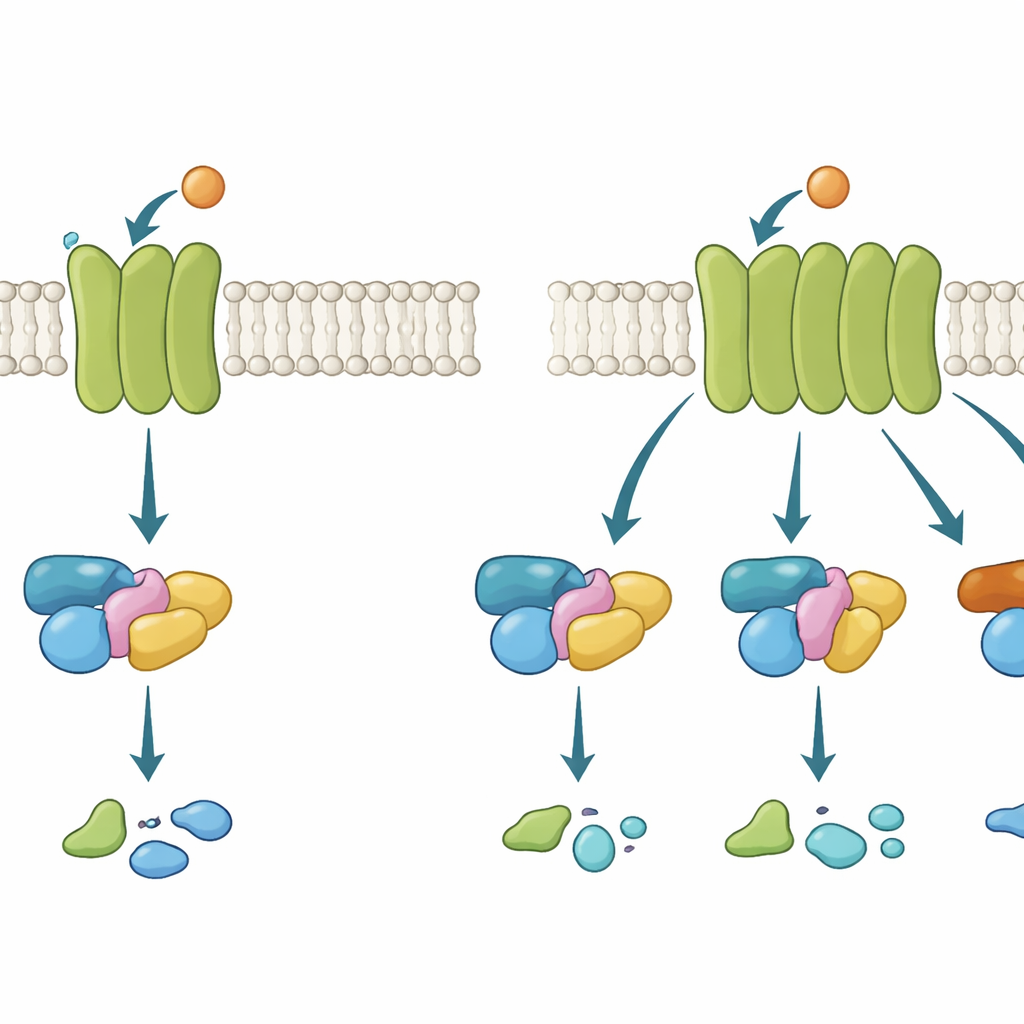
G-eiwit–gekoppelde receptoren (GPCR's) werken een beetje als zendmasten voor mobiele telefoons die in de buitenste laag van de cel zijn ingebed. Wanneer een signaalmolecuul, zoals de neurotransmitter acetylcholine, aan de buitenkant bindt, verandert de receptor van vorm aan de binnenkant en werft een G-eiwit. Dat G-eiwit schakelt dan van een inactieve naar een actieve staat en draagt het bericht verder. Er zijn verschillende families van G-eiwitten, die elk andere cellulaire reacties teweegbrengen. Sommige GPCR's zijn erg kieskeurig en gebruiken slechts één familie; andere zijn meer promiscuïteit en betrekken meerdere families. Begrijpen wat een receptor selectief of flexibel maakt is cruciaal, omdat veel succesvolle geneesmiddelen deze paden beïnvloeden.
Delen verwisselen om het signaal te herschrijven
De onderzoekers concentreerden zich op twee nauw verwante acetylcholinereceptoren in hersenen en lichaam: de M2-receptor, die normaal gesproken voornamelijk via een Gi/o-type G-eiwit signaleert, en de M3-receptor, die de voorkeur geeft aan een Gq-type G-eiwit maar ook zwak Gi/o kan betrekken. In plaats van te gokken naar enkele “magische” aminozuren volgde het team een modulaire aanpak. Ze bouwden chimere receptoren — hybriden waarbij ze gehele interne segmenten tussen M2 en M3 uitwisselden, zoals de korte lussen binnen de cel, de binnenuiteinden van twee belangrijke helices (genoemd 5 en 6), een korte staarthelix, en gedeelten van de staart rijk aan positief geladen residuen. Voor elk chimera stelden ze vervolgens twee afzonderlijke vragen: bindt het aan een gegeven G-eiwit, en zo ja, activeert het dat G-eiwit succesvol?
Binding en activatie afzonderlijk bekijken
Om deze microscopische interacties te volgen, gebruikte het team lichtgebaseerde methoden in levende cellen. In een eerste reeks experimenten gebruikten ze een techniek genaamd FRET om te detecteren hoe stabiel een receptor een G-eiwit vasthoudt in een gecontroleerde situatie waar het gebruikelijke energiedragende nucleotide GTP afwezig is. Dit laat zien hoe waarschijnlijk en hoe lang een receptor–G-eiwitpaar bij elkaar blijft. In een tweede reeks experimenten gebruikten ze een verwante methode, BRET, met gespecialiseerde sensorsconstructies om te meten of de gebonden G-eiwitten daadwerkelijk in hun actieve staat overgaan. Door te vergelijken hoe wildtype en chimere receptoren met twee G-eiwitfamilies — Gi/o en Gq — omgingen, konden de onderzoekers uitzoeken welke structurele segmenten welke partner bevoordeelden en in welke stap.
Veel kleine veranderingen, grote gedragsverschuivingen
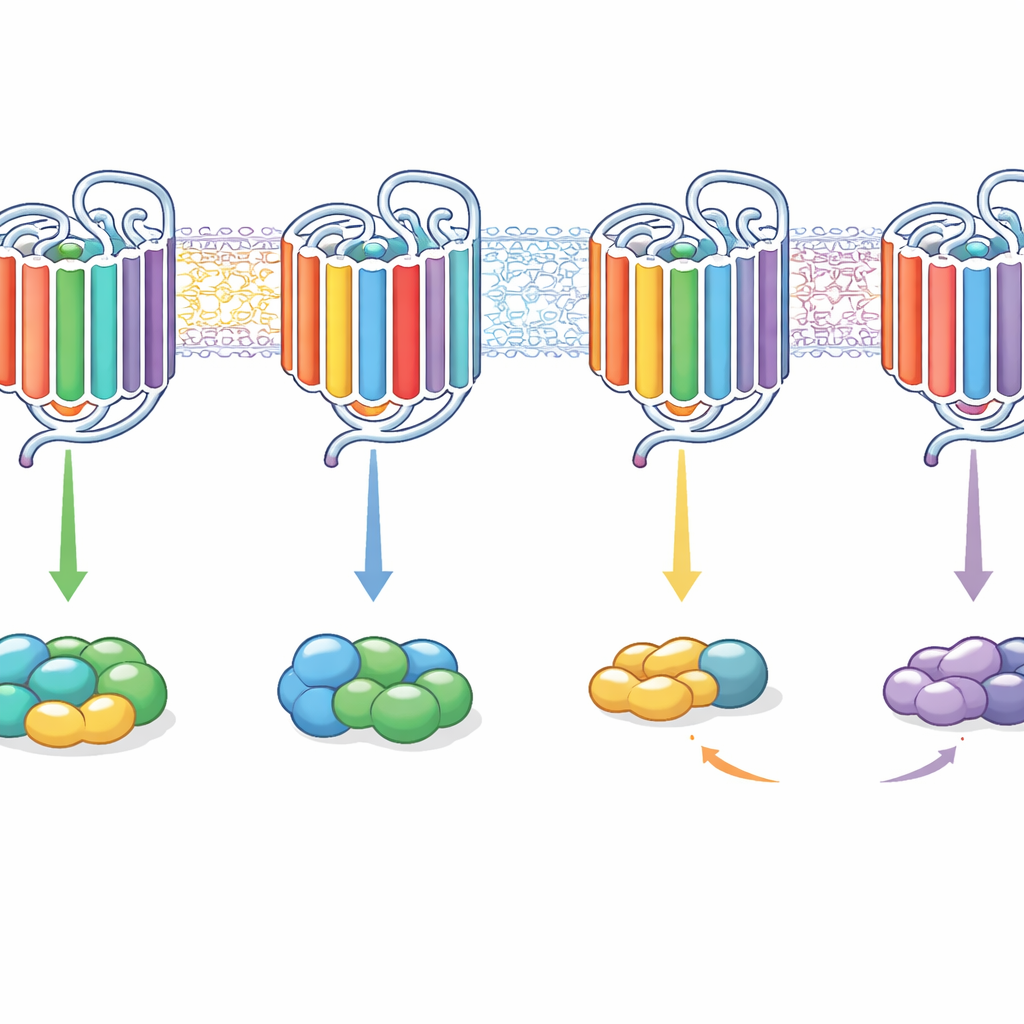
De resultaten toonden aan dat geen enkel intern kenmerk fungeerde als een aan/uit-schakelaar voor de keuze van G-eiwit. In plaats daarvan werkten combinaties van motieven samen, en hun effecten hingen af van de receptorachtergrond. Bijvoorbeeld, het transplanteren van de binnenuiteinden van helices 5 en 6 van de meer flexibele M3-receptor in de selectieve M2-receptor verschuift die om voornamelijk via Gq te signaleren in plaats van Gi/o, en veranderde M2 in sommige gevallen in een overwegend Gq-gekoppelde receptor. Het toevoegen van verdere lussegmenten kon het vermogen om beide G-eiwitfamilies te binden en te activeren herstellen. Omgekeerd kon het invoegen van M2-achtige segmenten in M3 ertoe leiden dat M3 Gi/o sterker verkoos of, met veranderingen in zijn staart, het naar bijna uitsluitend Gq-signaal duwen. Opmerkelijk was dat sommige chimera's een G-eiwit konden binden zonder het te activeren, terwijl andere nog steeds activatie konden uitlokken zelfs wanneer de binding te vluchtig was om met de bindingsassay te detecteren.
Wat dit betekent voor toekomstige geneesmiddelen
In gewone termen laat dit werk zien dat GPCR's hun signaalpartners niet kiezen via één sleutelgat, maar via een complete combinatieslot van interne onderdelen. De binnenlussen, de binnenuiteinden van bepaalde helices en de staart dragen allemaal gecoördineerd bij aan of een receptor de voorkeur geeft aan één G-eiwitfamilie, meerdere, of kan binden zonder ze echt aan te zetten. Door deze segmenten kunstig te herschikken konden de auteurs receptoren herprogrammeren van selectief naar breed signaalgevend en weer terug. Voor geneesmiddelontdekking suggereert dit dat het afstemmen van hoe een receptor zijn verschillende interne “knoppen” gebruikt toekomstige medicijnen in staat zou kunnen stellen signalen naar nuttige paden te leiden en bijwerkingen te vermijden, zonder de receptor volledig te hoeven herontwerpen.
Bronvermelding: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Trefwoorden: G-eiwit gekoppelde receptoren, muscarine receptoren, signaaltransductie, receptorselectiviteit, doelgerichte geneesmiddelen