Clear Sky Science · it
Un complesso intreccio di diversi motivi intracellulari determina il legame con le proteine G e l’attivazione dei recettori muscarinici
Perché i minuscoli interruttori cellulari sono importanti per la medicina
Ogni secondo, le nostre cellule si affidano a minuscoli interruttori molecolari chiamati recettori per percepire ormoni, neurotrasmettitori e farmaci. Una classe principale di questi interruttori, nota come recettori accoppiati a proteine G, è inserita nella membrana cellulare e trasmette messaggi all’interno tramite partner chiamati proteine G. Alcuni recettori comunicano con un solo tipo di proteina G, mentre altri trasmettono a più tipi, influenzando tutto, dalla frequenza cardiaca all’umore. Questo studio pone una domanda apparentemente semplice ma con grandi implicazioni per il design dei farmaci: quali caratteristiche all’interno di un recettore decidono con quali proteine G comunica — e con quale intensità?
Torri cellulari sulla membrana
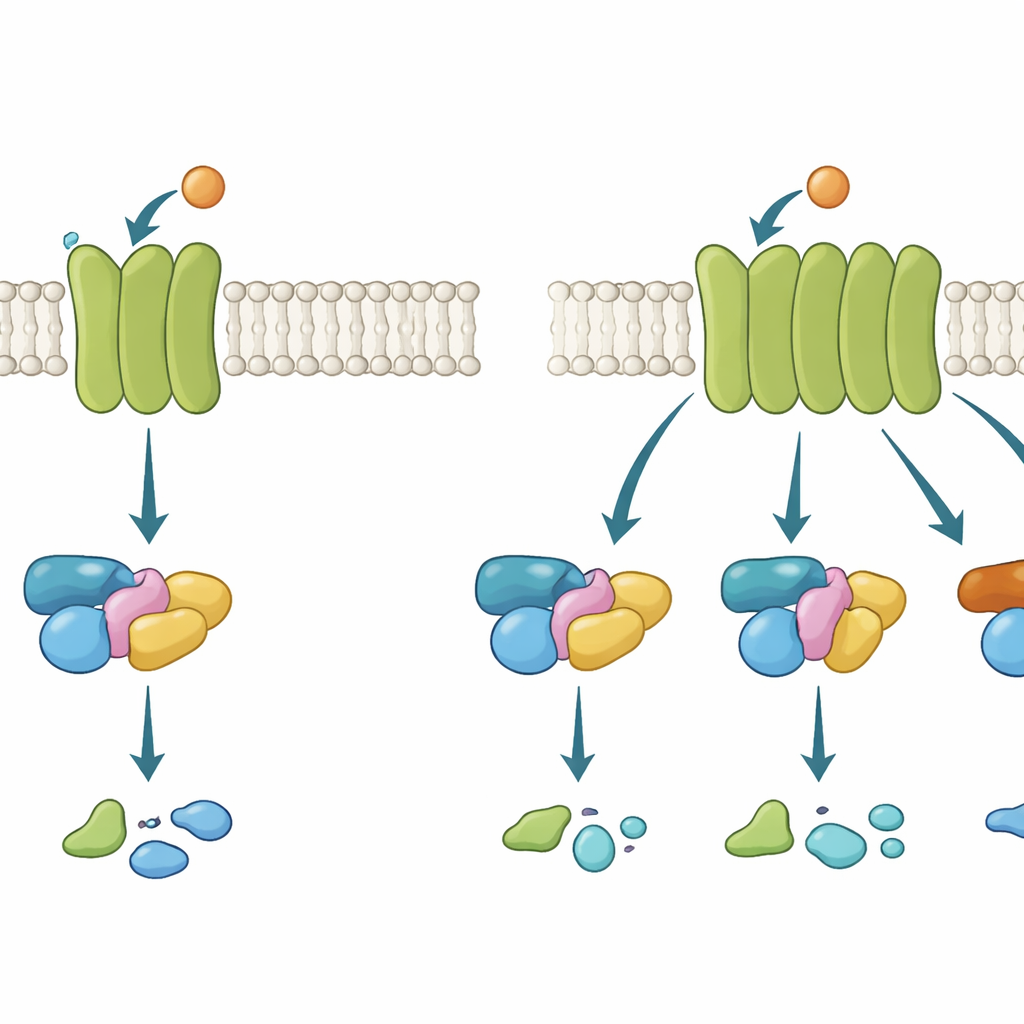
I recettori accoppiati a proteine G (GPCR) funzionano un po’ come torri di telefonia mobile incastonate nella parete esterna della cellula. Quando una molecola segnale, come il neurotrasmettitore acetilcolina, si lega all’esterno, il recettore cambia conformazione all’interno e recluta una proteina G. Quella proteina passa quindi da uno stato inattivo a uno attivo e continua il segnale. Esistono diverse famiglie di proteine G, ciascuna in grado di attivare risposte cellulari differenti. Alcuni GPCR sono molto selettivi, utilizzando una sola famiglia; altri sono più promiscui e ne coinvolgono diverse. Capire cosa rende un recettore selettivo o flessibile è cruciale, perché molti farmaci di grande successo agiscono modulando queste vie.
Sostituire parti per riscrivere il segnale
I ricercatori si sono concentrati su due recettori dell’acetilcolina strettamente imparentati nel cervello e nel corpo: il recettore M2, che normalmente segnala principalmente attraverso una proteina G di tipo Gi/o, e il recettore M3, che preferisce una proteina G di tipo Gq ma può anche coinvolgere debolmente Gi/o. Piuttosto che cercare singoli aminoacidi “magici”, il team ha adottato un approccio modulare. Hanno costruito recettori chimerici — ibridi in cui hanno scambiato interi segmenti interni tra M2 e M3, come le brevi spire all’interno della cellula, le estremità interne di due eliche chiave (dette 5 e 6), una breve elica della coda e tratti della coda ricchi di residui carichi positivamente. Poi hanno posto due domande separate per ciascun chimera: si lega a una data proteina G e, in tal caso, la attiva con successo?
Osservare legame e attivazione separatamente
Per tracciare queste interazioni microscopiche, il team ha usato metodi basati sulla luce in cellule vive. In un primo insieme di esperimenti hanno impiegato una tecnica chiamata FRET per rilevare quanto stabilmente un recettore trattiene una proteina G in un contesto controllato in cui manca il nucleotido energetico GTP. Questo rivela quanto è probabile e per quanto tempo una coppia recettore–proteina G resta insieme. In un secondo insieme di esperimenti hanno usato un metodo correlato, la BRET, con costrutti sensori specializzati per misurare se le proteine G legate effettivamente passano allo stato attivo. Confrontando come i recettori selvatici e quelli chimerici gestivano due famiglie di proteine G — Gi/o e Gq — i ricercatori hanno potuto separare quali segmenti strutturali favorivano quale partner e in quale fase.
Molte piccole modifiche, grandi cambiamenti di comportamento
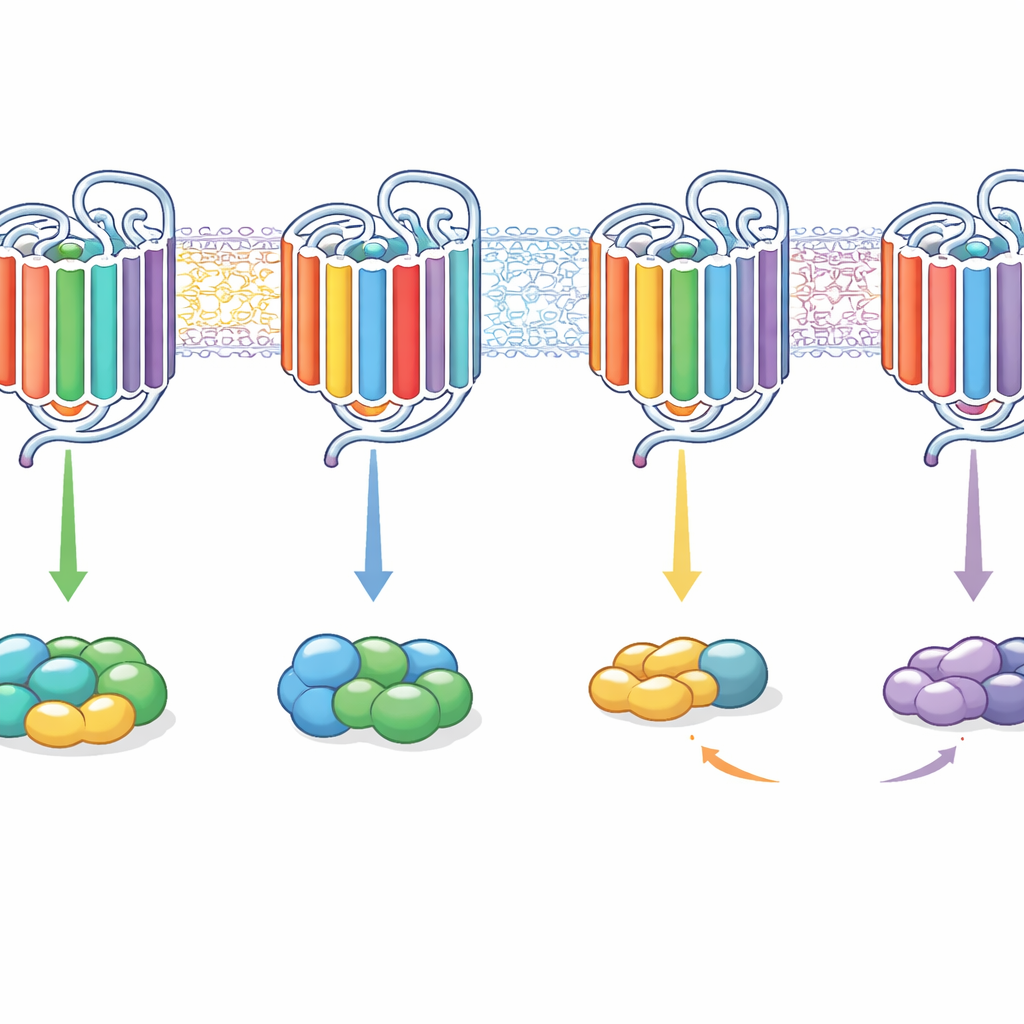
I risultati hanno mostrato che nessuna singola caratteristica interna agiva come un interruttore acceso/spento per la scelta della proteina G. Piuttosto, combinazioni di motivi agivano insieme e i loro effetti dipendevano dal contesto del recettore. Per esempio, trapiantare le estremità interne delle eliche 5 e 6 dal più flessibile recettore M3 nel recettore selettivo M2 lo spostava a segnalare principalmente tramite Gq invece che Gi/o, in alcuni casi trasformando M2 in un recettore prevalentemente accoppiato a Gq. L’aggiunta di ulteriori segmenti delle spire poteva ripristinare la capacità di legare e attivare entrambe le famiglie di proteine G. Viceversa, inserire segmenti simili a quelli di M2 in M3 poteva farla preferire maggiormente Gi/o o, con cambiamenti nella coda, spingerla a segnalare quasi esclusivamente tramite Gq. Notevolmente, alcuni chimeri potevano legare una proteina G senza attivarla, mentre altri potevano ancora innescare l’attivazione anche quando il legame era troppo fugace per essere rilevato con l’analisi di legame.
Cosa significa per i farmaci del futuro
In termini pratici, questo lavoro mostra che i GPCR scelgono i loro partner di segnalazione non attraverso una singola serratura ma tramite un vero e proprio combinatoreio di parti interne. Le spire interne, le estremità interne di certe eliche e la coda contribuiscono in modo coordinato a se un recettore preferisca una famiglia di proteine G, più famiglie o possa legare senza realmente attivarle. Rimescolando abilmente questi segmenti, gli autori sono riusciti a riprogrammare i recettori da selettivi a ampiamente segnalanti e viceversa. Per la scoperta di farmaci, questo suggerisce che modulare il modo in cui un recettore usa i suoi vari “manopole” interne potrebbe consentire ai futuri medicinali di indirizzare i segnali verso vie utili e lontano dagli effetti collaterali, senza dover riprogettare completamente il recettore stesso.
Citazione: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Parole chiave: Recettori accoppiati a proteine G, Recettori muscarinici, Trasduzione del segnale, Selettività del recettore, Targeting farmacologico