Clear Sky Science · ja
さまざまな細胞内モチーフの複雑な相互作用がムスカリン性受容体のGタンパク質結合と活性化を決定する
医療で重要ないちいちの細胞スイッチの意味
私たちの細胞は毎秒、受容体と呼ばれる小さな分子スイッチに頼ってホルモン、神経伝達物質、薬物を感知しています。これらのスイッチの主要なクラスであるGタンパク質共役受容体(GPCR)は細胞膜に埋まり、Gタンパク質と呼ばれるパートナーを介して内部に情報を伝えます。ある受容体は一種類のGタンパク質だけとやり取りし、別の受容体は複数の種類とやり取りして心拍や気分などを形作ります。本研究は、薬の設計に大きな示唆を与える一見単純な問いを投げかけます:受容体のどの内部要素がどのGタンパク質と(どれだけ強く)話すかを決めるのか?
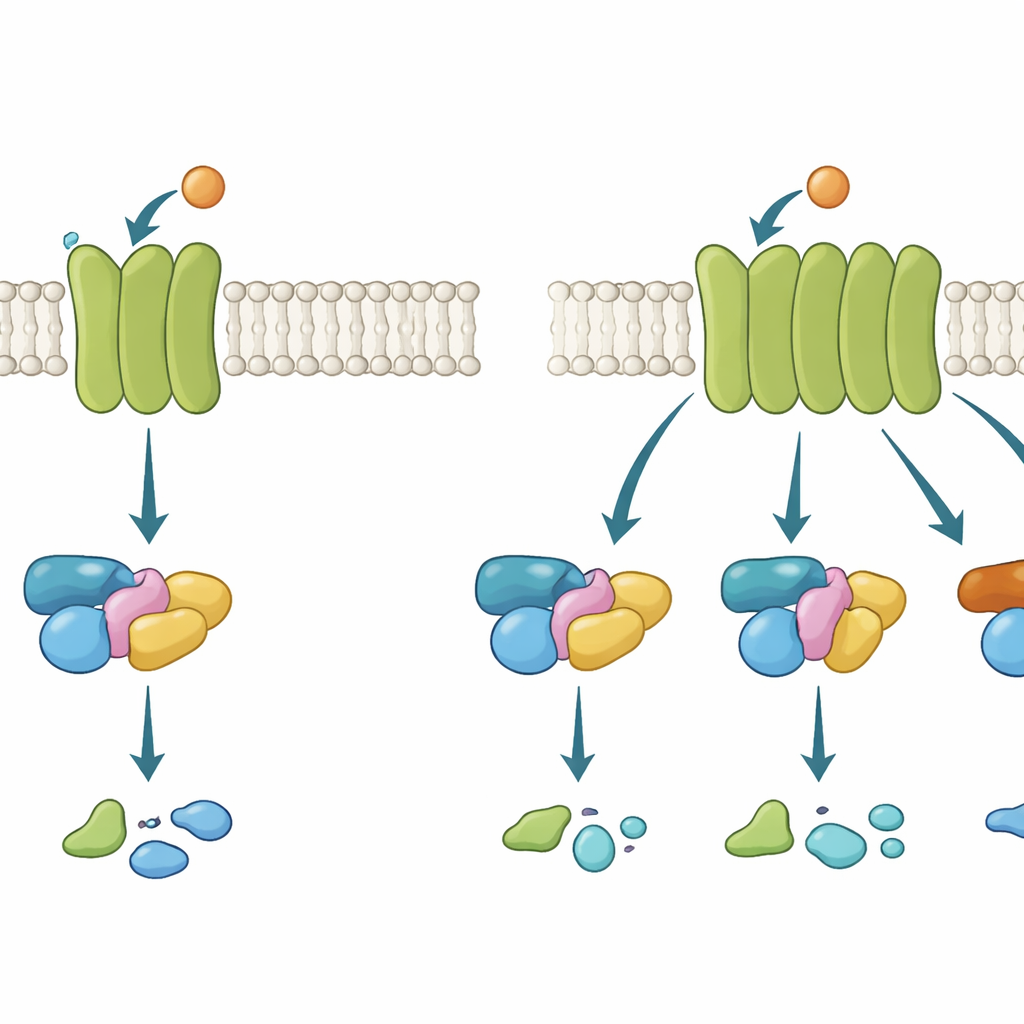
膜上の携帯電話の塔のような存在
Gタンパク質共役受容体(GPCR)は、細胞外側に信号分子(例えば神経伝達物質のアセチルコリン)が結合すると、内部で立体構造を変えGタンパク質を呼び寄せる携帯電話の塔のように働きます。結合したGタンパク質は不活性状態から活性状態へ切り替わり、信号を伝えます。Gタンパク質にはいくつかのファミリーがあり、それぞれ異なる細胞応答を引き起こします。あるGPCRは非常に選択的で一つのファミリーしか使わず、他は複数に対応します。受容体が選択的か柔軟かを理解することは重要で、多くの有力な薬はこれらの経路を調節することで効くからです。
部品を入れ替えて信号を書き換える
研究者たちは脳と体に存在する二つの近縁なアセチルコリン受容体、すなわち通常は主にGi/o型Gタンパク質を介してシグナルを伝えるM2受容体と、主にGq型を好むが弱くGi/oにも関与できるM3受容体に着目しました。単一の「魔法の」アミノ酸を当てるのではなく、彼らはモジュール式のアプローチを採りました。細胞内の短いループ、5番と6番の主要なヘリックスの内端、短い尾部ヘリックス、正に帯電した残基が多い尾部の区間など、M2とM3間で内部セグメント全体を入れ替えたキメラ受容体—ハイブリッド—を作製しました。各キメラについて二つの別々の問いを立てました:特定のGタンパク質に結合するか、そして結合した場合、それを実際に活性化できるか?
結合と活性化を分けて観察する
これらの微視的相互作用を追跡するために、チームは生細胞内で光を使った手法を用いました。最初の実験群では、通常のエネルギー担体ヌクレオチドGTPがない制御環境で、FRETと呼ばれる技術を使って受容体がGタンパク質をどれだけ安定して保持するかを検出しました。これにより受容体–Gタンパク質対がどれだけ生じやすく、どれだけ長く一緒にいられるかが明らかになります。第二の実験群では、関連法であるBRETを用い、専用のセンサー構成体を使って結合したGタンパク質が実際に活性状態に変換されるかを測定しました。野生型とキメラ受容体がGi/oおよびGqという二つのGタンパク質ファミリーをどのように扱うかを比較することで、どの構造セグメントがどの相手を、どの段階で好むかを解きほぐせます。
多くの小さな変化が行動に大きな変化をもたらす
結果は、単一の内部特徴がGタンパク質選択のオン・オフスイッチになるわけではないことを示しました。代わりに、複数のモチーフが組み合わさって作用し、その効果は受容体の背景(コンテクスト)に依存しました。例えば、より柔軟なM3受容体の5番と6番ヘリックスの内端を選択的なM2に移植すると、M2はGi/oよりも主にGqを介してシグナルを送るようにシフトし、場合によってはM2が主にGq結合の受容体に変わることがありました。さらにループ区間を追加すると、両方のGタンパク質ファミリーに結合し活性化する能力が回復することもありました。逆にM3にM2様の区間を挿入するとGi/oをより強く好むようになったり、尾部の変化でほぼ専らGqを介したシグナル伝達に傾くこともありました。注目すべきは、あるキメラはGタンパク質に結合するが活性化はしない一方で、他のキメラは結合が結合アッセイで検出できないほど短時間でも活性化を引き起こせる場合があったことです。
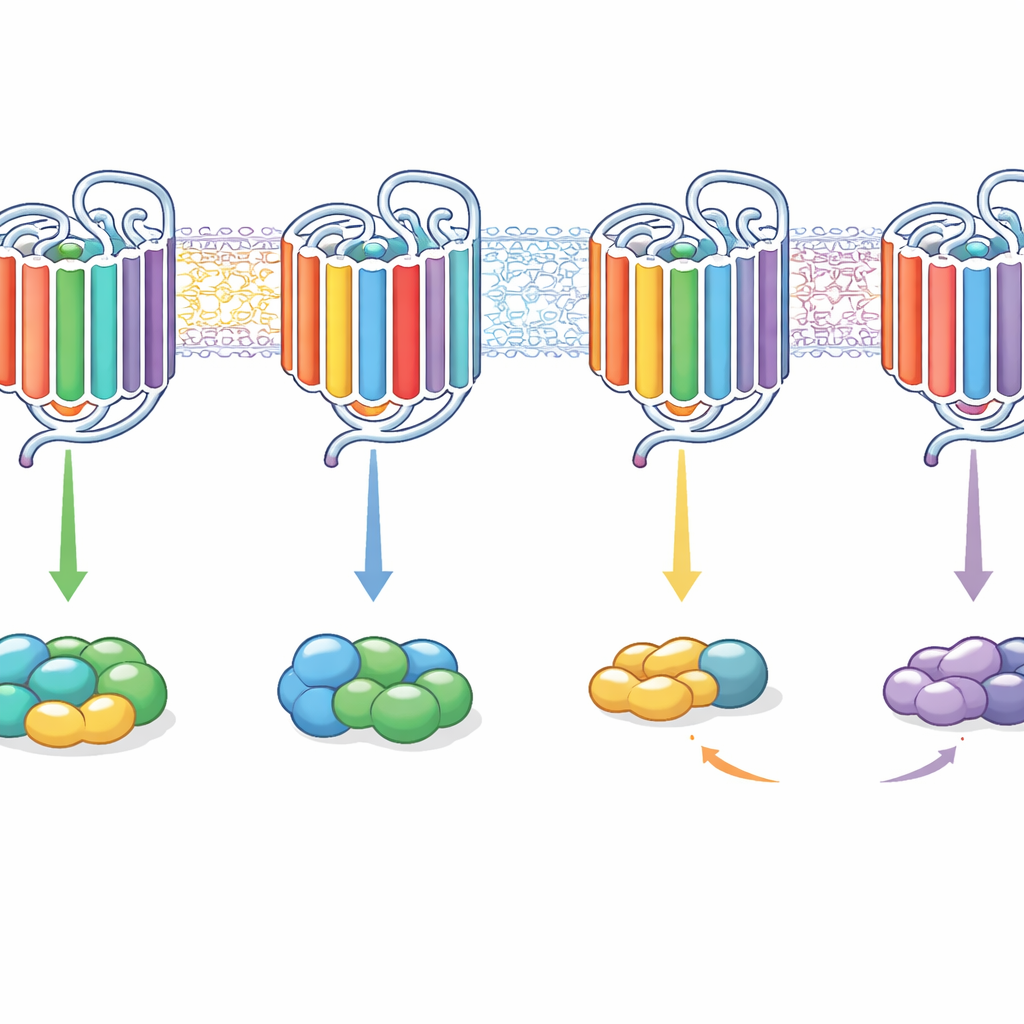
将来の薬にとっての意味
日常的な言い方をすれば、本研究はGPCRが単一の鍵穴を通じてシグナルパートナーを選ぶのではなく、内部の複数の部位で構成されるコンビネーションロックのように選ぶことを示しています。内側のループ、特定ヘリックスの内端、尾部が協調して、受容体が一つのGタンパク質ファミリーを好むのか、複数を扱えるのか、あるいは結合するが真に活性化しないのかを決めます。これらの区間を巧みに組み替えることで、著者らは受容体を選択的から広範囲に信号を出すものへ、そして再び選択的へと再プログラムできました。薬剤探索においては、受容体の内部にある様々な“ダイヤル”の使い方を微調整することで、受容体自体を完全に作り直すことなく、望ましい経路へ信号を誘導し副作用を避ける可能性が示唆されます。
引用: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
キーワード: Gタンパク質共役受容体, ムスカリン性受容体, シグナル伝達, 受容体選択性, 薬物標的化