Clear Sky Science · ru
Сложное взаимодействие различных внутриклеточных мотивов определяет связывание G‑белков и их активацию мускариновыми рецепторами
Почему крошечные клеточные переключатели важны для медицины
Каждую секунду наши клетки полагаются на крошечные молекулярные переключатели — рецепторы, которые улавливают гормоны, нейромедиаторы и препараты. Один из основных классов таких переключателей, известный как рецепторы, сопряжённые с G‑белками, встроен в мембрану клетки и передаёт сигналы внутрь через партнёров, называемых G‑белками. Некоторые рецепторы «разговаривают» только с одним типом G‑белка, тогда как другие передают сигналы нескольким типам, влияя на всё — от сердечного ритма до настроения. В этом исследовании поставлен на первый взгляд простой, но важный для разработки лекарств вопрос: какие внутриклеточные свойства рецептора определяют, с какими G‑белками он взаимодействует и с какой силой?
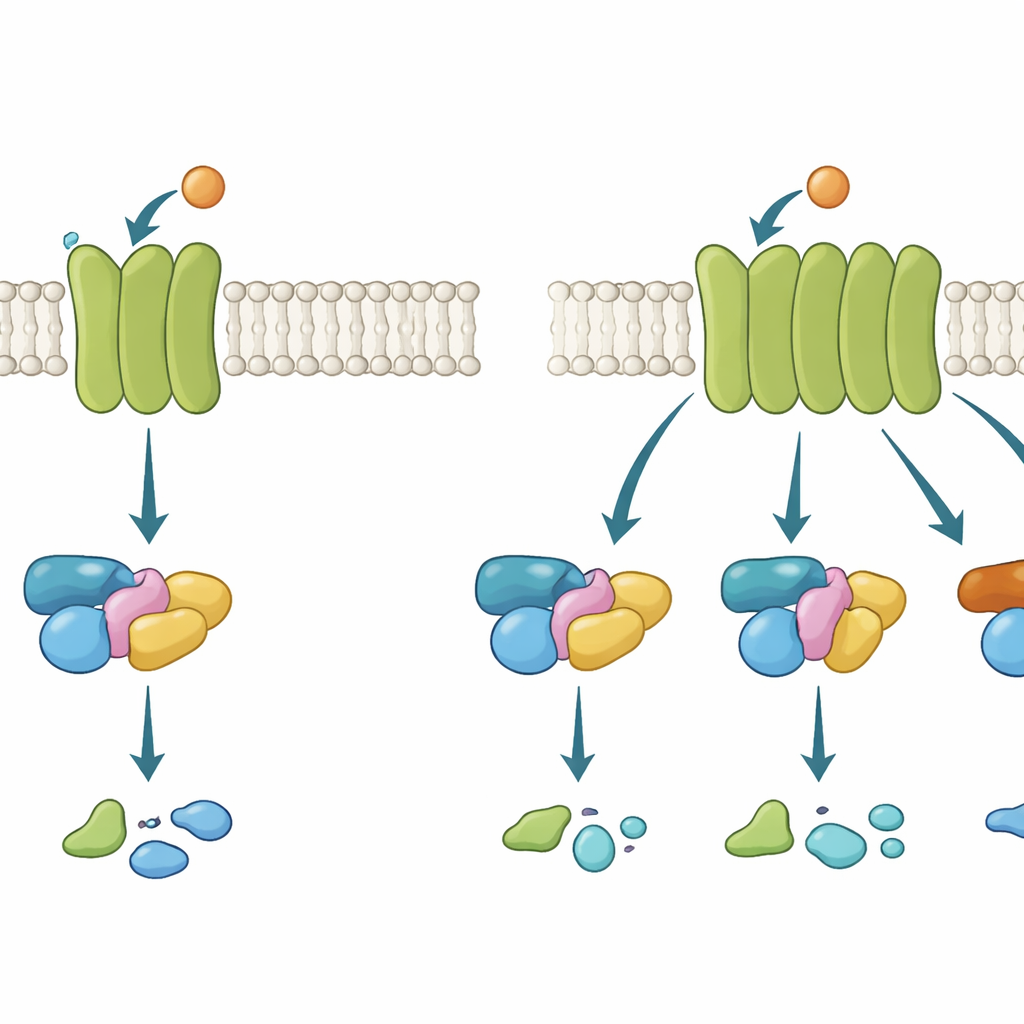
«Сотовые вышки» на мембране
Рецепторы, сопряжённые с G‑белками (GPCR), действуют как сотовые вышки, встроенные в наружную оболочку клетки. Когда молекула‑сигнал, например нейротрансмиттер ацетилхолин, связывается с рецептором снаружи, рецептор меняет конформацию внутри и привлекает G‑белок. Этот G‑белок затем переключается из неактивного состояния в активное и передаёт сигнал дальше. Существует несколько семейств G‑белков, каждое запускает разные клеточные ответы. Некоторые GPCR крайне разборчивы и используют только одно семейство; другие более «неразборчивы», вовлекая несколько семейств. Понимание того, что делает рецептор селективным или гибким, важно, поскольку многие успешные лекарства действуют, сдвигая эти пути.
Замена частей для перепрограммирования сигнала
Исследователи сосредоточились на двух близкородственных ацетилхолиновых рецепторах в мозге и периферии: рецепторе M2, который обычно сигнализирует главным образом через G‑белки типа Gi/o, и рецепторе M3, который предпочитает Gq‑тип, но может слабо вовлекать и Gi/o. Вместо того чтобы искать отдельные «волшебные» аминокислоты команда применила модульный подход. Они сконструировали химерные рецепторы — гибриды, в которых заменяли целые внутриклеточные сегменты между M2 и M3, такие как короткие петли внутри клетки, внутренние концы двух ключевых спиралей (обозначаемых как 5 и 6), короткая хвостовая спираль и участки хвоста, богатые положительно заряженными остатками. Для каждой химеры задавали два отдельных вопроса: связывается ли она с данным G‑белком и, если да, активирует ли его успешно?
Отдельное наблюдение связывания и активации
Чтобы отслеживать эти микроскопические взаимодействия, команда использовала оптические методы в живых клетках. В первом наборе экспериментов применяли метод FRET для определения того, насколько устойчиво рецептор удерживает G‑белок в контролируемых условиях, когда обычная энергопереносная нуклеотида GTP отсутствует. Это показывает, насколько вероятно и как долго пара рецептор–G‑белок остаётся вместе. Во втором наборе использовали родственный метод BRET с специальными сенсорными конструкциями, чтобы измерить, действительно ли связанные G‑белки переходят в активное состояние. Сравнивая поведение дикого типа и химерных рецепторов с двумя семействами G‑белков — Gi/o и Gq — исследователи могли выделить, какие структурные сегменты благоприятствуют какому партнёру и на каком этапе.
Многие мелкие изменения — большие сдвиги в поведении
Результаты показали, что ни одна внутренняя деталь сама по себе не служит простым выключателем выбора G‑белка. Вместо этого комбинации мотивов действуют совместно, а их эффекты зависят от рецепторного фона. Например, пересадка внутренних концов спиралей 5 и 6 из более гибкого рецептора M3 в селективный M2 смещала его к сигнализации преимущественно через Gq вместо Gi/o, в некоторых случаях превращая M2 в преимущественно Gq‑связанный рецептор. Добавление дополнительных сегментов петель могло восстановить способность связывать и активировать оба семейства G‑белков. Наоборот, вставка сегментов, похожих на M2, в M3 могла сделать его более склонным к Gi/o или, при изменениях в хвосте, сдвинуть его к почти исключительно Gq‑сигнализации. Поразительно, что некоторые химеры могли связывать G‑белок, не активируя его, в то время как другие могли вызывать активацию даже тогда, когда связывание было слишком кратковременным, чтобы его можно было зафиксировать в тесте связывания.
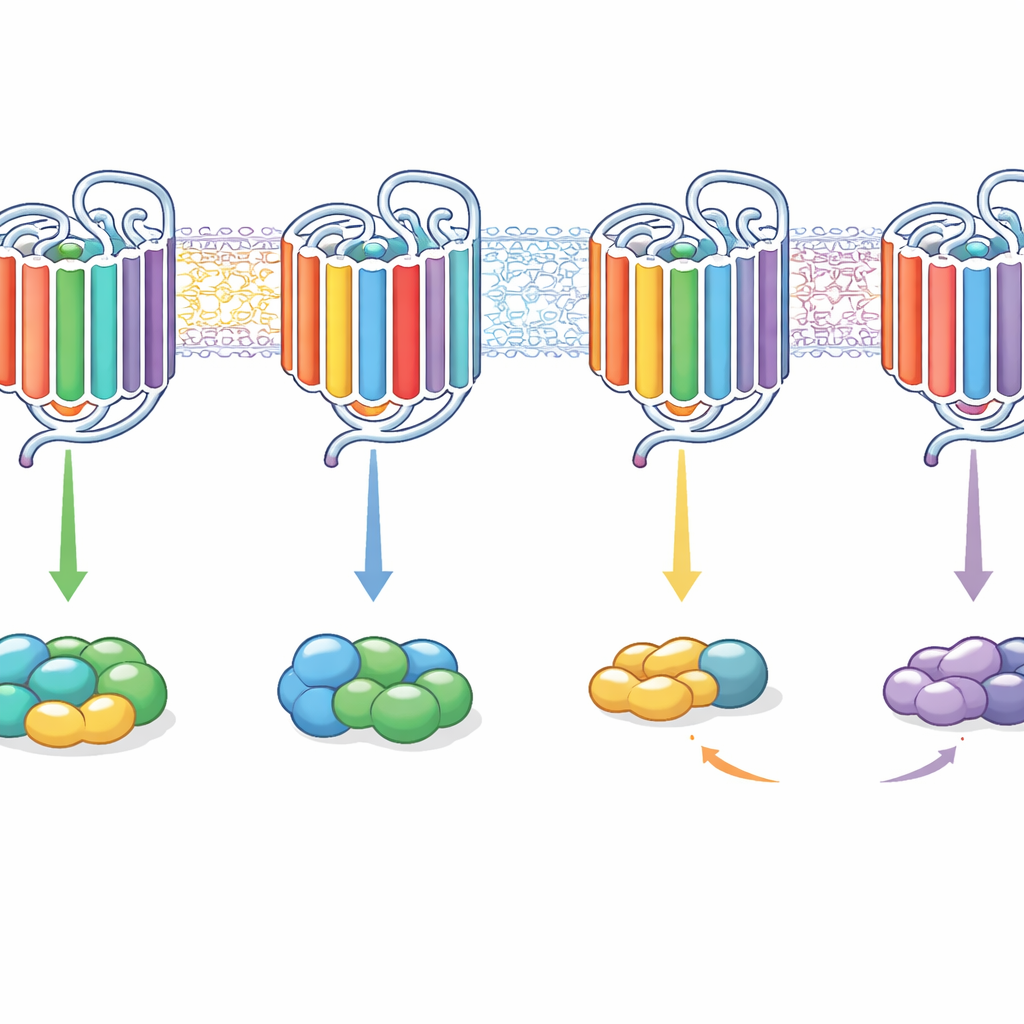
Что это значит для будущих лекарств
Проще говоря, эта работа показывает, что GPCR выбирают своих сигнальных партнёров не через один «ключевой» механизм, а через целую комбинацию внутренних частей. Внутренние петли, внутренние концы определённых спиралей и хвост совместно определяют, предпочитает ли рецептор одно семейство G‑белков, несколько или может связывать белки, не приводя к их полноценной активации. Искусно перераспределяя эти сегменты, авторы смогли перепрограммировать рецепторы от селективных к широко сигнализирующим и обратно. Для поиска лекарств это означает: настройка того, как рецептор использует свои внутренние «ручки», может позволить будущим препаратам направлять сигналы по полезным путям и избегать побочных эффектов без необходимости полного перепроектирования самого рецептора.
Цитирование: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Ключевые слова: рецепторы, связанные с G‑белками, мускариновые рецепторы, передача сигнала, селективность рецепторов, целевое действие препаратов