Clear Sky Science · sv
En komplex samverkan mellan olika intracellulära motiv avgör G-proteinsbindning och aktivering av muskarinreceptorer
Varför små cellulära brytare spelar roll för medicin
Varje sekund förlitar sig våra celler på små molekylära brytare kallade receptorer för att känna av hormoner, neurotransmittorer och läkemedel. En stor klass av dessa brytare, kända som G-proteinkopplade receptorer, sitter i cellmembranet och förmedlar besked inåt via partners som kallas G-proteiner. Vissa receptorer talar endast med en typ av G-protein, medan andra sänder till flera, vilket formar allt från hjärtfrekvens till humör. Denna studie ställer en till synes enkel fråga med stora implikationer för läkemedelsdesign: vilka egenskaper inne i en receptor avgör vilka G-proteiner den kommunicerar med — och hur starkt?
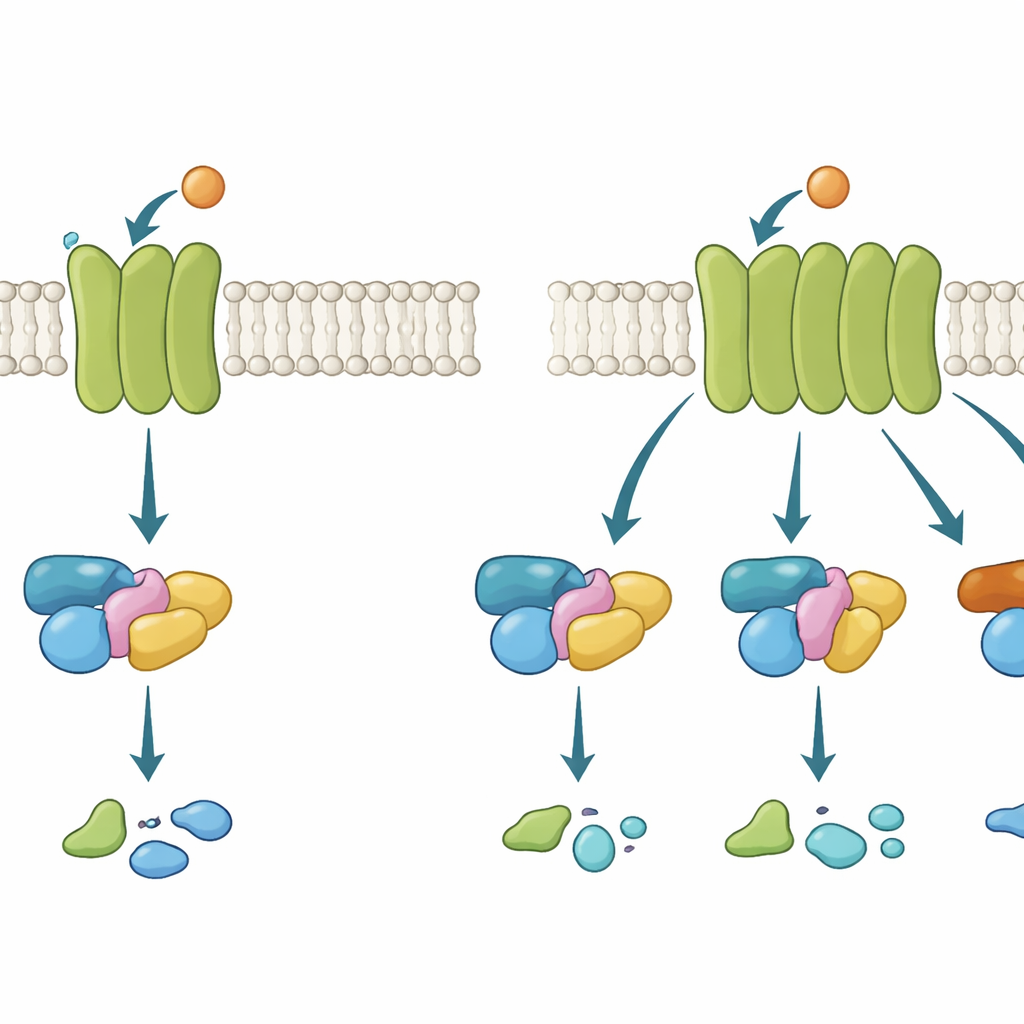
Mobilmaster på membranet
G-proteinkopplade receptorer (GPCR:er) fungerar lite som mobilmaster inbäddade i cellens yttre skikt. När en signalmolekyl, till exempel neurotransmittorn acetylkolin, binder på utsidan ändrar receptorn form på insidan och rekryterar ett G-protein. Det G-proteinet växlar då från ett inaktivt till ett aktivt tillstånd och förmedlar signalen vidare. Det finns flera G-proteinfamiljer, som var och en triggar olika cellulära svar. Vissa GPCR:er är mycket petiga och använder bara en familj; andra är mer promiscuösa och engagerar flera. Att förstå vad som gör en receptor selektiv eller flexibel är avgörande, eftersom många storsäljande läkemedel verkar genom att påverka dessa vägar.
Byta delar för att skriva om signalen
Forskarna fokuserade på två närbesläktade acetylkolinreceptorer i hjärna och kropp: M2-receptorn, som normalt signalerar främst via ett Gi/o-typ G-protein, och M3-receptorn, som föredrar ett Gq-typ G-protein men också svagt kan engagera Gi/o. Istället för att gissa enskilda ”magiska” aminosyror valde teamet en modulär strategi. De byggde kirala receptorer — hybrider där de bytte hela interna segment mellan M2 och M3, såsom de korta looparna inne i cellen, de inre ändarna av två viktiga helixar (kallade 5 och 6), en kort svanshelix och delar av svansen rika på positivt laddade rester. De ställde sedan två separata frågor för varje chimär: binder den till ett givet G-protein, och i så fall aktiverar den det framgångsrikt?
Observera bindning och aktivering separat
För att följa dessa mikroskopiska interaktioner använde teamet ljusbaserade metoder i levande celler. I en första uppsättning experiment använde de en teknik kallad FRET för att upptäcka hur stabilt en receptor håller fast vid ett G-protein i ett kontrollerat läge där det vanliga energibärande nukleotidet GTP är frånvarande. Detta avslöjar hur sannolikt och hur länge ett receptor–G-protein-par stannar ihop. I en andra uppsättning experiment använde de en närbesläktad metod, BRET, med specialiserade sensors Konstruktioner för att mäta om de bundna G-proteinerna faktiskt växlar till sitt aktiva tillstånd. Genom att jämföra hur vildtyp- och chimära receptorer hanterade två G-proteinfamiljer — Gi/o och Gq — kunde forskarna urskilja vilka strukturella segment som gynnade vilken partner och i vilket steg.
Många små förändringar, stora beteendeskiften
Resultaten visade att ingen enskild intern egenskap fungerade som en av- och på-knapp för val av G-protein. Istället samarbetade kombinationer av motiv, och deras effekter berodde på receptorbakgrunden. Till exempel förflyttade transplantationen av de inre ändarna av helixar 5 och 6 från den mer flexibla M3-receptorn till den selektiva M2-receptorn dess signalering mot huvudsakligen Gq istället för Gi/o, i vissa fall och gjorde M2 till en huvudsakligen Gq-kopplad receptor. Att lägga till ytterligare loopsegment kunde återställa förmågan att både binda och aktivera båda G-proteinfamiljerna. Omvänt kunde insättning av M2-liknande segment i M3 få den att favorisera Gi/o starkare eller, med förändringar i dess svans, driva den mot att signalera nästan uteslutande via Gq. Slående var att vissa chimärer kunde binda ett G-protein utan att aktivera det, medan andra fortfarande kunde utlösa aktivering även när bindningen var för flyktig för att upptäckas med bindningsassayet.
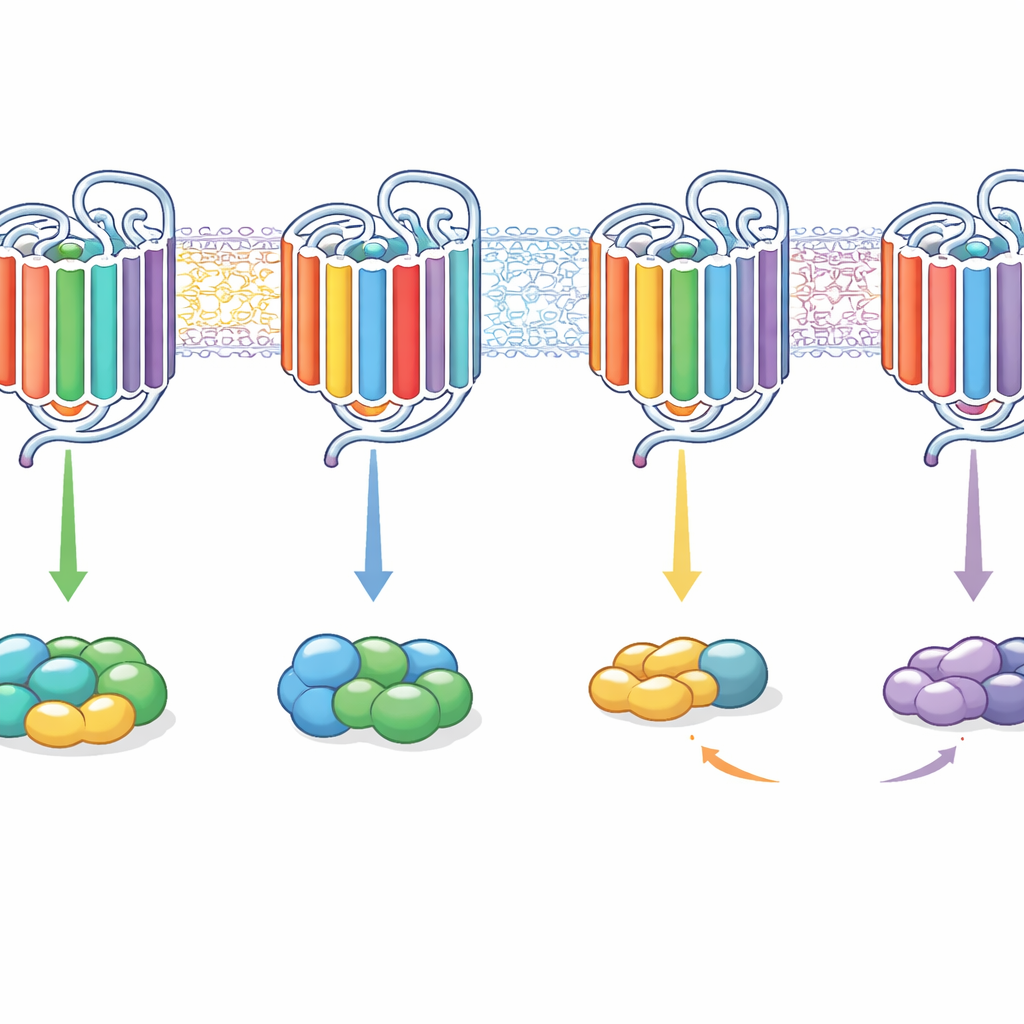
Vad detta betyder för framtida läkemedel
På vardagsspråk visar detta arbete att GPCR:er väljer sina signaleringspartners inte genom ett enda nyckelhål utan genom ett helt kombinationslås av interna delar. De inre looparna, de inre ändarna av vissa helixar och svansen bidrar alla i samordning till om en receptor föredrar en G-proteinfamilj, flera eller kan binda utan att verkligen slå på dem. Genom att skickligt omfördela dessa segment kunde författarna omprogrammera receptorer från selektiv till bred signalering och tillbaka igen. För läkemedelsforskning antyder detta att finjustering av hur en receptor använder sina olika inre ”vred” kan låta framtida läkemedel styra signaler mot gynnsamma vägar och bort från biverkningar, utan att behöva helt redesigna receptorn själv.
Citering: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Nyckelord: G-proteinkopplade receptorer, muskarina receptorer, signaltransduktion, receptorselektivitet, Läkemedelsinriktning