Clear Sky Science · fr
Une interaction complexe entre divers motifs intracellulaires détermine la liaison et l’activation des protéines G par les récepteurs muscariniques
Pourquoi ces petits interrupteurs cellulaires comptent pour la médecine
Chaque seconde, nos cellules s’appuient sur de petits interrupteurs moléculaires appelés récepteurs pour détecter hormones, neurotransmetteurs et médicaments. Une grande classe de ces interrupteurs, connue sous le nom de récepteurs couplés aux protéines G (RCPG), siège dans la membrane cellulaire et transmet des messages vers l’intérieur via des partenaires appelés protéines G. Certains récepteurs ne communiquent qu’avec un type de protéine G, tandis que d’autres diffusent le signal vers plusieurs, influençant tout, du rythme cardiaque à l’humeur. Cette étude pose une question apparemment simple mais importante pour la conception des médicaments : quelles caractéristiques internes d’un récepteur déterminent à quelles protéines G il s’adresse — et avec quelle intensité ?
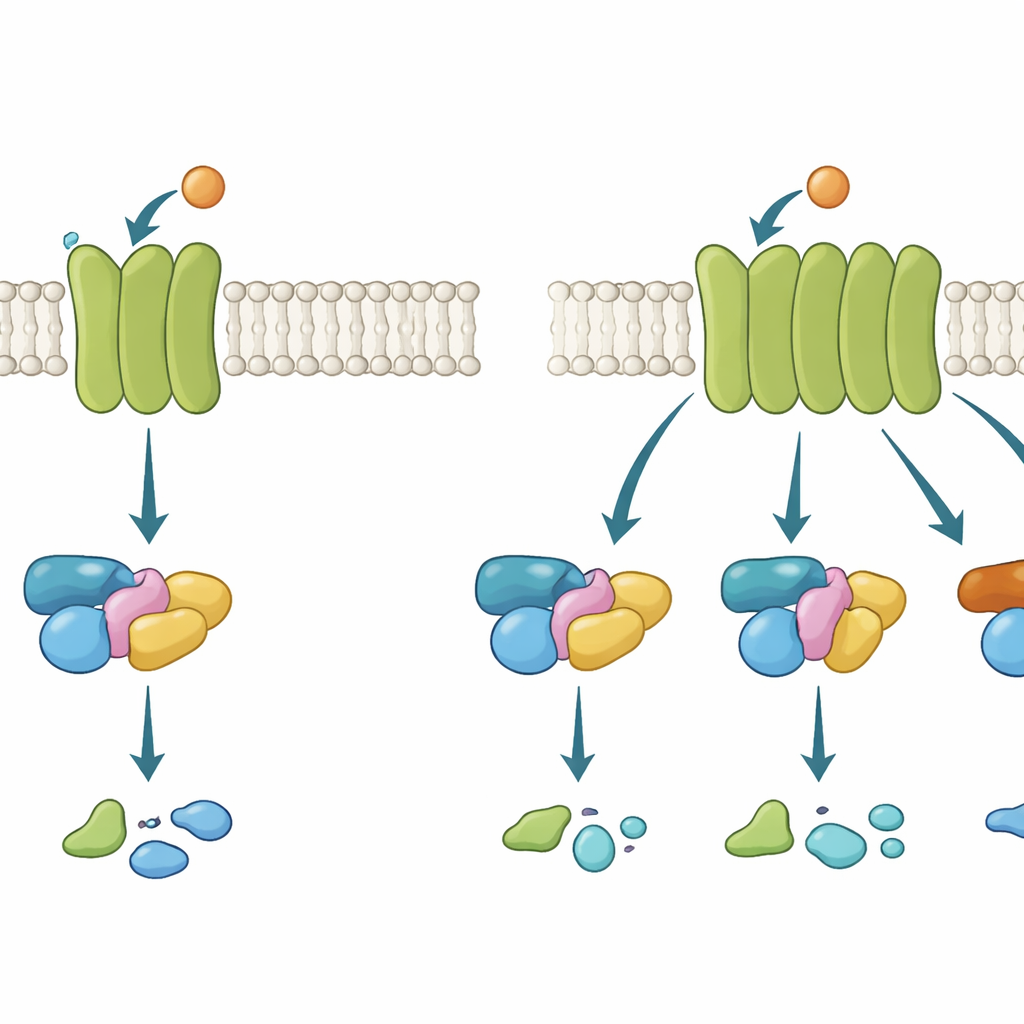
Des antennes téléphoniques sur la membrane
Les récepteurs couplés aux protéines G agissent un peu comme des antennes de téléphonie mobile intégrées à l’enveloppe externe de la cellule. Quand une molécule signal, comme le neurotransmetteur acétylcholine, se lie à l’extérieur, le récepteur change de conformation à l’intérieur et recrute une protéine G. Cette protéine G passe alors d’un état inactif à un état actif et transmet le message. Il existe plusieurs familles de protéines G, chacune déclenchant des réponses cellulaires différentes. Certains RCPG sont très exigeants et n’utilisent qu’une seule famille ; d’autres sont plus flexibles et en sollicitent plusieurs. Comprendre ce qui rend un récepteur sélectif ou polyvalent est crucial, car de nombreux médicaments majeurs agissent en modulant ces voies.
Échanger des parties pour réécrire le signal
Les chercheurs se sont concentrés sur deux récepteurs à l’acétylcholine étroitement liés, présents dans le cerveau et le corps : le récepteur M2, qui signale normalement principalement via une protéine G de type Gi/o, et le récepteur M3, qui préfère une protéine G de type Gq mais peut aussi, faiblement, engager Gi/o. Plutôt que de rechercher un seul acide aminé « magique », l’équipe a adopté une approche modulaire. Ils ont construit des récepteurs chimériques — des hybrides dans lesquels ils ont interverti des segments internes entiers entre M2 et M3, tels que de courtes boucles intracellulaires, les extrémités internes de deux hélices clés (appelées 5 et 6), un court hélice terminale et des portions de la queue riches en résidus positivement chargés. Ils ont ensuite posé deux questions distinctes pour chaque chimère : se lie-t-il à une protéine G donnée, et si oui, l’active-t-il réellement ?
Observer séparément la liaison et l’activation
Pour suivre ces interactions microscopiques, l’équipe a utilisé des méthodes optiques dans des cellules vivantes. Dans une première série d’expériences, ils ont employé une technique appelée FRET pour détecter la stabilité avec laquelle un récepteur retient une protéine G dans un contexte contrôlé où le nucléotide transporteur d’énergie habituel, le GTP, est absent. Cela révèle la probabilité et la durée pendant lesquelles une paire récepteur–protéine G reste associée. Dans une deuxième série d’expériences, ils ont utilisé une méthode apparentée, la BRET, avec des capteurs spécialisés pour mesurer si les protéines G liées passent effectivement à leur état actif. En comparant la façon dont les récepteurs sauvages et chimériques traitaient deux familles de protéines G — Gi/o et Gq — les chercheurs ont pu démêler quels segments structurels favorisaient quel partenaire et à quelle étape.
Beaucoup de petits changements, de grands changements de comportement
Les résultats montrent qu’aucune caractéristique interne unique n’agit comme un interrupteur marche/arrêt pour le choix de la protéine G. Au lieu de cela, des combinaisons de motifs agissent ensemble, et leurs effets dépendent du contexte du récepteur. Par exemple, transplanter les extrémités internes des hélices 5 et 6 du récepteur M3, plus flexible, dans le récepteur sélectif M2 l’a fait basculer pour signaler principalement via Gq plutôt que Gi/o, transformant dans certains cas M2 en un récepteur principalement couplé à Gq. L’ajout d’autres segments de boucle pouvait restaurer la capacité de se lier et d’activer les deux familles de protéines G. Inversement, l’insertion de segments de type M2 dans M3 pouvait le rendre plus favorable à Gi/o ou, avec des modifications de sa queue, le pousser vers une signalisation presque exclusivement via Gq. De manière frappante, certains chimères pouvaient se lier à une protéine G sans l’activer, tandis que d’autres pouvaient encore déclencher l’activation même lorsque la liaison était trop brève pour être détectée avec l’essai de liaison.
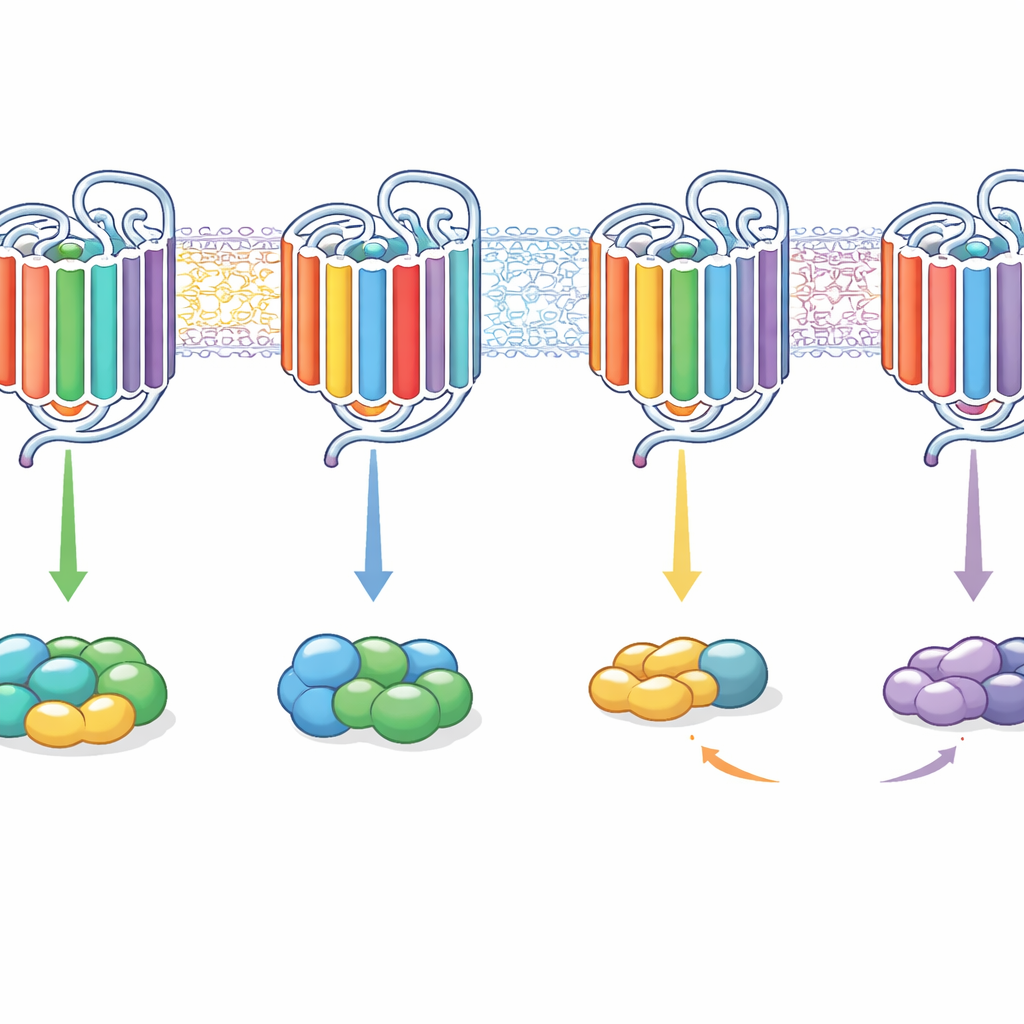
Ce que cela signifie pour les médicaments de demain
Concrètement, ce travail montre que les RCPG choisissent leurs partenaires de signalisation non pas par un simple trou de serrure, mais par une combinaison complexe de pièces internes. Les boucles internes, les extrémités internes de certaines hélices et la queue contribuent de manière coordonnée à la préférence d’un récepteur pour une famille de protéines G, plusieurs d’entre elles, ou à la capacité de se lier sans réellement les activer. En réorganisant habilement ces segments, les auteurs ont pu reprogrammer des récepteurs, passant de la sélectivité à une signalisation large et vice versa. Pour la découverte de médicaments, cela suggère que régler la façon dont un récepteur utilise ses différents « réglages » internes pourrait permettre à de futurs traitements d’orienter les signaux vers des voies bénéfiques et d’éviter les effets secondaires, sans avoir à redesigner complètement le récepteur lui‑même.
Citation: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Mots-clés: récepteurs couplés aux protéines G, récepteurs muscariniques, transduction du signal, sélectivité des récepteurs, ciblage médicamenteux