Clear Sky Science · he
אינטראקציה מורכבת של מוטיבים תוך-תאיים קובעת את קשירת וחילוף חלבון G בקולטני מוסקרין
למה ממסרים זעירים בתא חשובים לרפואה
כל שנייה, תאים שלנו מסתמכים על ממסרים מולקולריים זעירים הנקראים קולטנים כדי לחוש הורמונים, תרגילי-עצב (נוירוטרנסמיטרים) ותרופות. מחלקה מרכזית של ממסרים אלה, הידועה כקולטנים מצומדי חלבון G, יושבת בממברנת התא ומעבירה מסרים פנימה באמצעות שותפים הנקראים חלבוני G. חלק מהקולטנים מתקשרים רק עם סוג אחד של חלבון G, בעוד שאחרים משדרים למספר סוגים, ועיצוב זה משפיע על הכול מהדופק ועד מצב הרוח. המחקר הזה שואל שאלה שנראית פשוטה אך בעלת השלכות גדולות על עיצוב תרופות: אילו תכונות בתוך הקולטן קובעות עם אילו חלבוני G הוא מתקשר — ובאיזו עוצמה?
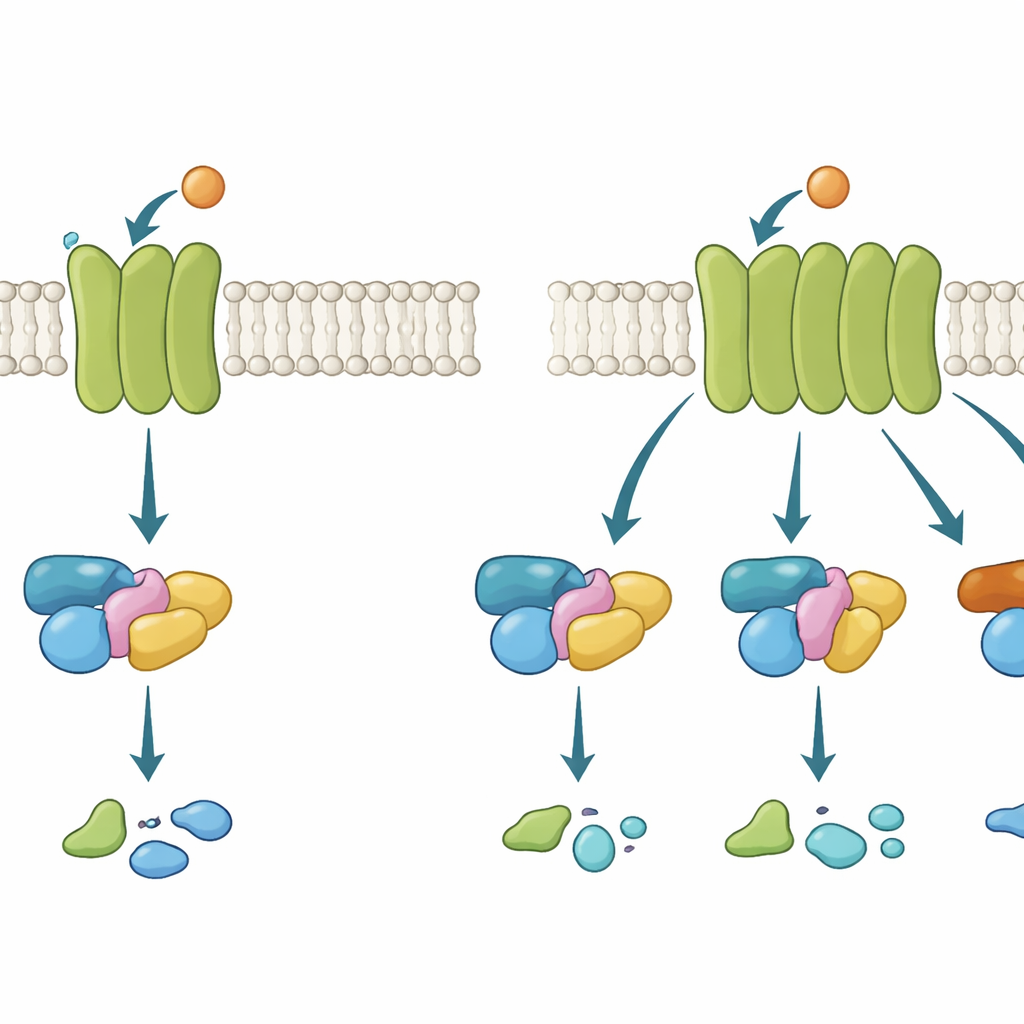
מגדלי סלולר על הממברנה
קולטנים מצומדי חלבון G (GPCRs) פועלים במעטה כמו מגדלי סלולר הטבועים בקליפת התא החיצונית. כשהמולקולה המשדרת, כמו הנוירוטרנסמיטר אצטילכולין, נקשרת מבחוץ, הקולטן משנה צורה בפנים ומגייס חלבון G. חלבון ה‑G הזה אז עובר ממצב לא פעיל לפעיל וממשיך את המסר. יש כמה משפחות של חלבוני G, שכל אחת מהן גורמת לתגובות תאיות שונות. חלק מה‑GPCRs בררניים מאוד ומשתמשים רק במשפחה אחת; אחרים גמישים יותר ומגייסים כמה. הבנת מה עושה קולטן לסלקטיבי או גמיש היא קריטית, משום שרבות מהתרופות המובילות פועלות על ידי דחיפה עדינה של מסלולים אלה.
החלפת חלקים כדי לכתוב מחדש את האות
החוקרים התרכזו בשני קולטני אצטילכולין קרובים זה לזה במוח ובגוף: הקולטן M2, שבדרך כלל משדר בעיקר דרך חלבון G מסוג Gi/o, וה‑M3, שמעדיף חלבון G מסוג Gq אך יכול גם להפעיל חלש Gi/o. במקום לנחש חומצות אמינו בודדות 'קסומות', הצוות נקט בגישה מודולרית. הם בנו קולטן כימרי — היברידים שבהם החליפו מקטעים פנימיים שלמים בין M2 ל‑M3, כגון לולאות קצרות בתוך התא, הקצוות הפנימיים של שתי הלים מרכזיות (המכונות 5 ו‑6), הל helix זנב קצר ומקטעי זנב עשירים ברקמות חיוביות. הם אחר כך שאלו שתי שאלות נפרדות לכל כימרה: האם היא נקשרת לחלבון G מסוים, ואם כן — האם היא מצליחה להפעילו?
צפייה בקשירה ובהפעלה בנפרד
כדי לעקוב אחרי אינטראקציות זעירות אלה, הצוות השתמש בשיטות מוארת בתאים חיים. בקבוצת ניסויים ראשונה השתמשו בטכניקה הנקראת FRET כדי לזהות עד כמה יציב הקולטן מחזיק חלבון G בסביבה מבוקרת שבה הנוקליאוטיד הנושא אנרגיה GTP נעדר. שיטה זו מגלה כמה סביר ולכמה זמן זוג קולטן–חלבון G נשאר יחד. בקבוצת ניסויים שנייה השתמשו בשיטה קשורה, BRET, עם חיישנים מיוחדים כדי למדוד האם חלבוני ה‑G הקשורים למעשה עוברים למצב הפעיל שלהם. בהשוואה בין הקולטנים הבריאים לכימריים בהתמודדות עם שתי משפחות חלבוני G — Gi/o ו‑Gq — החוקרים יכלו להבחין אילו מקטעים מבנים העדיפו איזה שותף ובאיזו שלב.
הרבה שינויים קטנים, שינויים גדולים בהתנהגות
התוצאות הראו שאף תכונה פנימית יחידה אינה שפיתה דולקת/כבויה לבחירת חלבון G. במקום זאת, קומבינציות של מוטיבים פעלו יחד, וההשפעות שלהן תלויות ברקע הקולטן. למשל, השתלת הקצוות הפנימיים של ההלים 5 ו‑6 מהקולטן הגמיש יותר M3 לתוך הקולטן הסלקטיבי M2 העבירה אותו לאות בעיקר דרך Gq במקום Gi/o, ובמקרים מסוימים הפכה את M2 לקולטן שמצומד בעיקר ל‑Gq. הוספת מקטעי לולאות נוספים יכלה לשחזר את היכולת לקשור ולהפעיל את שתי משפחות חלבוני ה‑G. להפך, הכנסת מקטעים בסגנון M2 ל‑M3 יכלה לגרום לו להעדיף חזק יותר את Gi/o או, בשינויי זנב, לדחוף אותו לכיוונון כמעט בלעדי דרך Gq. מעניין שברבים מהמקרים כימריים יכלו לקשור חלבון G בלי להפעילו, בעוד שאחרים יכלו עדיין לגרום להפעלה גם כשהקשירה היתה קצרה מדי כדי להתגלות במבחן הקשירה.
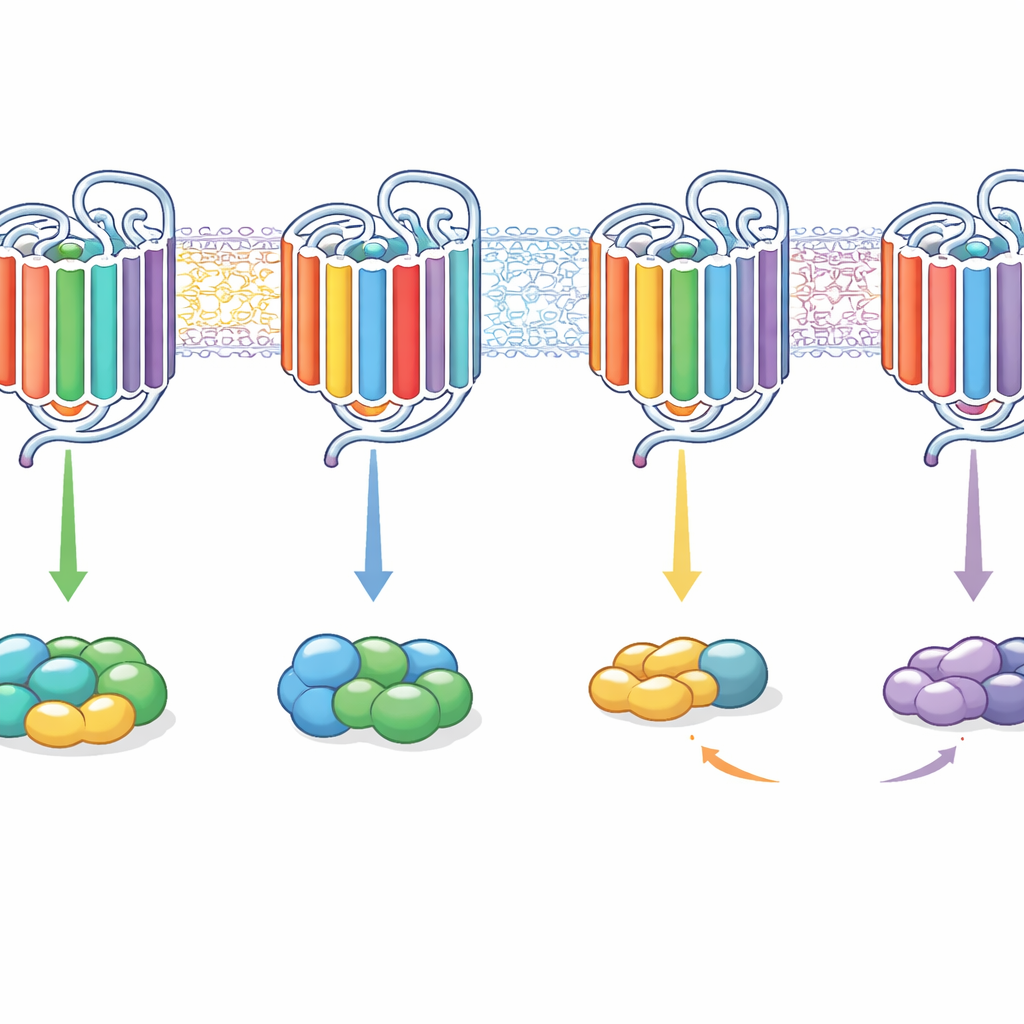
מה משמעות הדבר עבור תרופות עתידיות
במונחים פשוטים, עבודה זו מראה שקולטני GPCR בוחרים את שותפי האות שלהם לא דרך מנעול-מפתח יחיד אלא דרך מנגנון של קוד משולב של חלקים פנימיים. הלולאות הפנימיות, הקצוות הפנימיים של הלליות מסוימות והזנב כולם תורמים בתיאום לשאלה האם קולטן מעדיף משפחת חלבון G אחת, כמה משפחות, או יכול לקשור בלי באמת להפעיל. על ידי ערבוב חכם של מקטעים אלה, המחברים יכלו לתכנת מחדש קולטנים מסלקטיביים לרוחב-שידור ולהפך. עבור גילוי תרופות, הדבר מציע שהכוונת ה'דיאלוג' הפנימי של הקולטן יכולה לאפשר לתרופות לעתיד להכווין אותות למסלולים מועילים ולהרחיק מס副תיות, מבלי לייצר מחדש את הקולטן כולו.
ציטוט: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
מילות מפתח: קולטנים מצומדי חלבון G, קולטני מוסקרין, העברת אותות, סלקטיביות של קולטנים, מיקוד תרופתי