Clear Sky Science · tr
Çeşitli hücre içi motiflerin karmaşık etkileşimi muskarninik reseptörlerin G proteine bağlanmasını ve aktivasyonunu belirler
İlaçlar için neden küçük hücre anahtarları önemli
Her saniye hücrelerimiz, hormonları, nörotransmitterleri ve ilaçları algılamak için reseptör adı verilen küçük moleküler anahtarlara güvenir. Bu anahtarların önemli bir sınıfı olan G proteinine bağlı reseptörler (GPCR'ler) hücre zarına gömülüdür ve G proteinleri adı verilen ortaklar aracılığıyla mesajları hücre içine iletir. Bazı reseptörler yalnızca tek bir G protein türüyle konuşurken, diğerleri birden fazlasına yayın yapar; bu durum kalp atış hızından ruh haline kadar pek çok şeyi şekillendirir. Bu çalışma, ilaç tasarımı için büyük sonuçları olan, görünüşte basit bir soruyu soruyor: bir reseptörün içinde hangi özellikler hangi G proteinleriyle konuşacağını —ve ne kadar güçlü konuşacağını— belirler?
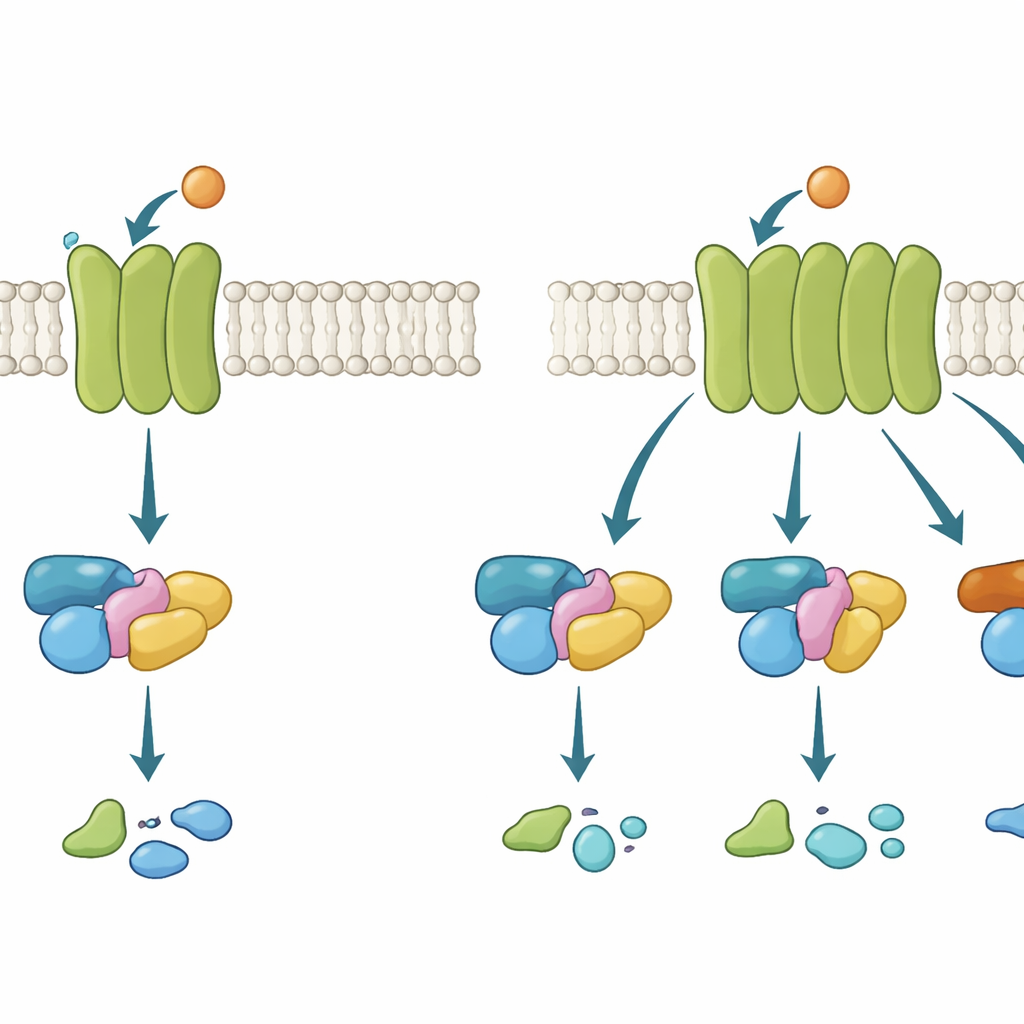
Zar üzerindeki cep telefonu kuleleri
G proteinine bağlı reseptörler (GPCR'ler), hücrenin dış kabuğuna gömülü cep telefonu kuleleri gibi davranır. Bir sinyal molekülü, örneğin nörotransmitter asetilkolin, dış tarafta bağlandığında, reseptör iç tarafta şekil değiştirir ve bir G proteinini çağırır. O G proteini daha sonra inaktif durumdan aktif duruma geçer ve mesajı iletir. Birkaç G protein ailesi vardır ve her biri farklı hücresel yanıtları tetikler. Bazı GPCR'ler çok seçicidir ve yalnızca bir aileyi kullanır; bazıları daha esnektir ve birkaçını birden bağlar. Bir reseptörü seçici veya esnek yapanın ne olduğunu anlamak önemlidir çünkü pek çok önemli ilaç bu yolları hafifçe iterek etki eder.
Sinyali yeniden yazmak için parçaları değiştirmek
Araştırmacılar beyindeki ve vücuttaki iki yakından ilişkili asetilkolin reseptörüne odaklandı: normalde ağırlıklı olarak Gi/o tipi G proteini aracılığıyla sinyal veren M2 reseptörü ve tercihen Gq tipi G proteini kullanan ancak zayıf da olsa Gi/o ile etkileşebilen M3 reseptörü. Tek bir “sihirli” amino asidi tahmin etmek yerine ekip modüler bir yaklaşım benimsedi. M2 ve M3 arasında tüm iç segmentleri değiştirdikleri kimerik reseptörler—hücresi içindeki kısa döngüler, iki önemli heliksin (5 ve 6) iç uçları, kısa bir kuyruk heliksi ve pozitif yüklü kalıntaklarla zengin kuyruk bölgeleri gibi—oluşturdular. Ardından her kimer için iki ayrı soru sordular: belirli bir G proteine bağlanıyor mu ve bağlanıyorsa onu başarılı şekilde aktive ediyor mu?
Bağlanmayı ve aktivasyonu ayrı ayrı izlemek
Bu mikroskobik etkileşimleri izlemek için ekip canlı hücrelerde ışık temelli yöntemler kullandı. İlk deney dizisinde, klasik enerji taşıyıcısı nükleotid GTP'nin bulunmadığı kontrollü bir ortamda FRET adlı bir teknik kullanarak bir reseptörün bir G proteinine ne kadar istikrarlı bağlandığını tespit ettiler. Bu, bir reseptör–G protein çiftinin bir arada kalma olasılığını ve süresini ortaya koyar. İkinci deney dizisinde ise BRET adlı bağlantılı bir yöntem ve özel sensör yapıları kullanılarak, bağlanmış G proteinlerin gerçekten aktif duruma geçip geçmediği ölçüldü. Vahşi tip ve kimerik reseptörlerin iki G protein ailesi—Gi/o ve Gq—ile nasıl davrandığını karşılaştırarak, hangi yapısal segmentlerin hangi adımı tercih ettiğini ayırt edebildiler.
Birçok küçük değişiklik, davranışta büyük kaymalar
Sonuçlar gösterdi ki tek bir iç özellik G protein seçimi için açık-kapalı düğmesi gibi davranmıyordu. Bunun yerine motiflerin kombinasyonları birlikte hareket ediyor ve etkileri reseptörün arka planına bağlı olarak değişiyordu. Örneğin, daha esnek olan M3 reseptörünün heliks 5 ve 6’nın iç uçlarını seçici M2'ye nakletmek, M2'yi bazı durumlarda Gi/o yerine ağırlıklı olarak Gq üzerinden sinyal veren bir reseptöre kaydırdı; bazı durumlarda M2'yi ağırlıklı olarak Gq-bağlı hale getirdi. İlave döngü segmentleri eklemek hem G protein ailelerine bağlanma hem de onları aktifleştirme yeteneğini geri getirebiliyordu. Tersine, M2 benzeri segmentleri M3'e yerleştirmek, M3'ün Gi/o'yu daha güçlü tercih etmesine veya kuyruğundaki değişikliklerle neredeyse tamamen Gq üzerinden sinyal vermeye itmesine neden olabiliyordu. Dikkat çekici biçimde bazı kimerler bir G proteine bağlanabildiği halde onu aktive edemiyor, diğerleri ise bağlanma bağlanmanın belirgin olmadığı kadar kısa olsa bile yine de aktivasyonu tetikleyebiliyordu.
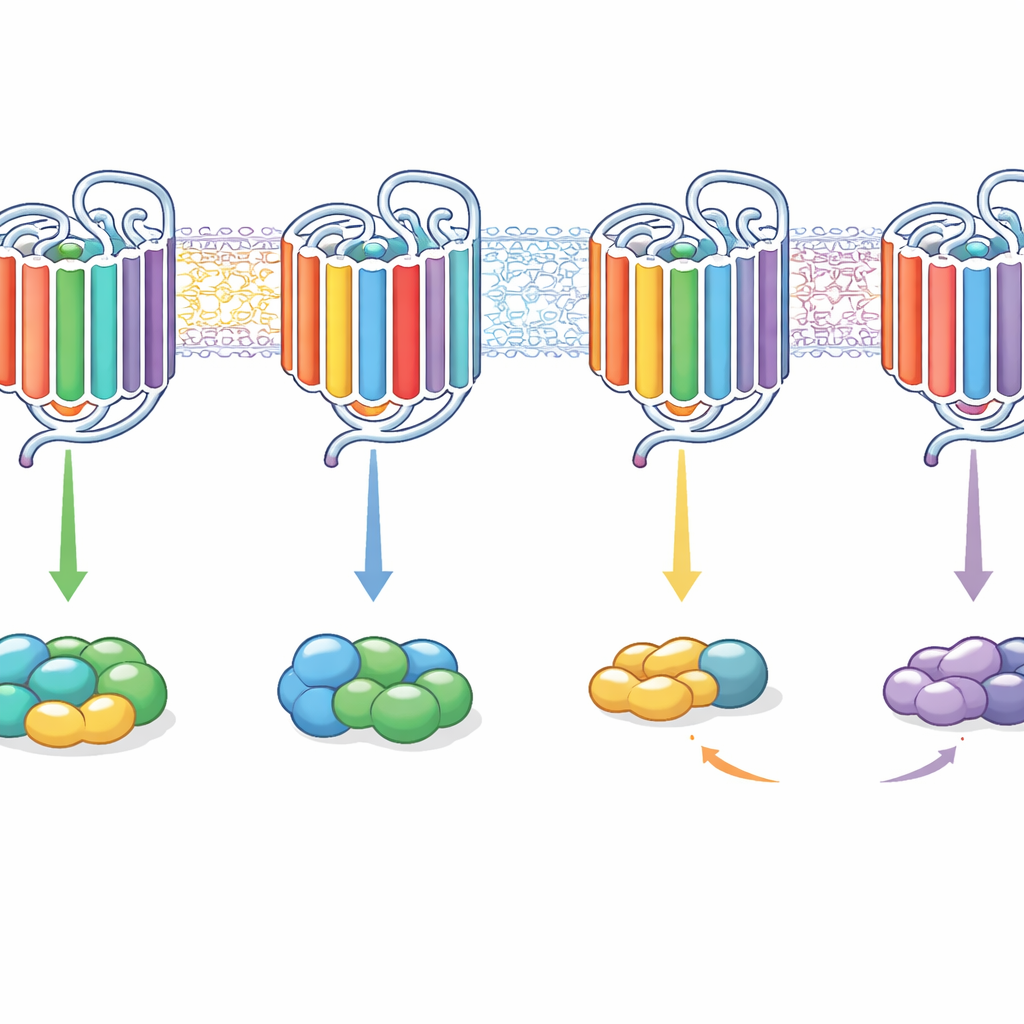
Gelecekteki ilaçlar için bunun anlamı
Günlük anlatımla bu çalışma, GPCR'lerin sinyal ortaklarını tek bir anahtar deliği aracılığıyla değil, iç parçaların bütünü bir kombinasyon kilidi gibi seçtiğini gösteriyor. İç döngüler, belirli helikslerin iç uçları ve kuyruk, bir reseptörün tek bir G protein ailesini, birkaçını tercih edip etmeyeceğine veya bağlanıp bağlansa bile onları gerçekten açıp açmayacağına koordineli şekilde katkıda bulunur. Bu segmentleri ustalıkla yeniden düzenleyerek yazarlar reseptörleri seçiciden yaygın sinyal verene ve tekrar geri çevirebildiler. İlaç keşfi için bu, bir reseptörün çeşitli iç “düzenlerini” nasıl kullandığını ayarlamanın, gelecekteki ilaçların sinyalleri yararlı yollara yönlendirip yan etkilere gidenleri azaltmasına izin verebileceğini, reseptörü tamamen yeniden tasarlamaya gerek kalmadan önerir.
Atıf: Kirchhofer, S.B., Jelinek, V., Klingelhöfer, K. et al. A complex interplay of various intracellular motifs determines G protein binding and activation of muscarinic receptors. Sci Rep 16, 12370 (2026). https://doi.org/10.1038/s41598-026-48667-0
Anahtar kelimeler: G proteinine bağlı reseptörler, muskarninik reseptörler, sinyal iletimi, reseptör seçiciliği, ilaç hedefleme