Clear Sky Science · zh
细菌脂多糖抑制α-凝血酶活性的分子基础
为何细菌毒素与血栓相关
由革兰氏阴性菌引发的严重感染可将机体推入一种危险的恶性循环,血液开始不受控地凝固,阻塞微小血管并损害器官。本研究提出了一个看似简单却意义深远的问题:当细菌细胞壁的片段进入血流时,它们是否会以物理方式干扰凝血酶——这一促成血栓的关键酶?通过揭示特定细菌分子如何与凝血酶相互作用,这项工作阐明了为何脓毒症相关的凝血问题在不同患者间差异巨大,并可能为预测或控制这些危及生命的事件提供新的思路。
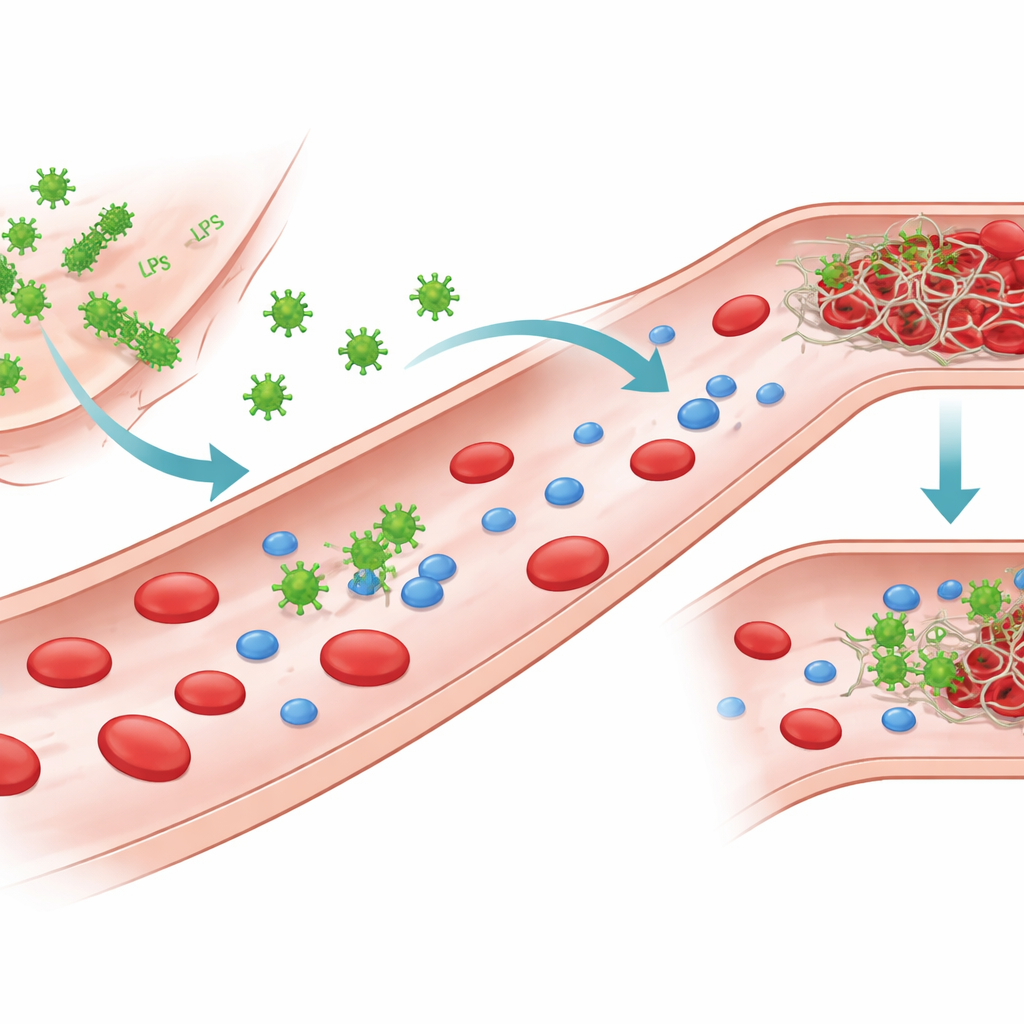
与血液“对话”的细菌片段
革兰氏阴性菌在其外表面携带一种强活性的分子——脂多糖(LPS)。当细菌受损或被破坏时,LPS 可释放并在血液中循环。作者关注了来自几种常见病原体的 LPS,包括两株大肠杆菌,以及克雷伯氏肺炎菌和铜绿假单胞菌。尽管它们基于相同的基本骨架,不同菌株在糖链和电荷分布上存在差异,形成不同的“化学型”。这些结构差异改变了 LPS 在水中如何聚集,可能以单个分子、小簇或更大的片状组装体存在,同时也影响 LPS 与血中蛋白的相互作用。
LPS 如何抓住凝血酶
凝血酶表面有两个带强正电荷的斑块,称为外位点,通常帮助其识别并定位天然配体如纤维蛋白原和调节性辅因子。由于 LPS 带有强负电荷,研究团队推测它可能钩住这些区域。通过结合测定和灵敏的荧光检测相结合的方法,他们证明了四种细菌的 LPS 确实可以与凝血酶结合。然而,只有某些化学型——尤以一株大肠杆菌(O26:B6)和克雷伯氏肺炎菌为代表——诱导了凝血酶的明显构象变化。通过使用短的基于 DNA 的探针阻断各外位点,研究者证明 LPS 必须接触这些带电斑块才能产生作用,从而证实结合发生在凝血酶执行其正常功能所用的相同表面。
当细菌片段放慢凝血“机器”
为检验这种结合是否实际改变了凝血酶的性能,作者跟踪了酶切割小型模型底物的速率以及将纤维蛋白原转化为纤维蛋白网络的效率。他们发现特定的 LPS 化学型,尤其是大肠杆菌 O26:B6 和克雷伯氏肺炎菌,能显著降低凝血酶的催化能力,有时下降超过百倍。这种抑制不仅取决于 LPS 的类型,还取决于 LPS 分子的组织方式。当 LPS 以较小、曲率更大的簇状存在时,它与凝血酶接触更紧密并强烈抑制其活性;当钙离子促使 LPS 形成更大、更有序的聚集体时,对于某些化学型而言,抑制作用会减弱甚至消失。重要的是,这些模式在凝块形成实验中也同样显现:某些 LPS 形式可在纯化体系中完全阻止纤维蛋白网络的组装,而另一些则只是减慢或甚至加速凝块生长。
不同细菌,不同凝血结局
在血浆这一更复杂的环境中,许多其他蛋白参与竞争,故事变得更为丰富。在这种更接近生理的背景下,LPS 化学型仍然呈现出截然不同的“指纹”。在低浓度时,几种类型会延迟凝血的起始,但在较高水平时,许多类型会转为促凝行为,缩短凝血时间。一种大肠杆菌化学型 O26:B6尤为突出:当其 LPS 组装成由钙稳定的聚集体时,即使在高浓度下仍持续减慢凝血,暗示该菌株可能促成持续性的凝血生成受损。总体而言,这项工作表明 LPS 的微观化学特性及其宏观的聚集状态共同决定了凝血酶是被抑制、保持不变,还是被推动向更快的凝血方向发展。
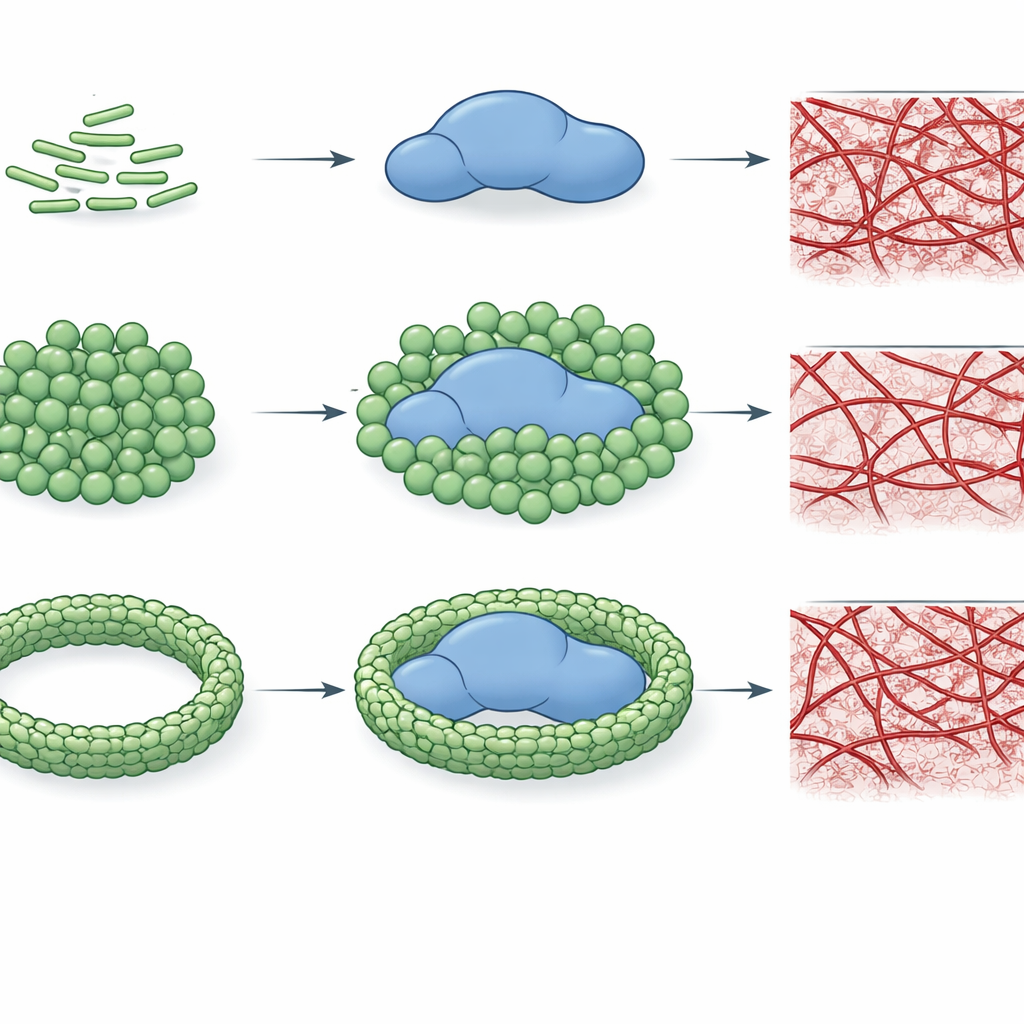
这对脓毒症与血液健康的意义
作者得出结论:细菌 LPS 不仅是远程诱导炎症的触发物,还能通过物理接触直接调节凝血酶的活性,其影响因细菌菌株不同并取决于分子在血流中的聚集状态而异。从实践角度看,这意味着即便总体感染负荷相同,不同 LPS 混合物和存在状态也会导致截然不同的凝血模式。通过绘制这一新的相互作用层面,该研究有助于解释为何脓毒症既能引起过度凝血又能导致凝血功能受损,并为针对 LPS—凝血酶结合或干预 LPS 组织状态以恢复机体凝血平衡的治疗策略打开了可能的大门。
引用: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
关键词: 脓毒症, 凝血酶, 脂多糖, 血液凝固, 革兰氏阴性菌