Clear Sky Science · es
Base molecular de la inhibición de la actividad de la α-trombina por lipopolisacáridos bacterianos
Por qué importan las toxinas bacterianas para los coágulos sanguíneos
Las infecciones graves causadas por bacterias Gram-negativas pueden empujar al organismo a una espiral peligrosa en la que la sangre comienza a coagularse sin control, bloqueando vasos pequeños y dañando órganos. Este estudio plantea una pregunta aparentemente simple pero de grandes implicaciones: cuando fragmentos de la pared bacteriana entran en el torrente sanguíneo, ¿alteran físicamente a la trombina, la enzima clave que forma los coágulos? Al desvelar cómo interactúan moléculas bacterianas específicas con la trombina, el trabajo arroja luz sobre por qué los problemas de coagulación relacionados con la sepsis varían tanto entre pacientes y podría señalar nuevas vías para predecir o incluso controlar estos eventos potencialmente mortales.
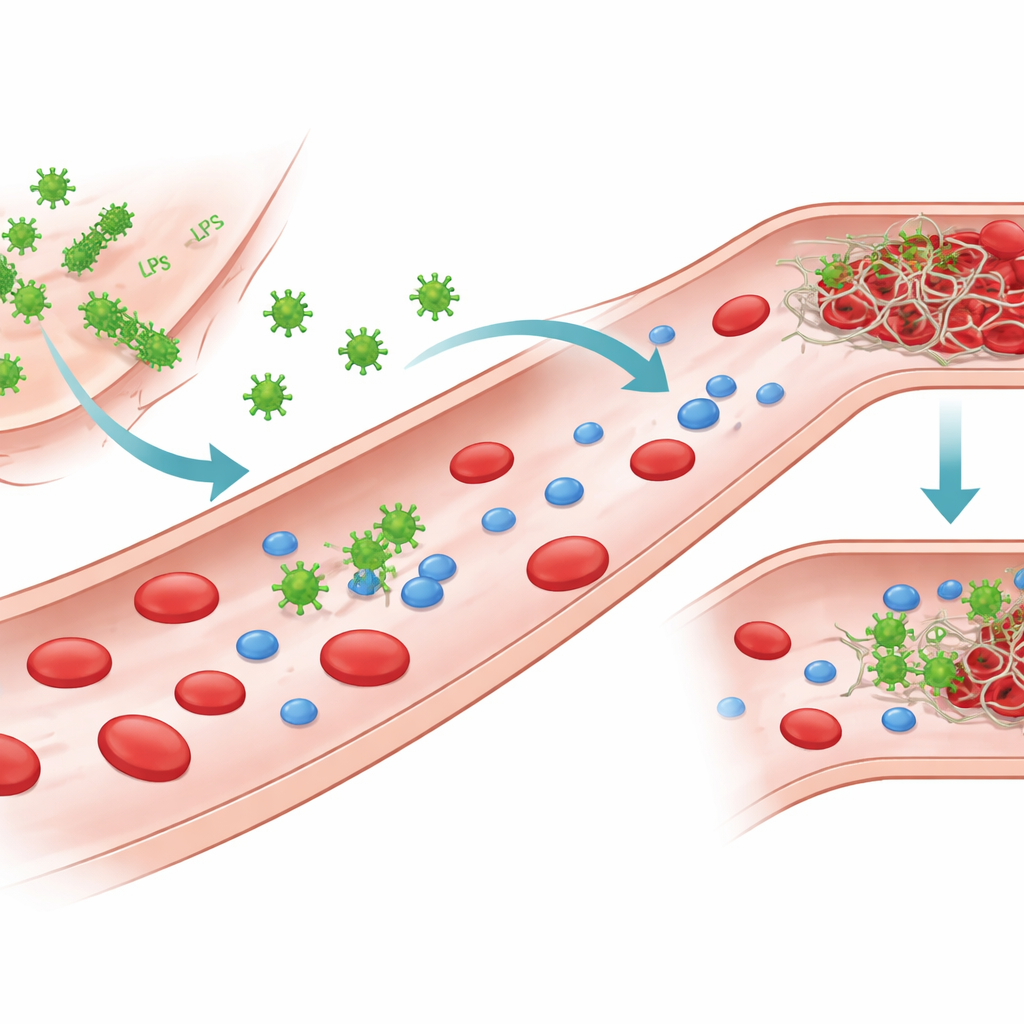
Fragmentos bacterianos que dialogan con la sangre
Las bacterias Gram-negativas portan en su superficie externa una molécula potente llamada lipopolisacárido, o LPS. Cuando las bacterias se dañan o destruyen, el LPS puede liberarse y circular en la sangre. Los autores se centraron en LPS procedente de varios patógenos comunes, incluidas dos cepas de Escherichia coli, así como Klebsiella pneumoniae y Pseudomonas aeruginosa. Aunque todos se basan en el mismo andamiaje fundamental, sus cadenas de azúcares y patrones de carga difieren, creando “quimotipos” distintivos. Estas diferencias estructurales modifican la forma en que el LPS se organiza en agua, formando moléculas individuales, pequeños conglomerados o ensamblajes más extensos en forma de lámina, y también alteran cómo el LPS interactúa con las proteínas en la sangre.
Cómo el LPS se agarra a la enzima de la coagulación
La trombina presenta en su superficie dos parches fuertemente cargados positivamente, llamados exositos, que normalmente la ayudan a reconocer y posicionar socios naturales como el fibrinógeno y cofactors reguladores. Dado que el LPS es muy cargado negativamente, el equipo sospechó que podría adherirse a estas regiones. Usando una combinación de ensayos de unión y medidas sensibles de fluorescencia, demostraron que el LPS de las cuatro bacterias puede, efectivamente, unirse a la trombina. Sin embargo, solo algunos quimotipos —especialmente una cepa de E. coli (O26:B6) y Klebsiella pneumoniae— indujeron cambios estructurales claros en la trombina. Al bloquear cada exosito con sondas cortas basadas en ADN, los investigadores demostraron que el LPS debe engancharse a estos parches cargados para ejercer sus efectos, confirmando que la unión ocurre en las mismas superficies que la trombina usa para su función normal.
Cuando fragmentos bacterianos ralentizan la máquina de coagulación
Para probar si esta unión cambia realmente el rendimiento de la trombina, los autores siguieron la velocidad con que la enzima corta un sustrato modelo pequeño y con qué eficacia convierte el fibrinógeno en una red de fibrina. Encontraron que quimotipos de LPS específicos, especialmente E. coli O26:B6 y Klebsiella pneumoniae, pueden reducir notablemente el poder catalítico de la trombina, a veces más de cien veces. Esta supresión depende no solo del tipo de LPS sino también de cómo se organizan las moléculas de LPS. Cuando el LPS existe como conglomerados más pequeños y curvados, interactúa de forma más íntima con la trombina y la inhibe con fuerza; cuando los iones calcio inducen al LPS a formar agregados mayores y más ordenados, la inhibición se debilita o incluso se pierde para algunos quimotipos. De forma importante, estos mismos patrones se trasladan a la formación del coágulo: ciertas formas de LPS pueden impedir por completo el ensamblaje de la red de fibrina en sistemas purificados, mientras que otras solo ralentizan o incluso aceleran el crecimiento del coágulo.
Diferentes bacterias, distintos resultados de coagulación
La historia se enriquece aún más en el plasma, donde muchas otras proteínas compiten por la atención. En este entorno más realista, los quimotipos de LPS siguen mostrando “huellas” distintas. A bajas concentraciones, varios tipos retrasan el inicio de la coagulación, pero a concentraciones más altas muchos cambian a un comportamiento pro-coagulante, acortando los tiempos de coagulación. Un quimotipo de E. coli, O26:B6, destaca: cuando su LPS se ensambla en agregados estabilizados por calcio, continúa ralentizando la coagulación incluso a altas concentraciones, lo que sugiere que esta cepa bacteriana en particular puede promover una tendencia persistente hacia una formación de coágulos deficiente. En conjunto, el trabajo revela que tanto la química detallada del LPS como su estado de empaquetamiento a mayor escala determinan si la trombina se inhibe, permanece intacta o se impulsa hacia una coagulación más rápida.
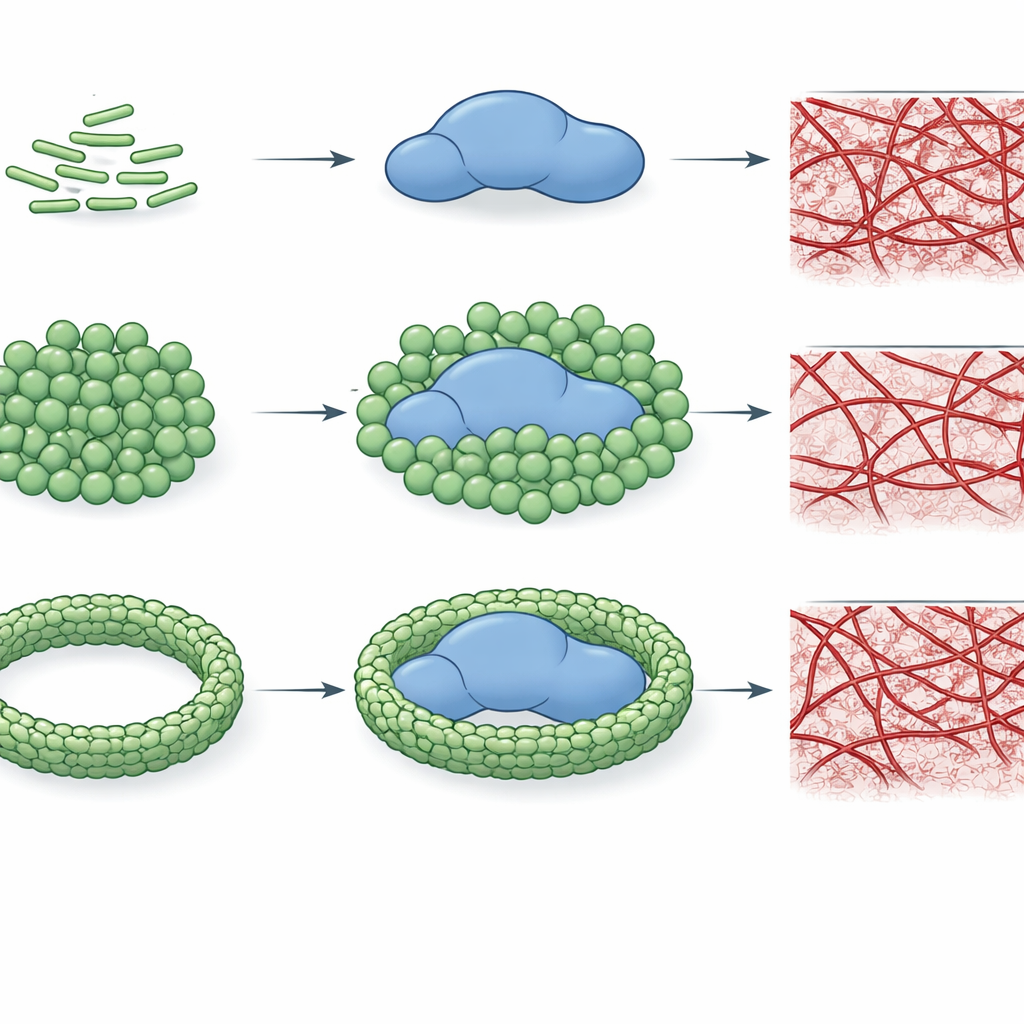
Qué significa esto para la sepsis y la salud sanguínea
Los autores concluyen que el LPS bacteriano no es solo un disparador lejano de la inflamación, sino que puede afinar directamente la actividad de la trombina mediante contacto físico, con efectos que varían según la cepa bacteriana y dependen de cómo se agrupen las moléculas en el torrente sanguíneo. En términos prácticos, esto implica que la misma carga global de infección puede traducirse en patrones de coagulación muy distintos según la mezcla y el estado del LPS presente. Al mapear esta nueva capa de interacción, el estudio ayuda a explicar por qué la sepsis puede causar tanto una coagulación excesiva como una formación de coágulos deficiente, y abre la puerta a terapias que apunten a la unión LPS–trombina o a la organización del LPS para restaurar el equilibrio del sistema de coagulación del organismo.
Cita: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Palabras clave: sepsis, trombina, lipopolisacárido, coagulación sanguínea, bacterias Gram-negativas