Clear Sky Science · ar
الأساس الجزيئي لتثبيط نشاط α-الثرومبين بواسطة الليبوفوسفوليبيدات البكتيرية
لماذا تهم سموم البكتيريا في تجلط الدم
يمكن أن تدفع الإصابات الشديدة الناجمة عن البكتيريا سالبة الغرام الجسم إلى دورة خطيرة حيث يبدأ الدم في التجلط بشكلٍ غير مسيطر عليه، مما يسد الأوعية الدقيقة ويتلف الأعضاء. تثير هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو عواقب كبيرة: عندما تدخل أجزاء من جدران الخلايا البكتيرية مجرى الدم، هل تتداخل مادياً مع الثرومبين، الإنزيم الأساسي المسؤول عن تكوين الجلطات؟ من خلال الكشف عن كيفية تفاعل جزيئات بكتيرية محددة مع الثرومبين، تسلط الدراسة الضوء على سبب اختلاف اضطرابات التجلط المرتبطة بالإنتان بشكل كبير بين المرضى، وقد تشير إلى طرق جديدة للتنبؤ بهذه الأحداث أو التحكم فيها.
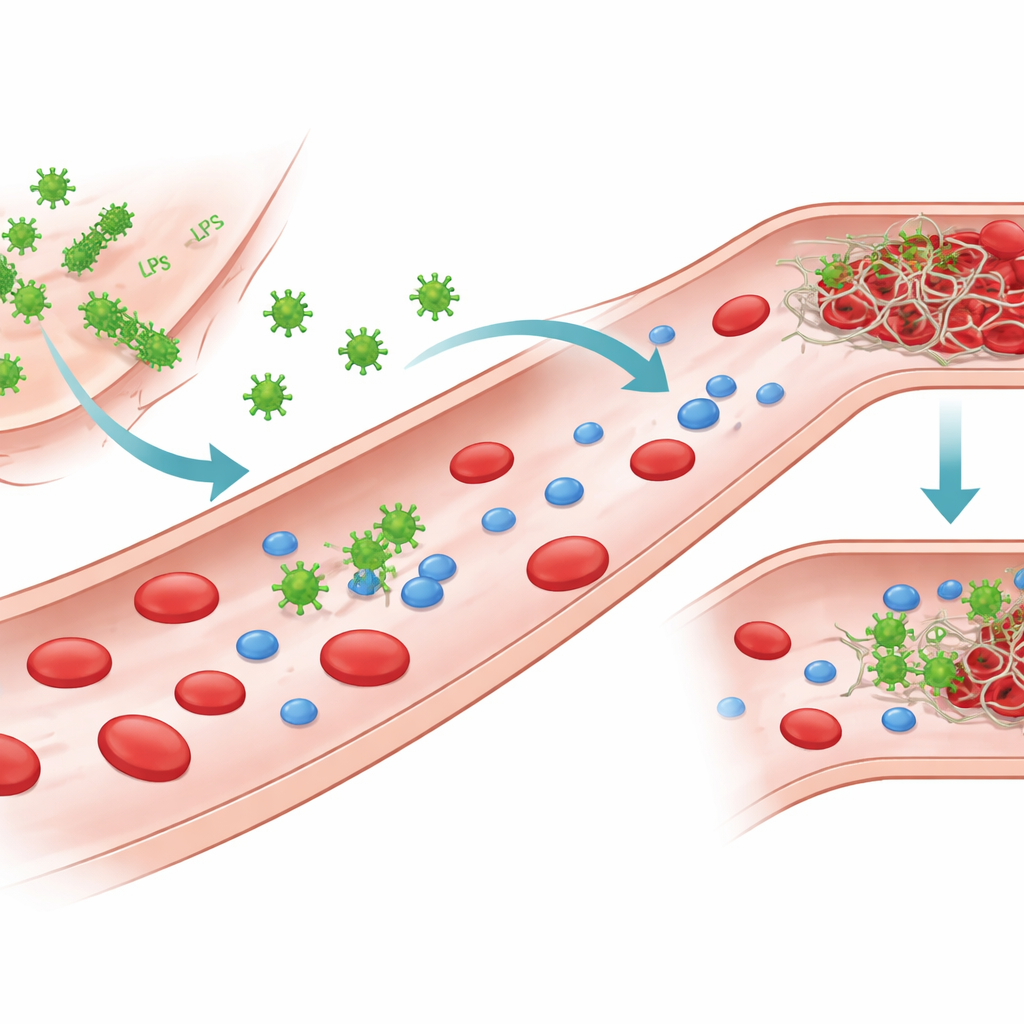
قطع من البكتيريا تتواصل مع الدم
تحمل البكتيريا سالبة الغرام جزيئاً قوياً يسمى الليبوفوسفوليبيد، أو LPS، على سطحها الخارجي. عندما تتعرض البكتيريا للضرر أو التحلل، يمكن أن يتحرر LPS ويجري في الدم. ركز المؤلفون على LPS من عدة مسببات شائعة للأمراض، بما في ذلك سلالتان من الإشريكية القولونية، وكذلك Klebsiella pneumoniae وPseudomonas aeruginosa. على الرغم من أن جميعها مبنية على نفس الهيكل الأساسي، تختلف سلاسلها السكرية وأنماط شحنتها، ما يخلق «أنماطًا كيميائية» مميزة. تغيّر هذه الاختلافات التركيبية كيفية تجمّع LPS في الماء، لتكوّن جزيئات مفردة أو عناقيد صغيرة أو هياكل شبيهة بالألواح، وتغير أيضاً كيفية تفاعل LPS مع البروتينات الموجودة في الدم.
كيف يمسك LPS بإنزيم التجلط
يحمل الثرومبين رقعتين على سطحه شديدة الشحنة الموجبة تُسمى المواضع الخارجية (exosites)، والتي تساعده عادةً على التعرف على شركائه الطبيعيين مثل الفيبرينوجين والعوامل المنظمة. وبما أن LPS مشحون سلبياً بشدة، توقع الفريق أنه قد يرتبط بهذه المناطق. باستخدام مزيج من اختبارات الارتباط وقياسات الفلورسنت الحساسة، أظهروا أن LPS من البكتيريا الأربعة يمكنه بالفعل ربط الثرومبين. ومع ذلك، لم تؤدِ جميع الأنماط الكيميائية إلى تغيّرات بنيوية واضحة في الثرومبين؛ فقد كانت بعض الأنماط — وبشكل بارز سلالة واحدة من الإشريكية القولونية (O26:B6) وKlebsiella pneumoniae — هي التي أحدثت تحوّلات واضحة. من خلال حجب كل موضع خارجي بمسبارات قصيرة قائمة على الحمض النووي، برهن الباحثون أن LPS يجب أن يتفاعل مع هذه البقع المشحونة لممارسة تأثيره، مؤكّدين أن الارتباط يحدث عند نفس السطوح التي يستخدمها الثرومبين في عمله الطبيعي.
عندما تبطئ شظايا البكتيريا آلة التجلط
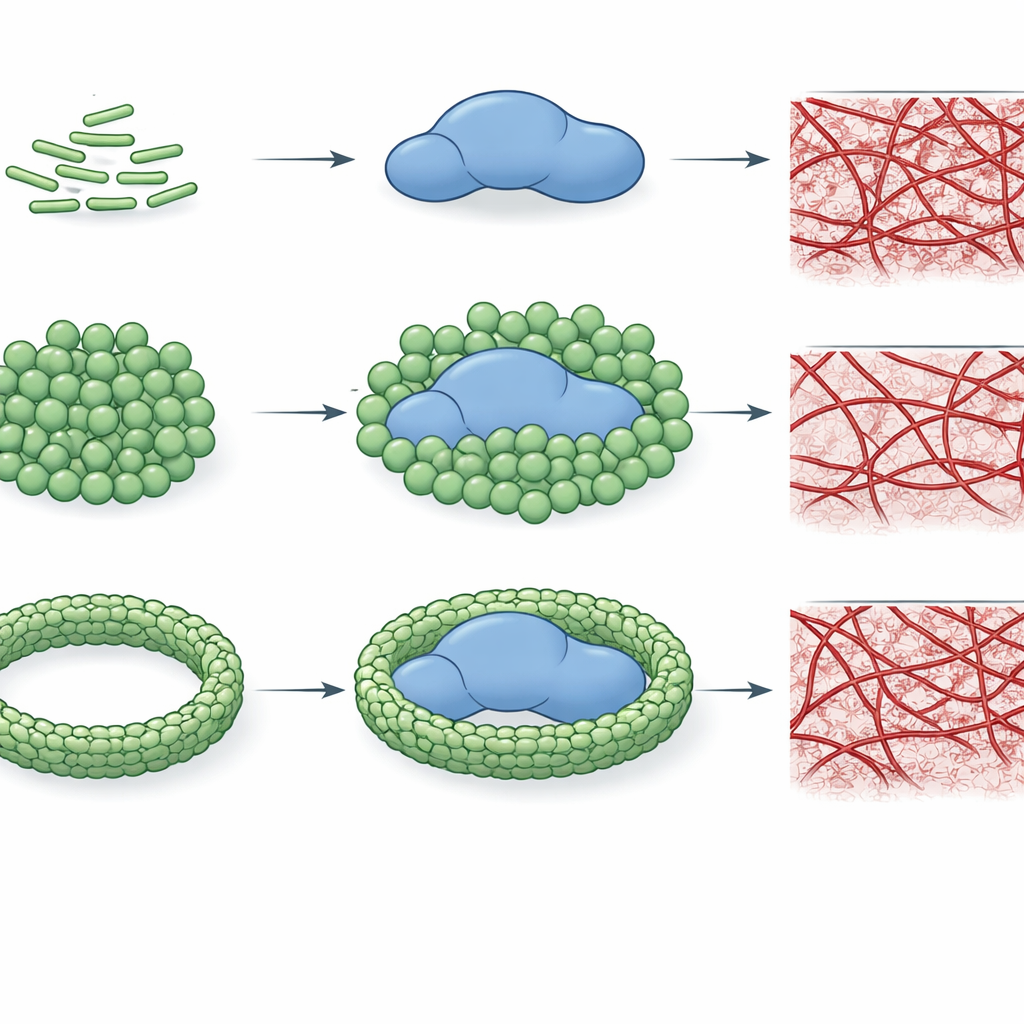
لاختبار ما إذا كان هذا الارتباط يغير فعلاً أداء الثرومبين، تتبع المؤلفون مدى سرعة قطع الإنزيم لرزيم نموذج صغير ومدى كفاءته في تحويل الفيبرينوجين إلى شبكة فيبرين. وجدوا أن أنماط LPS الكيميائية المحددة، لا سيما الإشريكية القولونية O26:B6 وKlebsiella pneumoniae، يمكن أن تقلل بشكل ملحوظ القوة التحفيزية للثرومبين، أحياناً بأكثر من مائة ضعف. لا يعتمد هذا التثبيط فقط على نوع LPS بل أيضاً على كيفية تنظيم جزيئات LPS. عندما يتواجد LPS كعناقيد أصغر وأكثر انحناءً، يتفاعل بصورة أوثق مع الثرومبين ويثبطه بشدة؛ وعندما تدفع أيونات الكالسيوم LPS لتكوين تجمعات أكبر وأكثر انتظاماً، يضعف التثبيط أو يختفي لبعض الأنماط الكيميائية. والأهم أن هذه الأنماط نفسها تنعكس في تشكيل الجلطات: إذ تستطيع بعض أشكال LPS منع تجميع شبكة الفيبيرين تماماً في أنظمة منفصلة من المكونات النقية، بينما تبطئ أشكال أخرى النمو أو حتى تسرّعه.
بكتيريا مختلفة، نتائج تجلط مختلفة
تصبح القصة أكثر ثراءً في البلازما، حيث تتنافس العديد من البروتينات الأخرى على الانتباه. في هذا البيئ الأكثر واقعية، لا تزال الأنماط الكيميائية لـLPS تظهر «بصمات» مميزة. ففي تراكيز منخفضة، تؤخر عدة أنواع بدء التجلط، لكن عند مستويات أعلى يتحول العديد منها إلى سلوك محفز للتجلط، مختصراً أوقات التجلط. تبرز إحدى الأنماط الكيميائية للإشريكية القولونية، O26:B6: عندما يُجمع LPS الخاص بها في تجمعات مستقرة بالكالسيوم، يواصل إبطاء التجلط حتى عند تراكيز عالية، مما يشير إلى أن هذه السلالة البكتيرية قد تعزز ميلًا مستمراً نحو ضعف تكوّن الجلطات. عموماً، تكشف الدراسة أن كل من الكيمياء التفصيلية للـLPS وحالته على مقياس أكبر تحددان ما إذا كان الثرومبين سيُثبَّط أو يظل غير متأثر أو يُدفع نحو تشكيل جلطات أسرع.
ما يعنيه هذا بالنسبة للإنتان وصحة الدم
يخلص المؤلفون إلى أن LPS البكتيري ليس مجرد مُثير بعيد للالتهاب، بل يمكنه ضبط نشاط الثرومبين مباشرة عبر تلامس فيزيائي، مع تأثيرات تختلف من سلالة بكتيرية إلى أخرى وتعتمد على كيفية تجمع الجزيئات في مجرى الدم. عملياً، يعني هذا أن نفس حمل العدوى الكلي قد يؤدي إلى أنماط تجلط مختلفة تماماً حسب مزيج وحالة LPS الموجود. من خلال رسم خريطة لهذه الطبقة الجديدة من التفاعل، تساعد الدراسة في تفسير لماذا يمكن أن يسبب الإنتان كلتا الحالتين — التجمع الزائد للجلطات وضعف تكوين الجلطات — وتفتح الباب أمام علاجات تستهدف ارتباط LPS بالثرومبين أو تنظيم تجمّع LPS نفسه لاستعادة التوازن في نظام تجلط الجسم.
الاستشهاد: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
الكلمات المفتاحية: الإنتان, الثرومبين, الليبوفوسفوليبيد, تجلط الدم, البكتيريا سالبة الغرام