Clear Sky Science · pt
Base molecular para a inibição da atividade da α-trombina por lipopolissacarídeos bacterianos
Por que as toxinas bacterianas importam para coágulos sanguíneos
Infecções graves por bactérias Gram-negativas podem arrastar o corpo para uma espiral perigosa em que o sangue começa a coagular de forma descontrolada, bloqueando pequenos vasos e danificando órgãos. Este estudo faz uma pergunta aparentemente simples, com grandes implicações: quando fragmentos da parede celular bacteriana entram na corrente sanguínea, eles interferem fisicamente na trombina, a enzima-chave que forma coágulos? Ao revelar como moléculas bacterianas específicas interagem com a trombina, o trabalho esclarece por que os problemas de coagulação relacionados à sepse variam tanto entre pacientes e pode apontar para novas maneiras de prever ou mesmo controlar esses eventos potencialmente fatais.
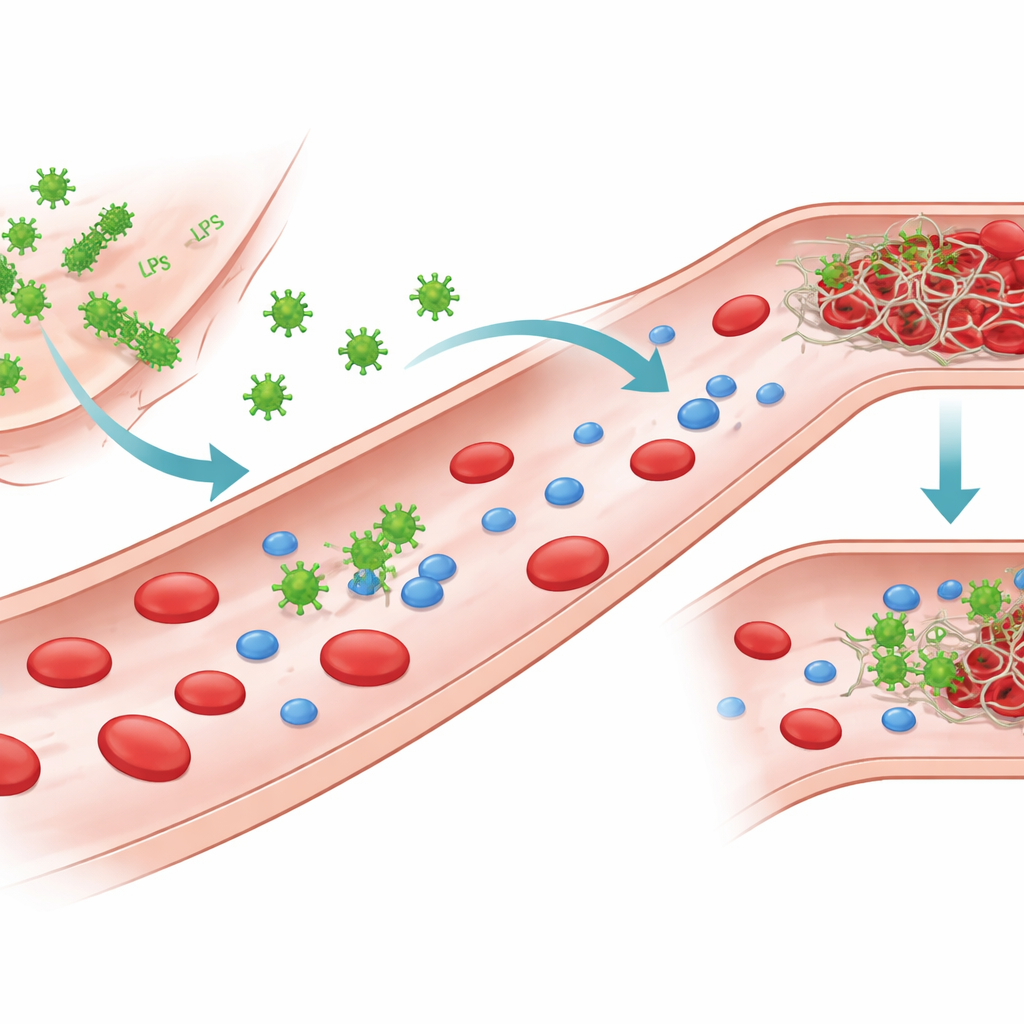
Pedaços de bactérias que conversam com o sangue
Bactérias Gram-negativas exibem na superfície externa uma molécula potente chamada lipopolissacarídeo, ou LPS. Quando as bactérias são danificadas ou destruídas, o LPS pode se soltar e circular no sangue. Os autores se concentraram no LPS de vários patógenos comuns, incluindo duas cepas de Escherichia coli, além de Klebsiella pneumoniae e Pseudomonas aeruginosa. Embora todos compartilhem a mesma estrutura básica, suas cadeias de açúcar e padrões de carga diferem, criando “quimotipos” distintos. Essas diferenças estruturais alteram como o LPS se organiza na água, formando moléculas isoladas, pequenos aglomerados ou montagens em folhas maiores, e também modificam como o LPS interage com proteínas no sangue.
Como o LPS se agarra à enzima da coagulação
A trombina apresenta duas regiões fortemente carregadas positivamente em sua superfície, chamadas exossítios, que normalmente a ajudam a reconhecer e posicionar parceiros naturais como a fibrinogênio e cofatores reguladores. Como o LPS é altamente carregado negativamente, a equipe suspeitou que ele poderia se ligar a essas regiões. Usando uma combinação de ensaios de ligação e medidas de fluorescência sensíveis, demonstraram que o LPS de todas as quatro bactérias pode, de fato, se ligar à trombina. No entanto, apenas alguns quimotipos — notadamente uma cepa de E. coli (O26:B6) e Klebsiella pneumoniae — induziram mudanças estruturais claras na trombina. Ao bloquear cada exossítio com sondas curtas baseadas em DNA, os pesquisadores mostraram que o LPS precisa envolver essas áreas carregadas para exercer seus efeitos, confirmando que a ligação ocorre nas mesmas superfícies que a trombina usa para seu funcionamento normal.
Quando fragmentos bacterianos desaceleram a máquina de coagulação
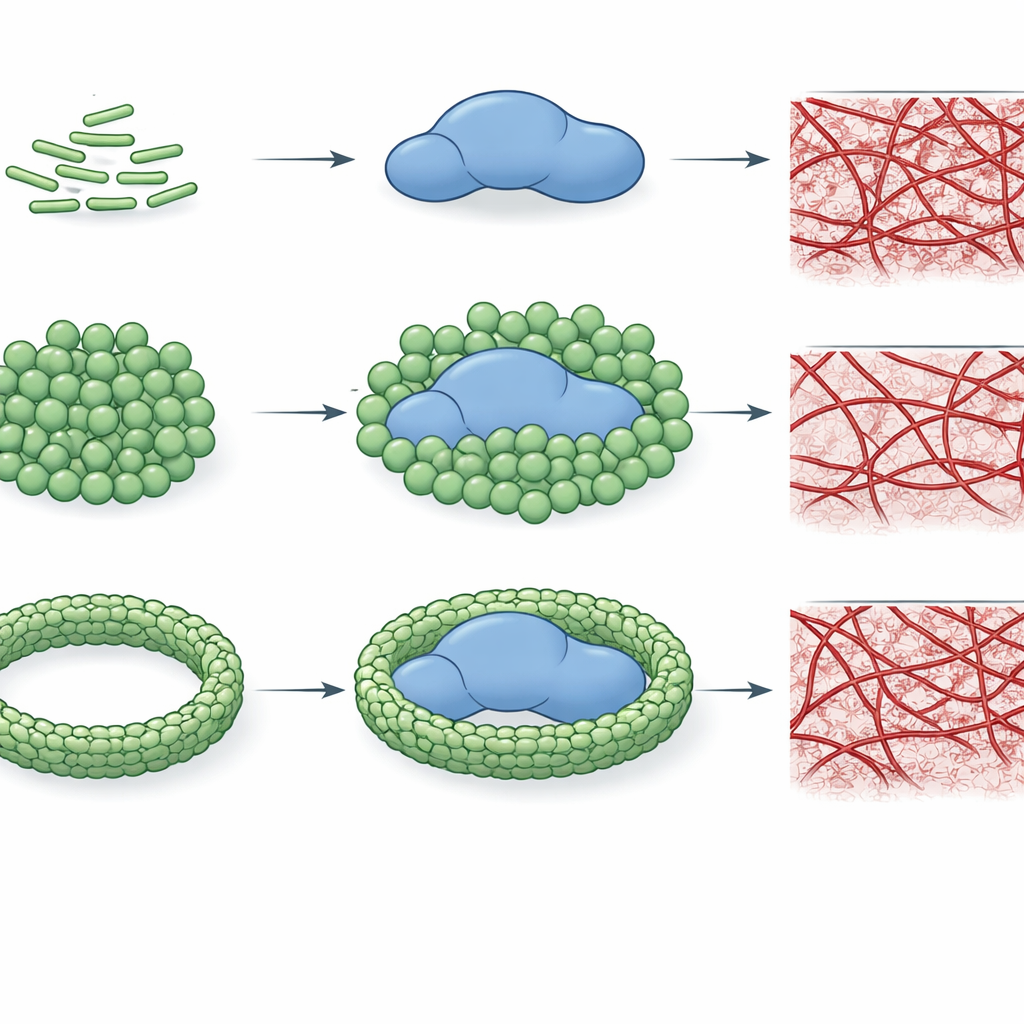
Para testar se essa ligação realmente altera o desempenho da trombina, os autores acompanharam com que rapidez a enzima cliva um pequeno substrato modelo e quão eficientemente converte fibrinogênio em uma rede de fibrina. Descobriram que quimotipos específicos de LPS, especialmente E. coli O26:B6 e Klebsiella pneumoniae, podem reduzir marcadamente o poder catalítico da trombina, às vezes em mais de cem vezes. Essa supressão depende não apenas do tipo de LPS, mas também de como as moléculas de LPS estão organizadas. Quando o LPS existe como aglomerados menores e mais curvos, interage de forma mais íntima com a trombina e a inibe fortemente; quando íons cálcio promovem a formação de agregados maiores e mais ordenados, a inibição diminui ou até desaparece para alguns quimotipos. Importante, esses mesmos padrões se refletem na formação de coágulos: certas formas de LPS podem impedir completamente a montagem da rede de fibrina em sistemas purificados, enquanto outras apenas retardam ou até aceleram o crescimento do coágulo.
Bactérias diferentes, desfechos de coagulação diferentes
A história fica ainda mais complexa no plasma, onde muitas outras proteínas competem por atenção. Nesse ambiente mais realista, os quimotipos de LPS ainda mostram “impressões digitais” distintas. Em concentrações baixas, vários tipos atrasam o início da coagulação, mas em níveis mais altos muitos mudam para um comportamento pró-coagulação, encurtando os tempos de coagulação. Um quimotipo de E. coli, O26:B6, destaca-se: quando seu LPS está montado em agregados estabilizados por cálcio, ele continua a retardar a coagulação mesmo em concentrações elevadas, sugerindo que essa cepa bacteriana particular pode promover uma tendência persistente à formação de coágulos prejudicada. No conjunto, o trabalho revela que tanto a química detalhada do LPS quanto seu estado de empacotamento em escala maior determinam se a trombina é inibida, permanece inalterada ou é empurrada para uma coagulação mais rápida.
O que isso significa para a sepse e a saúde do sangue
Os autores concluem que o LPS bacteriano não é apenas um gatilho distante da inflamação, mas pode ajustar diretamente a atividade da trombina por contato físico, com efeitos que variam entre cepas bacterianas e dependem de como as moléculas se agregam na corrente sanguínea. Em termos práticos, isso significa que a mesma carga geral de infecção pode levar a padrões de coagulação muito diferentes dependendo da mistura e do estado do LPS presente. Ao mapear essa nova camada de interação, o estudo ajuda a explicar por que a sepse pode causar tanto coagulação excessiva quanto formação de coágulos prejudicada, e abre caminho para terapias que visem a ligação LPS–trombina ou a própria organização do LPS para restaurar o equilíbrio do sistema de coagulação do corpo.
Citação: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Palavras-chave: sepse, trombina, lipopolissacarídeo, coagulação sanguínea, bactérias Gram-negativas