Clear Sky Science · nl
Moleculaire basis voor remming van α-thrombine-activiteit door bacteriële lipopolysacchariden
Waarom bacteriële toxines van belang zijn voor bloedstolsels
Ernstige infecties veroorzaakt door Gram-negatieve bacteriën kunnen het lichaam in een gevaarlijke spiraal duwen waarin het bloed ongecontroleerd gaat stollen, kleine vaten blokkeert en organen beschadigt. Deze studie stelt een deceptief eenvoudige vraag met grote implicaties: wanneer fragmenten van bacteriële celwanden in de bloedbaan terechtkomen, tasten ze dan fysiek thrombine aan, het sleutelenzym dat bloedstolsels vormt? Door te onthullen hoe specifieke bacteriële moleculen met thrombine interageren, werpt het werk licht op waarom bij sepsis de stollingsproblemen zo sterk kunnen variëren tussen patiënten en kan het wijzen op nieuwe manieren om deze levensbedreigende gebeurtenissen te voorspellen of zelfs te beheersen.
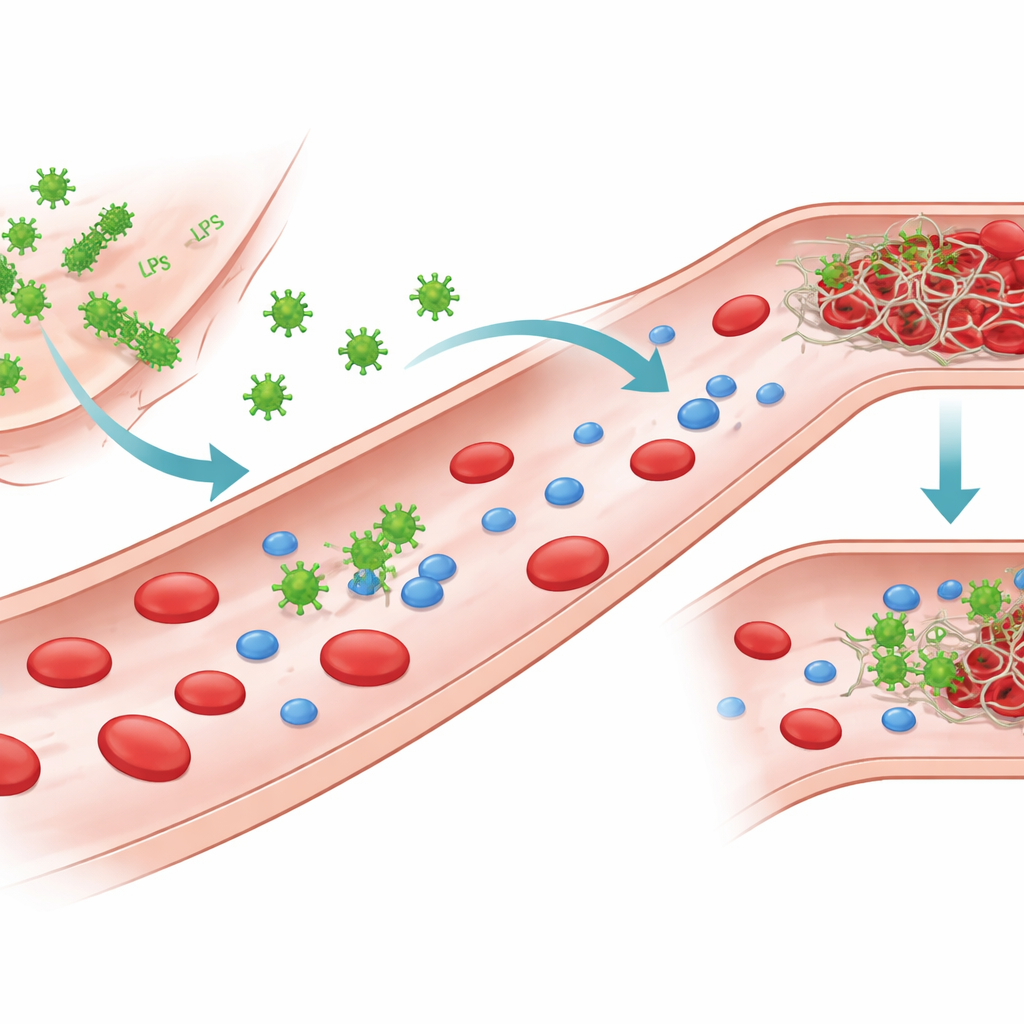
Fragmenten van bacteriën die met bloed communiceren
Gram-negatieve bacteriën dragen een krachtige molecule op hun buitenzijde die lipopolysaccharide (LPS) wordt genoemd. Wanneer bacteriën beschadigd raken of worden vernietigd, kan LPS loskomen en in het bloed circuleren. De auteurs concentreerden zich op LPS uit meerdere veelvoorkomende ziekteverwekkers, waaronder twee stammen van Escherichia coli, evenals Klebsiella pneumoniae en Pseudomonas aeruginosa. Hoewel ze allemaal zijn opgebouwd op hetzelfde basisraamwerk, verschillen hun suikerketens en ladingspatronen, waardoor er verschillende „chemotypes” ontstaan. Deze structurele verschillen veranderen hoe LPS zich in water verpakt: als individuele moleculen, kleine clusters of grotere plaatachtige assemblages, en ze beïnvloeden ook hoe LPS met eiwitten in het bloed omgaat.
Hoe LPS zich vastgrijpt aan het stollingsenzym
Thrombine heeft twee sterk positief geladen vlakken op zijn oppervlak, exosites genoemd, die normaal helpen bij het herkennen en positioneren van natuurlijke partners zoals fibrinogeen en regulerende cofactoren. Omdat LPS sterk negatief geladen is, vermoedde het team dat het zich aan deze regio’s kan hechten. Met een combinatie van bindingsassays en gevoelige fluorescentiemetingen toonden ze aan dat LPS van alle vier de bacteriën inderdaad aan thrombine kan binden. Echter, slechts sommige chemotypes — met name één stam van E. coli (O26:B6) en Klebsiella pneumoniae — veroorzaakten duidelijke structurele verschuivingen in thrombine. Door elk exosite te blokkeren met korte DNA-gebaseerde probes lieten de onderzoekers zien dat LPS deze geladen vlakken moet betrekken om zijn effecten uit te oefenen, wat bevestigt dat de binding plaatsvindt op dezelfde oppervlakken die thrombine voor zijn normale functie gebruikt.
Wanneer bacteriële fragmenten het stollingsapparaat vertragen
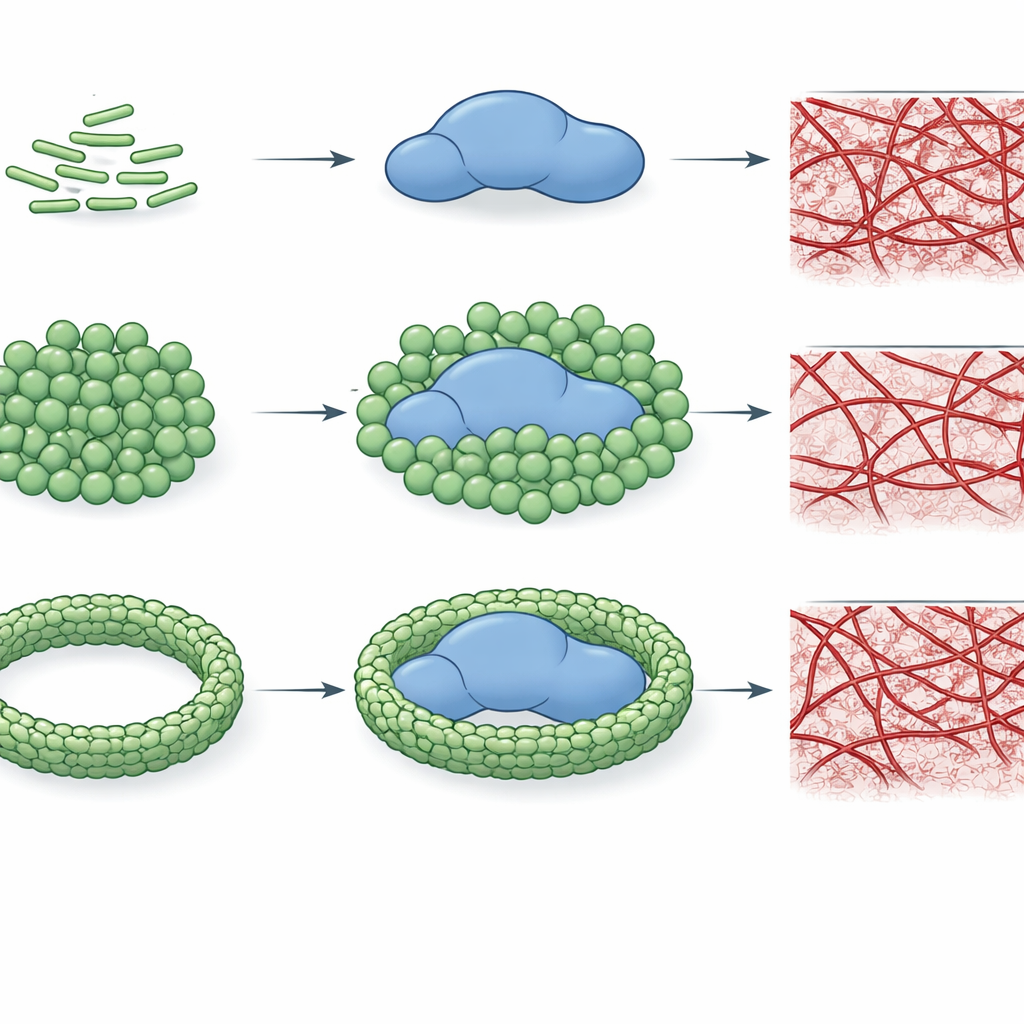
Om te testen of deze binding daadwerkelijk de prestaties van thrombine verandert, volgden de auteurs hoe snel het enzym een klein modelsubstraat knipt en hoe efficiënt het fibrinogeen omzet in een fibrinenetwerk. Ze ontdekten dat specifieke LPS-chemotypes, vooral E. coli O26:B6 en Klebsiella pneumoniae, de katalytische kracht van thrombine aanzienlijk kunnen verminderen, soms meer dan honderdvoudig. Deze remming hangt niet alleen af van het type LPS maar ook van hoe de LPS-moleculen georganiseerd zijn. Wanneer LPS voorkomt als kleinere, sterker gekromde clusters, gaat het intenser met thrombine interageren en remt het krachtig; wanneer calciumionen LPS in grotere, meer geordende aggregaten doen samenklonteren, wordt de remming verzwakt of verdwijnt zelfs voor sommige chemotypes. Belangrijk is dat dezelfde patronen ook terugkomen bij stolingsvorming: bepaalde LPS-vormen kunnen de assemblage van het fibrinenetwerk volledig verhinderen in gezuiverde systemen, terwijl andere slechts de klontering vertragen of zelfs de klontering versnellen.
Verschillende bacteriën, verschillende stollingsuitkomsten
Het verhaal wordt nog complexer in plasma, waar vele andere eiwitten om aandacht concurreren. In deze realistischer omgeving tonen LPS-chemotypes nog steeds onderscheidende “vingerafdrukken”. Bij lage concentraties vertragen meerdere types het begin van stolling, maar bij hogere concentraties schakelen veel over naar een pro-stollend gedrag en verkorten ze de stollingstijden. Eén E. coli-chemotype, O26:B6, valt op: wanneer zijn LPS is geassembleerd tot calcium-gestabiliseerde aggregaten, blijft het zelfs bij hoge concentraties de stolling vertragen, wat suggereert dat deze specifieke bacteriestam een aanhoudende neiging tot verminderde stolingsvorming kan bevorderen. Over het geheel genomen laat het werk zien dat zowel de fijnchemie van LPS als de grootschalige verpakkingsstaat bepalen of thrombine wordt geremd, onaangetast blijft of wordt aangespoord tot snellere stolingsvorming.
Wat dit betekent voor sepsis en bloedgezondheid
De auteurs concluderen dat bacterieel LPS niet alleen een afstandelijke trigger van ontsteking is, maar thrombine-activiteit door fysiek contact direct kan afstemmen, met effecten die variëren tussen bacteriestammen en afhankelijk zijn van hoe de moleculen in de bloedbaan clusteren. In praktische termen betekent dit dat dezelfde totale infectielast zeer verschillende stollingspatronen kan opleveren, afhankelijk van de samenstelling en de toestand van het aanwezige LPS. Door deze nieuwe laag van interactie in kaart te brengen, helpt de studie verklaren waarom sepsis zowel overdreven stolling als verminderde stolingsvorming kan veroorzaken, en opent ze de deur naar therapieën die LPS–thrombine-binding of de organisatie van LPS zelf richten om het evenwicht in het stolingssysteem van het lichaam te herstellen.
Bronvermelding: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Trefwoorden: sepsis, thrombine, lipopolysaccharide, bloedstolling, Gram-negatieve bacteriën