Clear Sky Science · ru
Молекулярная основа ингибирования активности α-тромбина бактериальными липополисахаридами
Почему бактериальные токсины важны для свертывания крови
Тяжёлые инфекции, вызванные грам-отрицательными бактериями, могут запустить опасную спираль: кровь начинает бесконтрольно свёртываться, закупоривая мелкие сосуды и повреждая органы. В этом исследовании задаётся на первый взгляд простой, но важный вопрос: когда фрагменты бактериальной клеточной стенки попадают в кровоток, вмешиваются ли они физически в работу тромбина — ключевого фермента, формирующего сгустки? Раскрывая, как конкретные бактериальные молекулы взаимодействуют с тромбином, работа проясняет, почему при сепсисе нарушения свертывания крови так сильно различаются у разных пациентов, и может указать путь к новым способам предсказания или контроля этих опасных состояний.
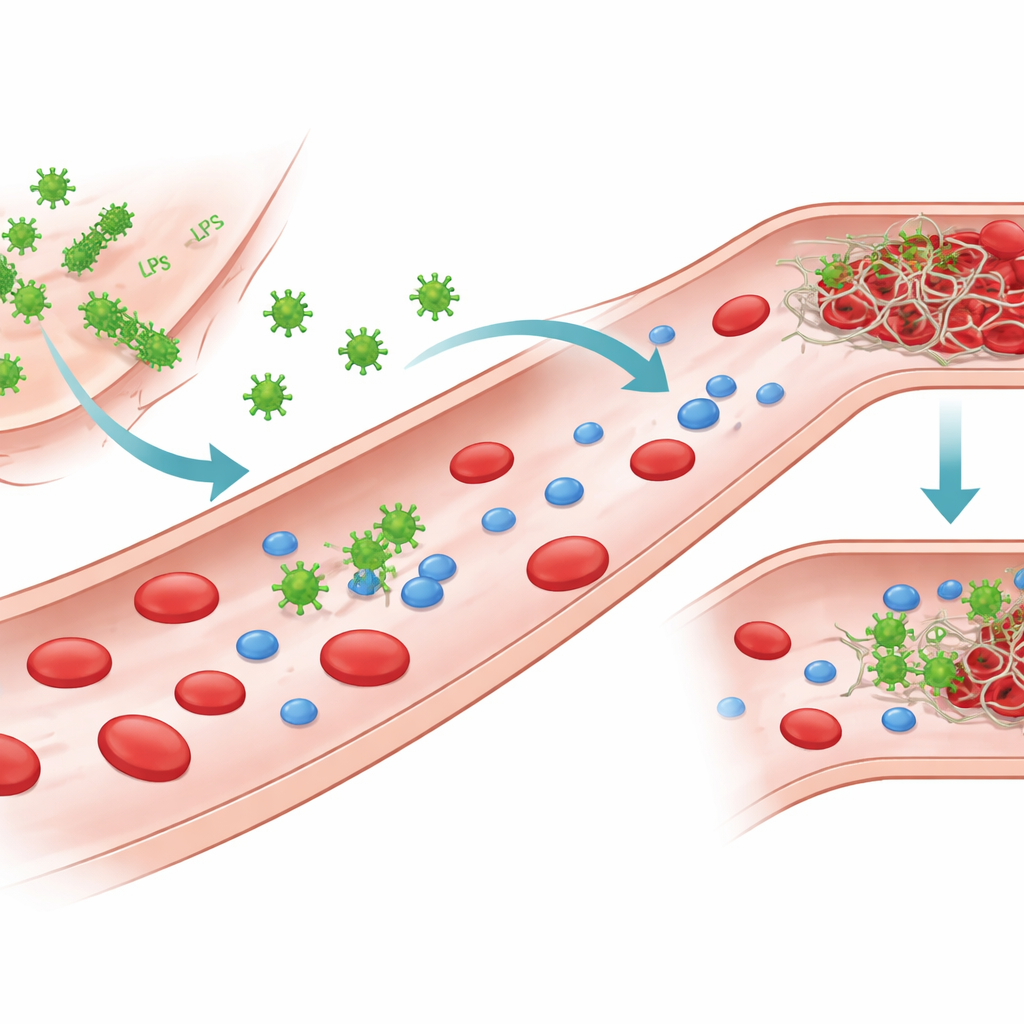
Фрагменты бактерий, которые «разговаривают» с кровью
У грам-отрицательных бактерий на внешней поверхности присутствует мощная молекула — липополисахарид, или ЛПС. Когда бактерии повреждаются или разрушаются, ЛПС может освобождаться и циркулировать в крови. Авторы сосредоточились на ЛПС нескольких распространённых патогенов, включая два штамма Escherichia coli, а также Klebsiella pneumoniae и Pseudomonas aeruginosa. Хотя все они построены на одном и том же базовом каркасе, их сахарные цепи и распределение зарядов различаются, образуя разные «хемотипы». Эти структурные различия меняют то, как ЛПС упаковывается в воде — формируя отдельные молекулы, мелкие кластеры или большие листообразные структуры — и также влияют на взаимодействие ЛПС с белками в крови.
Как ЛПС хватается за фермент свертывания
Тромбин имеет на своей поверхности два сильно положительно заряженных участка, называемых экзосайтами, которые обычно помогают ему распознавать и правильно позиционировать естественные партнёры, такие как фибриноген и регуляторные кофакторы. Поскольку ЛПС сильно негативно заряжен, исследователи предположили, что он может прицепляться к этим участкам. С помощью сочетания связывающих анализов и чувствительных флуоресцентных измерений они показали, что ЛПС всех четырёх бактерий действительно может связываться с тромбином. Однако лишь некоторые хемотипы — в частности один штамм E. coli (O26:B6) и Klebsiella pneumoniae — вызывали заметные структурные сдвиги в тромбине. Блокируя каждый экзосайт короткими ДНК-зондами, исследователи продемонстрировали, что ЛПС должен задействовать эти заряженные участки, чтобы оказывать своё влияние, подтвердив, что связывание происходит на тех же поверхностях, которые тромбин использует для своей обычной работы.
Когда бактериальные фрагменты замедляют «механизм» свертывания
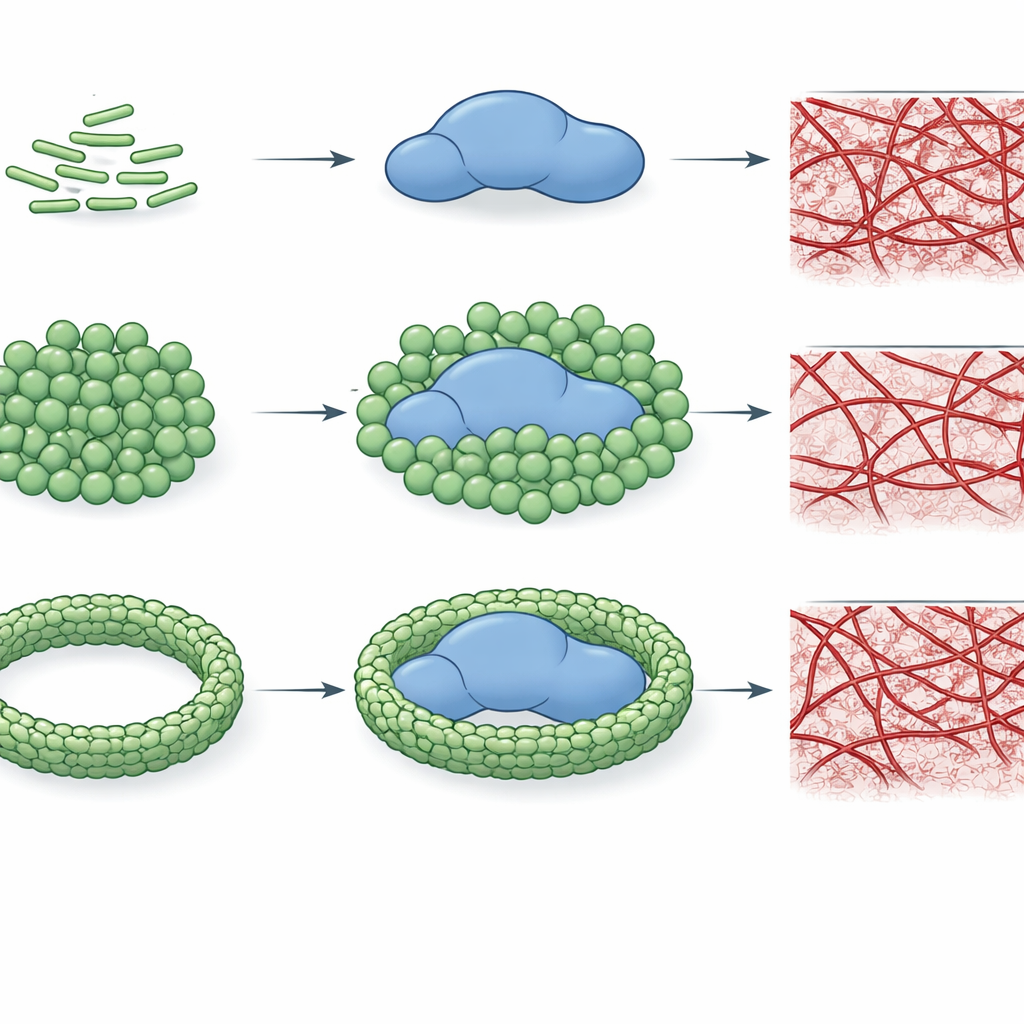
Чтобы проверить, действительно ли это связывание меняет работу тромбина, авторы отслеживали, как быстро фермент расщепляет небольшой модельный субстрат и насколько эффективно он превращает фибриноген в фибриновую сеть. Они обнаружили, что отдельные хемотипы ЛПС, особенно E. coli O26:B6 и Klebsiella pneumoniae, могут существенно снижать каталитическую активность тромбина, иногда более чем в сто раз. Это подавление зависит не только от типа ЛПС, но и от того, как сами молекулы ЛПС организованы. Когда ЛПС существует в виде меньших, более изогнутых кластеров, он теснее взаимодействует с тромбином и сильно ингибирует его; когда ионы кальция приводят ЛПС к образованию больших, более упорядоченных агрегатов, ингибирование ослабевает или даже исчезает для некоторых хемотипов. Важно, что эти же закономерности проявляются и при формировании сгустка: определённые формы ЛПС полностью препятствуют сборке фибриновой сети в очищённых системах, тогда как другие лишь замедляют или даже ускоряют рост сгустка.
Разные бактерии — разные исходы свертывания
Картина становится ещё сложнее в плазме, где многие другие белки конкурируют за внимание. В этой более реалистичной среде хемотипы ЛПС по-прежнему имеют отличительные «отпечатки». При низких концентрациях несколько типов задерживают начало свертывания, но при более высоких уровнях многие переключаются на про-свертывающее поведение, сокращая времена свертывания. Один хемотип E. coli, O26:B6, выделяется: когда его ЛПС сформировано в кальцием стабилизированные агрегаты, оно продолжает замедлять свертывание даже при высоких концентрациях, что указывает на то, что этот конкретный штамм бактерий может способствовать устойчивой склонности к нарушению формирования сгустков. В целом работа показывает, что и детальная химия ЛПС, и его упаковка в масштабе определяют, будет ли тромбин ингибирован, останется ли нетронутым или будет сдвинут в сторону ускоренного образования сгустков.
Что это значит для сепсиса и здоровья крови
Авторы приходят к выводу, что бактериальный ЛПС — это не просто отдалённый триггер воспаления, но и молекула, способная напрямую регулировать активность тромбина через физический контакт, при этом эффекты различаются в зависимости от штамма бактерии и от того, как молекулы ЛПС агрегируются в кровотоке. На практике это означает, что одна и та же степень заражения может приводить к очень разным паттернам свертывания в зависимости от состава и состояния присутствующего ЛПС. Нанёсив новую карту этих взаимодействий, исследование помогает объяснить, почему при сепсисе могут наблюдаться как чрезмерное свертывание, так и нарушенное формирование сгустков, и открывает путь к терапиям, нацеленным на связывание ЛПС с тромбином или на организацию самих молекул ЛПС, чтобы восстановить баланс в системе свертывания.»
Цитирование: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Ключевые слова: сепсис, тромбин, липополисахарид, свертывание крови, грам-отрицательные бактерии