Clear Sky Science · it
Base molecolare dell’inibizione dell’attività di α-trombina da parte dei lipopolisaccaridi batterici
Perché le tossine batteriche contano per i coaguli del sangue
Le infezioni gravi causate da batteri Gram-negativi possono trascinare l’organismo in una spirale pericolosa in cui il sangue comincia a coagulare in modo incontrollato, ostruendo i piccoli vasi e danneggiando gli organi. Questo studio pone una domanda apparentemente semplice ma di grande portata: quando frammenti della parete batterica entrano nel circolo sanguigno, interferiscono fisicamente con la trombina, l’enzima chiave che forma i coaguli? Facendo luce su come specifiche molecole batteriche interagiscono con la trombina, il lavoro spiega perché i problemi di coagulazione correlati alla sepsi variano così tanto tra i pazienti e potrebbe indicare modi nuovi per prevedere o addirittura controllare questi eventi potenzialmente letali.
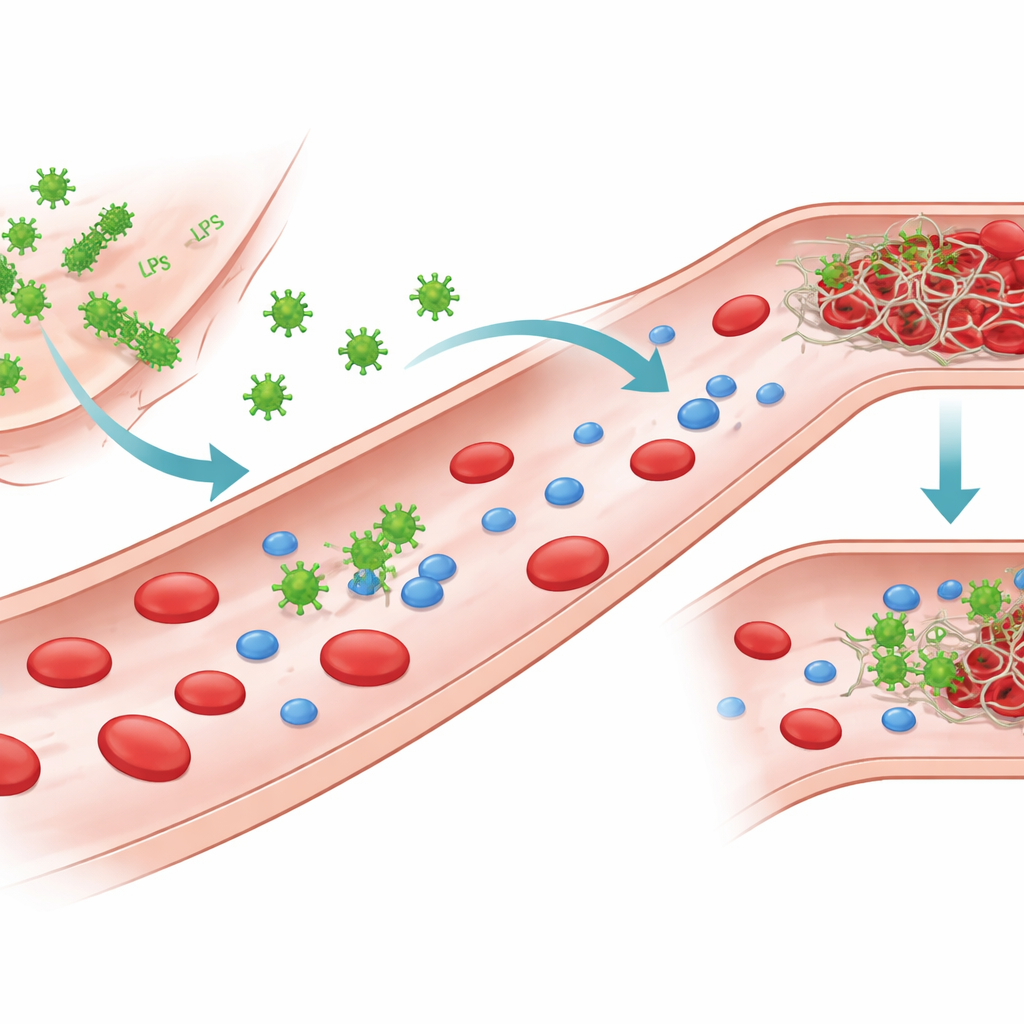
Frammenti di batteri che dialogano con il sangue
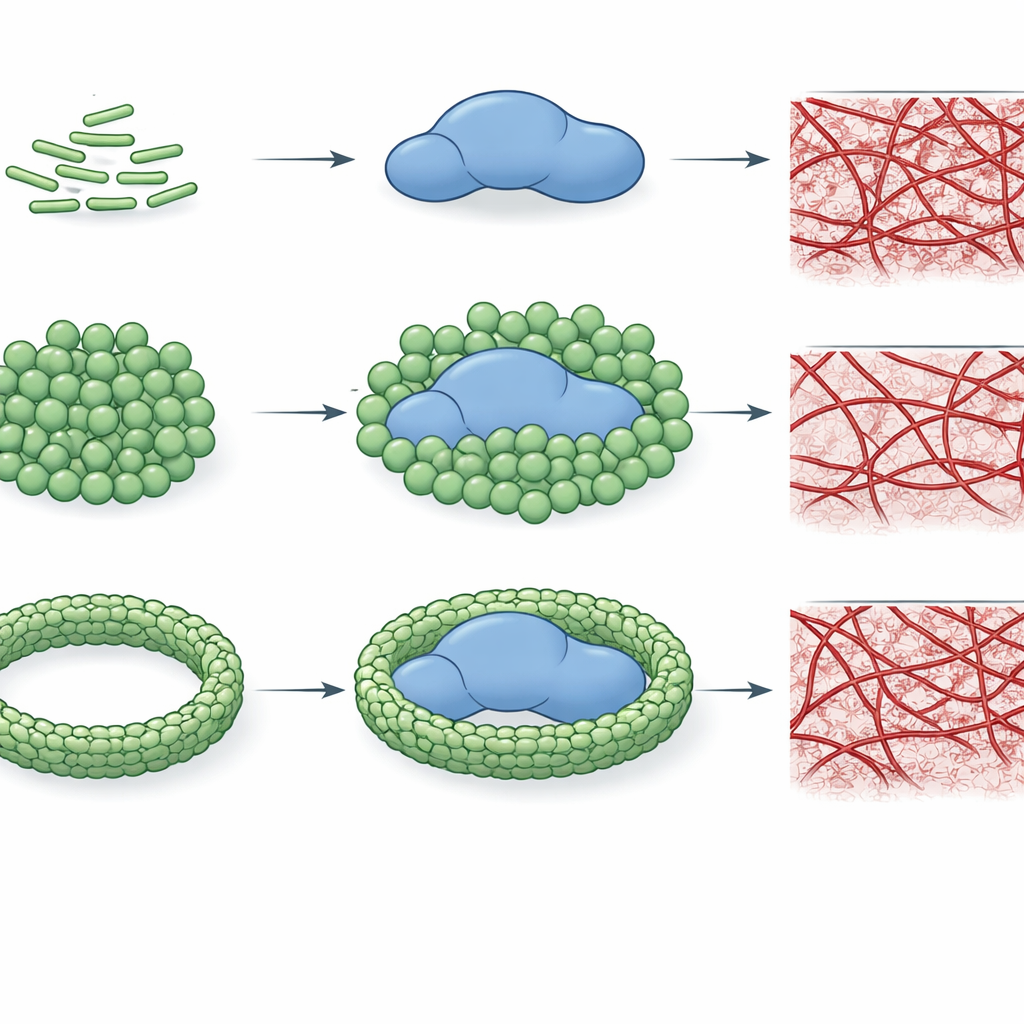
I batteri Gram-negativi portano sulla loro superficie esterna una molecola potente chiamata lipopolisaccaride, o LPS. Quando i batteri sono danneggiati o distrutti, l’LPS può staccarsi e circolare nel sangue. Gli autori si sono concentrati sull’LPS di diversi patogeni comuni, incluse due ceppi di Escherichia coli, oltre a Klebsiella pneumoniae e Pseudomonas aeruginosa. Pur basandosi sullo stesso impianto strutturale di base, le loro catene di zuccheri e i modelli di carica differiscono, creando distinti “chemiotipi”. Queste differenze strutturali modificano il modo in cui l’LPS si aggrega in acqua, formando singole molecole, piccoli ammassi o assemblaggi a foglio più ampi, e alterano anche come l’LPS interagisce con le proteine nel sangue.
Come l’LPS afferra l’enzima della coagulazione
La trombina presenta due aree fortemente caricate positivamente sulla sua superficie, chiamate esositi, che normalmente la aiutano a riconoscere e posizionare partner naturali come il fibrinogeno e cofattori regolatori. Poiché l’LPS è altamente carico negativamente, il gruppo sospettava che potesse agganciarsi a queste regioni. Usando una combinazione di saggi di legame e misure di fluorescenza sensibili, hanno dimostrato che l’LPS di tutti e quattro i batteri può effettivamente legarsi alla trombina. Tuttavia, solo alcuni chemiotipi — in particolare un ceppo di E. coli (O26:B6) e Klebsiella pneumoniae — hanno indotto evidenti spostamenti strutturali nella trombina. Bloccando ciascun esosito con sonde corte a base di DNA, i ricercatori hanno mostrato che l’LPS deve impegnare queste superfici cariche per esercitare i suoi effetti, confermando che il legame avviene sugli stessi siti che la trombina usa per svolgere la sua funzione normale.
Quando i frammenti batterici rallentano la macchina della coagulazione
Per verificare se questo legame modifica davvero le prestazioni della trombina, gli autori hanno monitorato la velocità con cui l’enzima taglia un piccolo substrato modello e quanto efficacemente converte il fibrinogeno in una rete di fibrina. Hanno scoperto che specifici chemiotipi di LPS, in particolare E. coli O26:B6 e Klebsiella pneumoniae, possono ridurre notevolmente il potere catalitico della trombina, talvolta di oltre cento volte. Questa soppressione dipende non solo dal tipo di LPS ma anche da come le molecole di LPS sono organizzate. Quando l’LPS esiste come ammassi più piccoli e più curvi, interagisce in modo più intimo con la trombina e la inibisce fortemente; quando gli ioni calcio inducono l’LPS ad aggregarsi in strutture più grandi e ordinate, l’inibizione si indebolisce o viene persino persa per alcuni chemiotipi. È importante che questi stessi schemi si riflettano nella formazione del coagulo: alcune forme di LPS possono impedire completamente l’assemblaggio della rete di fibrina in sistemi purificati, mentre altre rallentano o addirittura accelerano la crescita del coagulo.
Batteri diversi, esiti di coagulazione diversi
La storia diventa ancora più complessa nel plasma, dove molte altre proteine competono per interagire. In questo ambiente più realistico, i chemiotipi di LPS mostrano ancora distinti “impronte”. A basse concentrazioni, diversi tipi ritardano l’inizio della coagulazione, ma a livelli più alti molti passano a un comportamento pro-coagulante, accorciando i tempi di coagulazione. Un chemiotipo di E. coli, O26:B6, si distingue: quando il suo LPS è assemblato in aggregati stabilizzati dal calcio, continua a rallentare la coagulazione anche ad alte concentrazioni, suggerendo che questo particolare ceppo batterico potrebbe favorire una tendenza persistente a una coagulazione compromessa. Nel complesso, il lavoro rivela che sia la chimica dettagliata dell’LPS sia il suo stato di impacchettamento su scala maggiore determinano se la trombina viene inibita, lasciata intatta o spinta verso una formazione del coagulo più rapida.
Cosa significa per la sepsi e la salute del sangue
Gli autori concludono che l’LPS batterico non è solo un innesco distante dell’infiammazione ma può modulare direttamente l’attività della trombina attraverso il contatto fisico, con effetti che variano da un ceppo batterico all’altro e dipendono da come le molecole si aggregano nel circolo. In termini pratici, questo significa che lo stesso carico complessivo di infezione può portare a schemi di coagulazione molto diversi a seconda della miscela e dello stato dell’LPS presente. Mappando questo nuovo livello di interazione, lo studio contribuisce a spiegare perché la sepsi può causare sia coagulazione eccessiva sia formazione di coaguli compromessa, e apre la strada a terapie che prendono di mira il legame LPS–trombina o l’organizzazione dell’LPS stessa per ripristinare l’equilibrio nel sistema di coagulazione dell’organismo.
Citazione: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Parole chiave: sepsi, trombina, lipopolisaccaride, coagulazione del sangue, batteri Gram-negativi