Clear Sky Science · ja
細菌リポ多糖によるα-トロンビン活性抑制の分子基盤
血栓にとって細菌毒素が重要な理由
グラム陰性菌による重篤な感染は、血液が制御不能に凝固し始めて微小血管を塞ぎ臓器障害を引き起こす危険な連鎖を招くことがあります。本研究は一見単純だが重大な問いを投げかけます:細菌の細胞壁断片が血流に入ったとき、血栓を作る主要酵素であるトロンビンに物理的に影響を与えるのか?特定の細菌分子がトロンビンとどのように相互作用するかを解明することで、敗血症に伴う凝固障害が患者ごとに大きく異なる理由が明らかになり、これらの生命を脅かす事象を予測または制御する新たな手がかりが得られる可能性があります。
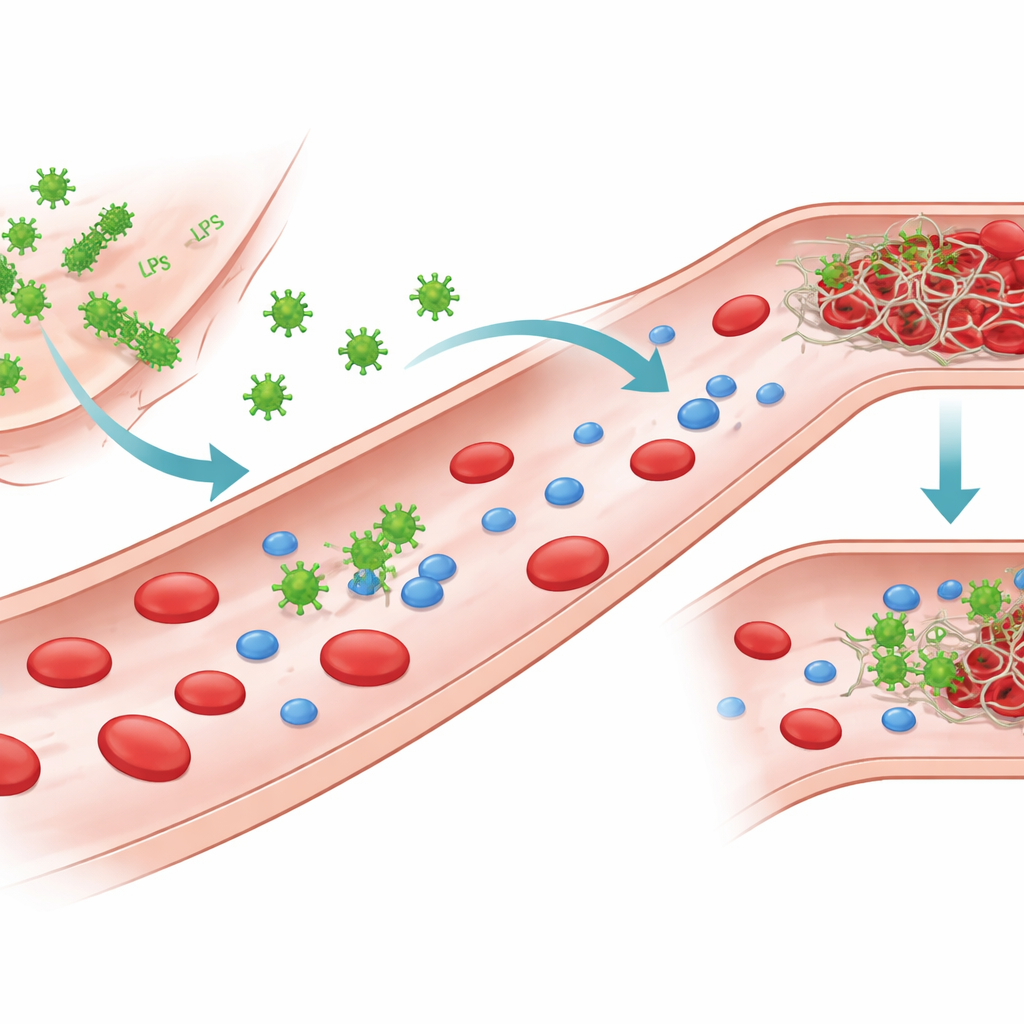
血液と対話する細菌の一部
グラム陰性菌は外膜上にリポ多糖(LPS)という強力な分子を持ちます。細菌が損傷したり破壊されたりすると、LPSは遊離して血中を循環することがあります。著者らは、大腸菌の二つの株を含むいくつかの一般的病原体由来のLPS、ならびにクレブシエラ・ニューモニエ(Klebsiella pneumoniae)と緑膿菌(Pseudomonas aeruginosa)からのLPSに着目しました。すべてが同じ基本骨格を持つ一方で、糖鎖や電荷の配置が異なり、それぞれ異なる「ケモタイプ」を生み出します。これらの構造的差異は、水中でのLPSの集合様式を変え、単分子、小規模クラスター、あるいはより大きなシート状集合体を形成させ、血中タンパク質との相互作用の仕方にも影響を与えます。
LPSが凝固酵素に取りつく仕組み
トロンビンは表面に二つの強く正に帯電したパッチ(エキソサイト)を持ち、通常はフィブリノーゲンや調節因子などの自然な結合相手を認識・配置するのに役立っています。LPSは高度に負に帯電しているため、研究チームはこれらの領域に結合する可能性を疑いました。結合アッセイと感度の高い蛍光測定を組み合わせることで、四種類の細菌由来のLPSがいずれもトロンビンに結合し得ることを示しました。ただし、明確な構造変化をトロンビンにもたらすケモタイプは限られ、特に大腸菌のある株(O26:B6)とクレブシエラ・ニューモニエ由来のLPSが顕著でした。短いDNAベースのプローブで各エキソサイトを遮断する実験により、LPSはこれらの帯電パッチと結合する必要があり、そのためにトロンビンが通常の機能で使う同じ表面に結合していることが確認されました。
細菌断片が凝固機構を遅らせるとき
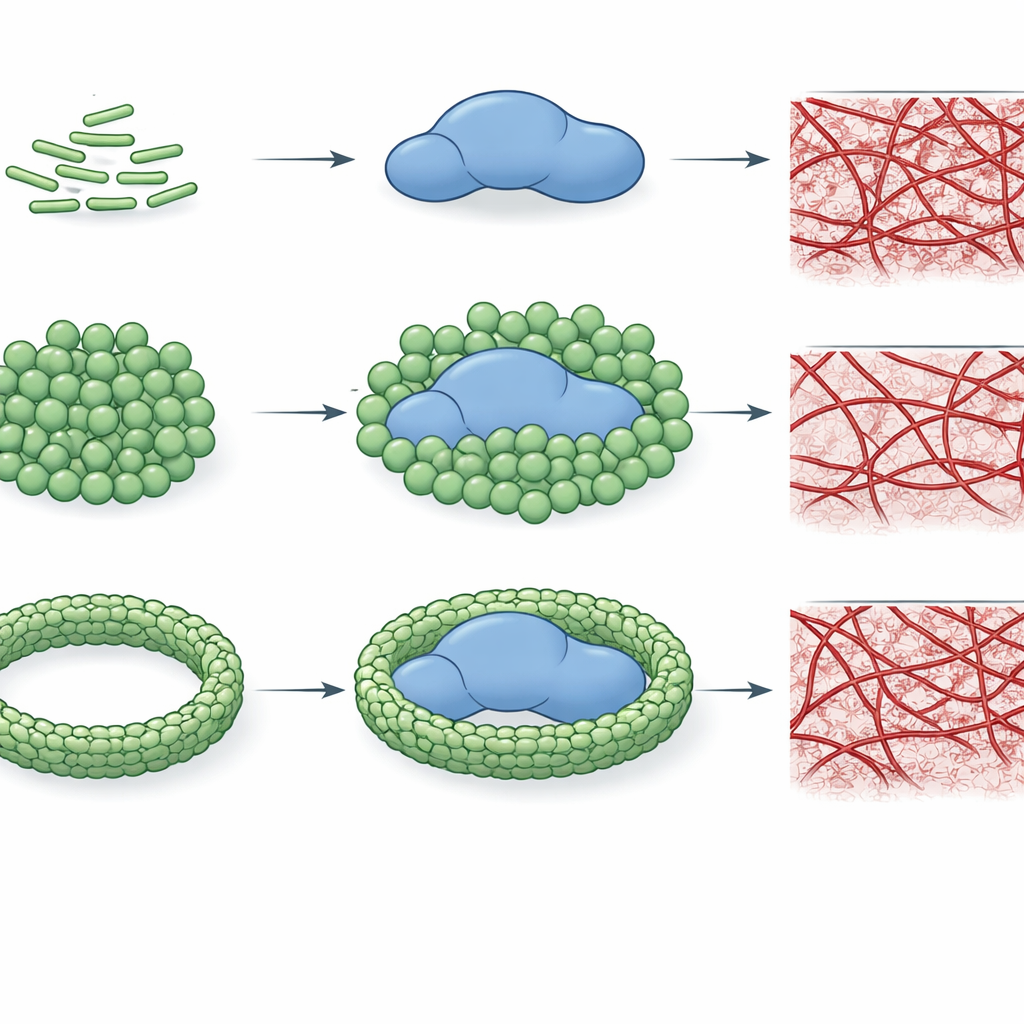
この結合が実際にトロンビンの性能を変えるかを調べるため、著者らは酵素が小さなモデル基質を切断する速度と、フィブリノーゲンをフィブリンネットワークに変換する効率を追跡しました。特定のLPSケモタイプ、特に大腸菌O26:B6およびクレブシエラ・ニューモニエはトロンビンの触媒活性を著しく低下させ、場合によっては百倍以上の抑制を引き起こしました。この抑制はLPSの種類だけでなく、LPS分子の配列や集合状態にも依存します。LPSが小さく曲がったクラスターとして存在するとトロンビンとより親密に相互作用して強く阻害しますが、カルシウムイオンがLPSをより大きく秩序だった凝集体へと駆動すると、あるケモタイプでは抑制が弱まるか失われます。重要なのは、これらのパターンが凝固形成にも反映されることで、特定のLPS形態は精製系においてフィブリンネットワークの組み立てを完全に阻止し得る一方で、他の形態は凝固の進行を遅らせたり、逆に促進したりします。
細菌が違えば凝固の結果も違う
より現実的な環境である血漿中では、多くの他のタンパク質が競合しますが、LPSのケモタイプはここでも明確な「フィンガープリント」を示します。低濃度ではいくつかのタイプが凝固開始を遅らせますが、高濃度になると多くは凝固促進の挙動に切り替わり、凝固時間を短縮します。大腸菌の一つのケモタイプ、O26:B6は際立っており、カルシウムで安定化した凝集体として組み立てられたとき、高濃度でも凝固を遅らせ続けるため、この特定の菌株由来のLPSが持続的に凝固形成不全を誘導する傾向を促す可能性を示唆しています。全体として本研究は、LPSの細かな化学的特性と大規模な配列状態の両方が、トロンビンが抑制されるのか、無傷のままなのか、あるいはむしろ凝固を促進されるのかを決定することを明らかにしています。
敗血症と血液の健康にとっての意義
著者らは、細菌由来のLPSは単なる炎症の遠因ではなく、物理的接触を通じてトロンビンの活性を直接調節し、その影響は菌株ごとに異なり、分子が血中でどのように集合するかに依存すると結論付けています。実務的には、同じ程度の感染負荷でも、存在するLPSの種類と状態の組み合わせによって非常に異なる凝固パターンが生じ得るということです。この新たな相互作用層をマッピングすることで、敗血症が過剰凝固と凝固不全の双方を引き起こす理由の説明に寄与し、LPS–トロンビン結合やLPSの組織化そのものを標的とする治療法によって凝固系のバランスを回復する道を開く可能性があります。
引用: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
キーワード: 敗血症, トロンビン, リポ多糖, 血液凝固, グラム陰性菌