Clear Sky Science · sv
Molekylär grund för hämning av α‑trombins aktivitet av bakteriella lipopolysackarider
Varför bakteriella toxiner spelar roll för blodproppar
Svåra infektioner orsakade av Gramnegativa bakterier kan driva kroppen in i en farlig spiral där blodet börjar koagulera okontrollerat, blockera små kärl och skada organ. Denna studie ställer en vilseledande enkel fråga med stora implikationer: när delar av bakteriers cellväggar kommer ut i blodomloppet, manipulerar de då trombin, den centrala enzymet som bildar blodproppar? Genom att kartlägga hur specifika bakteriella molekyler interagerar med trombin ger arbetet insikt i varför sepsis‑relaterade koagulationsproblem varierar så mycket mellan patienter och kan peka mot nya sätt att förutsäga eller till och med kontrollera dessa livshotande händelser.
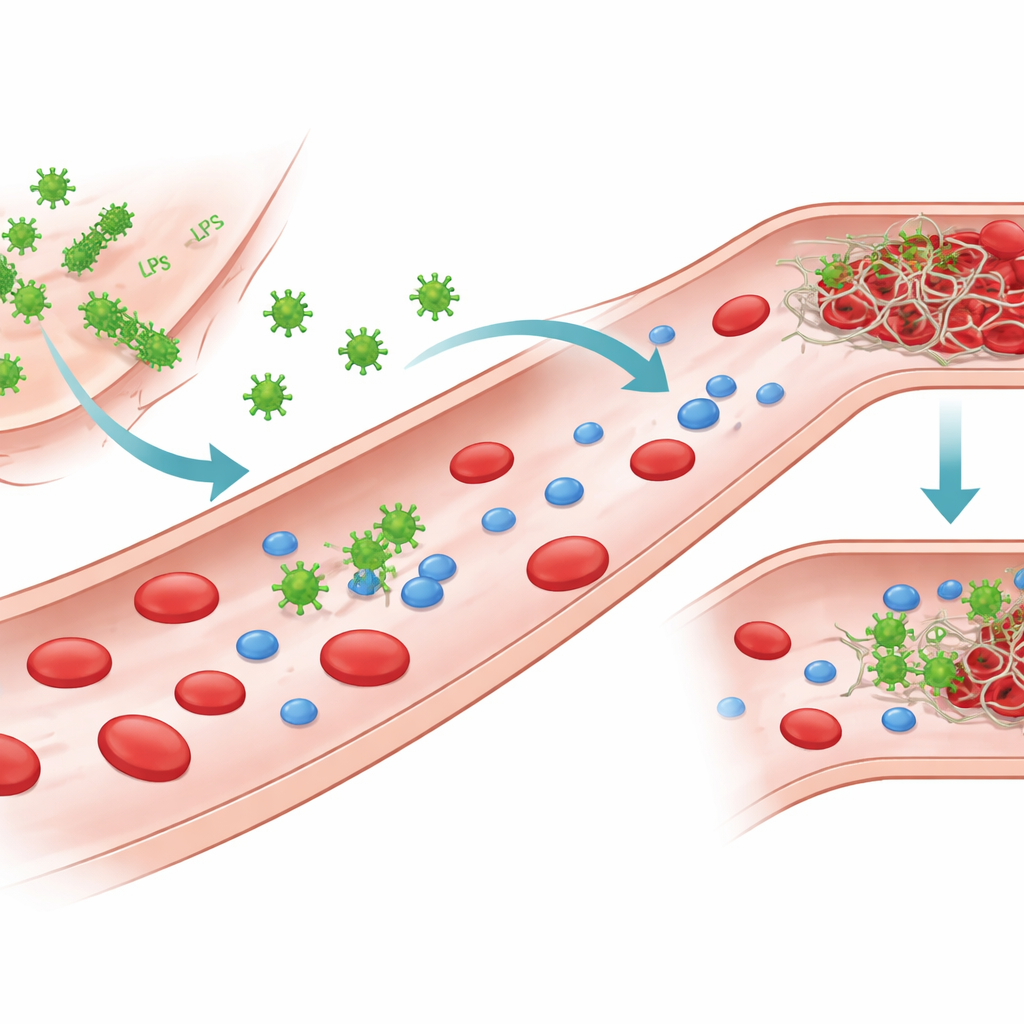
Bitar av bakterier som kommunicerar med blodet
Gramnegativa bakterier bär en potent molekyl kallad lipopolysackarid, eller LPS, på sin yttre yta. När bakterier skadas eller förstörs kan LPS lossna och cirkulera i blodet. Författarna fokuserade på LPS från flera vanliga patogener, inklusive två stammar av Escherichia coli, samt Klebsiella pneumoniae och Pseudomonas aeruginosa. Även om alla bygger på samma grundläggande stomme skiljer sig deras sockerled och laddningsmönster åt, vilket skapar distinkta ”kemotyper”. Dessa strukturella skillnader förändrar hur LPS packas i vatten, och kan bilda enskilda molekyler, små kluster eller större skivliknande assemblys, och de påverkar också hur LPS interagerar med proteiner i blodet.
Hur LPS tar grepp om koagulationsenzymet
Trombin har två starkt positivt laddade ytor på sin yta, kallade exositer, som normalt hjälper det att känna igen och positionera sina naturliga partners som fibrinogen och regulatoriska kofaktorer. Eftersom LPS är högt negativt laddat misstänkte teamet att det kan haka fast vid dessa områden. Genom en kombination av bindningsanalyser och känsliga fluorescensmätningar visade de att LPS från alla fyra bakterier faktiskt kan binda trombin. Men endast vissa kemotyper—framför allt en E. coli‑stam (O26:B6) och Klebsiella pneumoniae—orsakade tydliga strukturella förändringar i trombin. Genom att blockera varje exosit med korta DNA‑baserade prober visade forskarna att LPS måste engagera dessa laddade ytor för att utöva sina effekter, vilket bekräftar att bindningen sker vid samma ytor som trombin använder i sitt normala arbete.
När bakteriella fragment saktar ner koagulationsmaskineriet
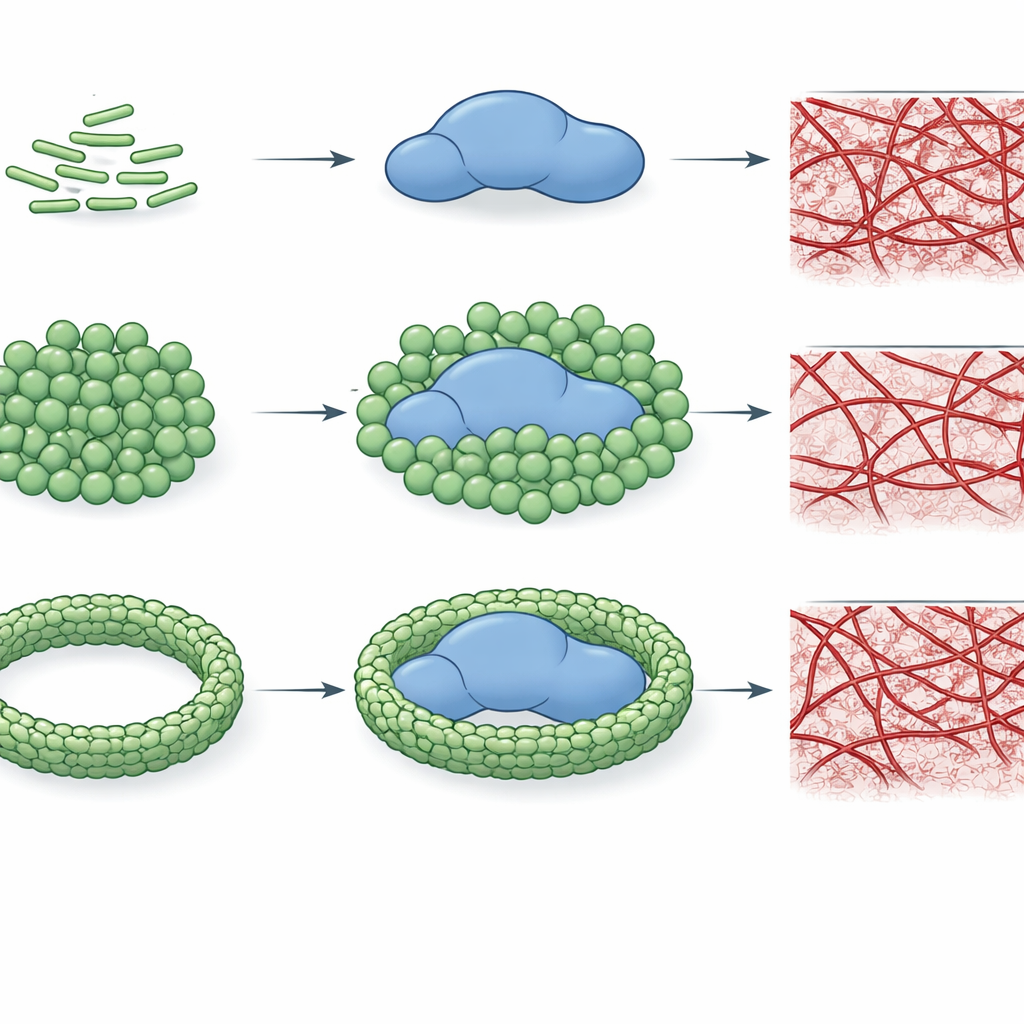
För att testa om denna bindning faktiskt förändrar trombins prestanda följde författarna hur snabbt enzymet klyver ett litet modellsubstrat och hur effektivt det omvandlar fibrinogen till ett fibrinnätverk. De fann att specifika LPS‑kemotyper, särskilt E. coli O26:B6 och Klebsiella pneumoniae, kraftigt kan minska trombins katalytiska förmåga, ibland med mer än hundrafaldig reducering. Denna suppresssion beror inte bara på vilken typ av LPS utan också på hur LPS‑molekylerna är organiserade. När LPS förekommer som mindre, mer krökta kluster interagerar det mer intimt med trombin och hämmar starkt; när kalciumjoner driver LPS till större, mer ordnade aggregationer försvagas hämningen eller försvinner helt för vissa kemotyper. Viktigt är att samma mönster gäller för själva koagelbildningen: vissa LPS‑former kan helt förhindra uppbyggnad av fibrinnätverk i renade system, medan andra bara saktar ner eller till och med påskyndar koageltillväxten.
Olika bakterier, olika koagulationsutfall
Berättelsen blir ännu rikare i plasma, där många andra proteiner konkurrerar om uppmärksamhet. I denna mer realistiska miljö visar LPS‑kemotyper fortfarande distinkta ”fingeravtryck”. Vid låga koncentrationer fördröjer flera typer koagelstart, men vid högre nivåer växlar många till ett pro‑koagulerande beteende och förkortar koagulationstiderna. En E. coli‑kemotyp, O26:B6, står ut: när dess LPS är sammansatt i kalciumstabiliserade aggregationer fortsätter det att sakta ner koagulation även vid höga koncentrationer, vilket antyder att denna särskilda bakteriella stam kan främja en bestående tendens till nedsatt koagelbildning. Sammanfattningsvis visar arbetet att både LPS detaljerade kemi och dess större packningstillstånd avgör om trombin hämmas, lämnas opåverkad eller skjuts mot snabbare koagulation.
Vad detta betyder för sepsis och blodhälsa
Författarna drar slutsatsen att bakteriell LPS inte bara är en avlägsen trigger för inflammation utan kan direkt ställa in trombins aktivitet genom fysisk kontakt, med effekter som varierar mellan bakteriestammar och beroende på hur molekylerna klustras i blodomloppet. I praktiska termer innebär det att samma totala infektionsbörda kan leda till mycket olika koagulationsmönster beroende på vilken blandning och tillstånd av LPS som är närvarande. Genom att kartlägga detta nya interaktionslager hjälper studien till att förklara varför sepsis kan orsaka både överdriven koagulering och nedsatt koagelbildning, och öppnar dörren för terapier som riktar in sig på LPS–trombin‑bindning eller LPS‑organisation för att återställa balansen i kroppens koagulationssystem.
Citering: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Nyckelord: sepsis, trombin, lipopolysackarid, blodkoagulering, Gramnegativa bakterier