Clear Sky Science · pl
Podstawa molekularna hamowania aktywności α-trombiny przez bakteryjne lipopolisacharydy
Dlaczego toksyny bakteryjne mają znaczenie dla krzepliwości krwi
Poważne zakażenia wywołane przez bakterie Gram-ujemne mogą wprowadzić organizm w niebezpieczną spiralę, w której krew zaczyna krzepnąć w niekontrolowany sposób, zatykając drobne naczynia i uszkadzając narządy. W tym badaniu zadano pozornie proste pytanie o dalekosiężnych konsekwencjach: czy fragmenty ścian komórkowych bakterii, trafiając do krwiobiegu, fizycznie zakłócają trombinę — kluczowy enzym odpowiadający za powstawanie skrzepów? Ujawnienie, w jaki sposób konkretne molekuły bakteryjne oddziałują z trombiną, wyjaśnia, dlaczego zaburzenia krzepnięcia związane z sepsą tak bardzo różnią się między pacjentami i może wskazać nowe sposoby przewidywania lub kontrolowania tych zagrażających życiu zdarzeń.
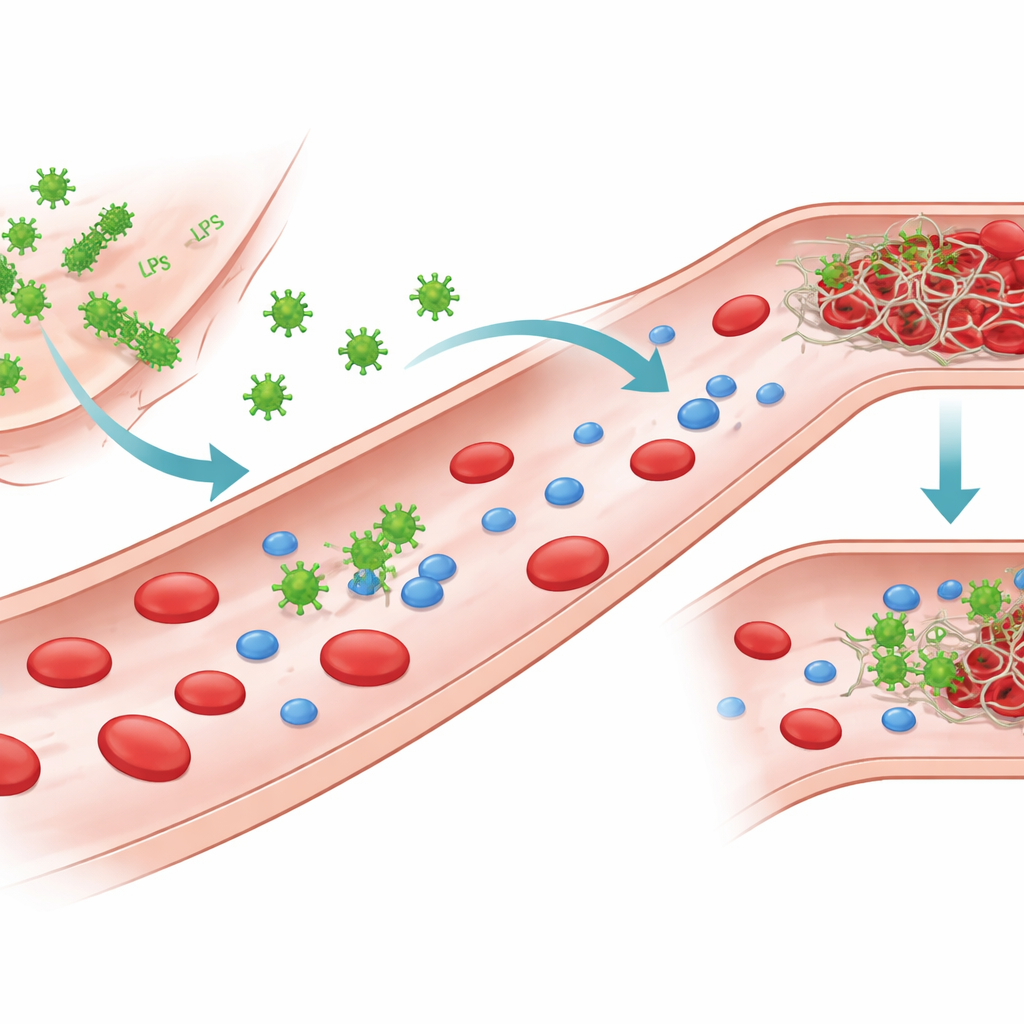
Fragmenty bakterii, które „rozmawiają” z krwią
Bakterie Gram-ujemne mają na swojej zewnętrznej powierzchni silnie działającą cząsteczkę zwaną lipopolisacharydem, w skrócie LPS. Gdy bakterie ulegają uszkodzeniu lub zniszczeniu, LPS może uwolnić się i krążyć we krwi. Autorzy skupili się na LPS pochodzącym od kilku powszechnych patogenów, w tym dwóch szczepów Escherichia coli, a także Klebsiella pneumoniae i Pseudomonas aeruginosa. Choć wszystkie oparte są na tym samym podstawowym szkielecie, różnią się łańcuchami cukrowymi i rozmieszczeniem ładunku, tworząc odrębne „chemotypy”. Te różnice strukturalne wpływają na to, jak LPS układa się w wodzie — tworząc pojedyncze cząsteczki, małe skupiska lub większe, płaskie struktury — oraz na to, jak LPS oddziałuje z białkami krwi.
Jak LPS chwyta enzym krzepnięcia
Trombina ma na swojej powierzchni dwa silnie dodatnio naładowane obszary zwane egzoistotami, które normalnie pomagają jej rozpoznawać i ustawiać naturalnych partnerów, takich jak fibrynogen, oraz kofaktory regulacyjne. Ponieważ LPS jest silnie naładowany ujemnie, zespół badawczy przypuszczał, że może przyłączać się do tych regionów. Wykorzystując kombinację testów wiązania i czułych pomiarów fluorescencyjnych, wykazali, że LPS ze wszystkich czterech bakterii może rzeczywiście wiązać się z trombiną. Jednak tylko niektóre chemotypy — przede wszystkim jeden szczep E. coli (O26:B6) oraz Klebsiella pneumoniae — powodowały wyraźne zmiany strukturalne w trombinie. Blokując każdy egzoistot krótkimi sondami opartymi na DNA, badacze udowodnili, że LPS musi angażować te naładowane powierzchnie, aby wywołać swoje efekty, potwierdzając, że wiązanie zachodzi w tych samych miejscach, których trombina używa do wykonywania swojej normalnej funkcji.
Kiedy fragmenty bakteryjne spowalniają „maszynę” krzepnięcia
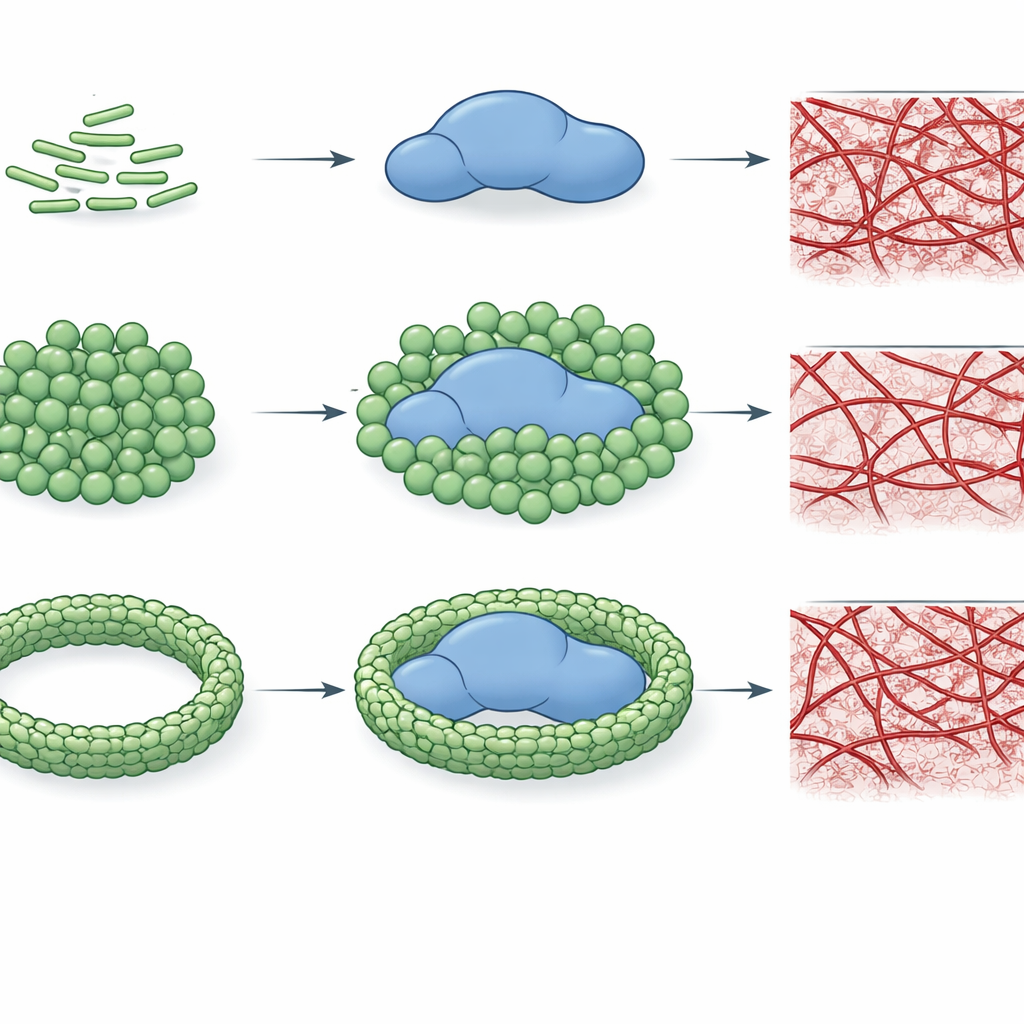
Aby sprawdzić, czy to wiązanie rzeczywiście zmienia wydajność trombiny, autorzy śledzili, jak szybko enzym rozcina mały modelowy substrat oraz jak efektywnie przekształca fibrynogen w sieć fibrynową. Stwierdzili, że określone chemotypy LPS, zwłaszcza E. coli O26:B6 i Klebsiella pneumoniae, mogą znacząco zmniejszać zdolność katalityczną trombiny, czasem nawet ponad sto razy. To tłumienie zależy nie tylko od rodzaju LPS, lecz także od sposobu, w jaki cząsteczki LPS są zorganizowane. Gdy LPS występuje jako mniejsze, bardziej zakrzywione skupiska, wchodzi w bliższe interakcje z trombiną i silnie ją hamuje; gdy jony wapnia powodują tworzenie większych, bardziej uporządkowanych agregatów LPS, hamowanie osłabia się lub znika dla niektórych chemotypów. Co istotne, te same wzorce obserwuje się przy formowaniu skrzepu: pewne formy LPS mogą całkowicie zapobiec tworzeniu się sieci fibrynowej w układach oczyszczonych, podczas gdy inne jedynie spowalniają albo nawet przyspieszają wzrost skrzepu.
Różne bakterie, różne skutki krzepnięcia
Obraz staje się jeszcze bardziej złożony w osoczu, gdzie wiele innych białek konkuruje o interakcje. W tym bardziej realistycznym środowisku chemotypy LPS nadal wykazują odrębne „odciski palców”. Przy niskich stężeniach kilka typów opóźnia początek krzepnięcia, ale przy wyższych wiele z nich przełącza się na prokrzepliwe działanie, skracając czasy krzepnięcia. Jeden chemotyp E. coli, O26:B6, wyróżnia się: gdy jego LPS tworzy wapniem stabilizowane agregaty, nadal spowalnia krzepnięcie nawet przy wysokich stężeniach, co sugeruje, że ten konkretny szczep bakteryjny może sprzyjać utrzymującej się tendencji do upośledzonego tworzenia skrzepów. Ogólnie rzecz biorąc, praca pokazuje, iż zarówno szczegółowa chemia LPS, jak i jego większa skala pakowania decydują o tym, czy trombina jest hamowana, pozostaje niezmieniona, czy skłaniana do szybszego tworzenia skrzepu.
Co to oznacza dla sepsy i zdrowia krwi
Autorzy wnioskują, że bakteryjny LPS nie jest tylko odległym wyzwalaczem zapalenia, lecz może bezpośrednio modulować aktywność trombiny przez kontakt fizyczny, z efektami, które różnią się między szczepami bakteryjnymi i zależą od sposobu, w jaki molekuły grupują się we krwiobiegu. W praktycznym ujęciu oznacza to, że ten sam ogólny ciężar infekcji może prowadzić do bardzo różnych wzorców krzepnięcia w zależności od składu i stanu LPS. Mapując tę nową warstwę interakcji, badanie pomaga wyjaśnić, dlaczego sepsa może powodować zarówno nadmierne krzepnięcie, jak i upośledzone tworzenie skrzepów, oraz otwiera drogę do terapii celujących w wiązanie LPS z trombiną lub w organizację LPS, by przywrócić równowagę systemu krzepnięcia.
Cytowanie: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Słowa kluczowe: sepsa, trombina, lipopolisacharyd, krzepnięcie krwi, bakterie Gram-ujemne