Clear Sky Science · de
Molekulare Grundlage der Hemmung der α-Thrombin-Aktivität durch bakterielle Lipopolysaccharide
Warum bakterielle Toxine für Blutgerinnsel wichtig sind
Schwere Infektionen durch gramnegative Bakterien können den Körper in eine gefährliche Spirale treiben, bei der das Blut unkontrolliert gerinnt, kleine Gefäße verstopft und Organe schädigt. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wenn Bruchstücke bakterieller Zellwände in den Blutkreislauf gelangen, beeinflussen sie dann physikalisch Thrombin, das Schlüsselenzym der Blutgerinnung? Indem untersucht wird, wie bestimmte bakterielle Moleküle mit Thrombin interagieren, trägt die Arbeit dazu bei zu erklären, warum sepsisbedingte Gerinnungsstörungen so sehr zwischen Patientinnen und Patienten variieren, und sie könnte neue Wege aufzeigen, diese lebensbedrohlichen Ereignisse vorherzusagen oder sogar zu steuern.
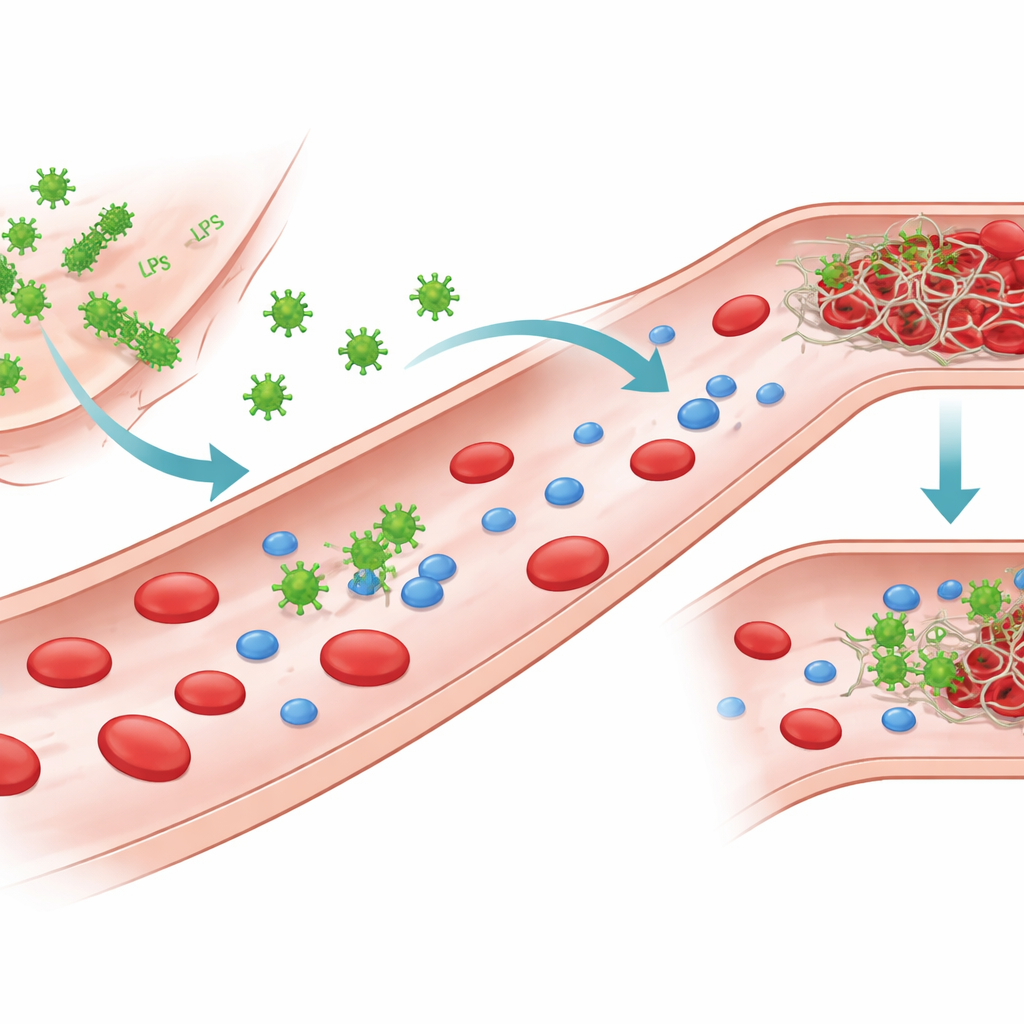
Bakterienstücke, die mit dem Blut kommunizieren
Gramnegative Bakterien tragen an ihrer Außenseite ein potentes Molekül, das Lipopolysaccharid (LPS) genannt wird. Wenn Bakterien beschädigt oder zerstört werden, kann LPS freiwerden und im Blut zirkulieren. Die Autoren konzentrierten sich auf LPS von mehreren verbreiteten Krankheitserregern, darunter zwei Stämme von Escherichia coli sowie Klebsiella pneumoniae und Pseudomonas aeruginosa. Obwohl alle auf derselben Grundstruktur beruhen, unterscheiden sich ihre Zuckerketten und Ladungsmuster und bilden dadurch verschiedene „Chemotypen“. Diese strukturellen Unterschiede verändern, wie sich LPS im Wasser packt — als Einzelmoleküle, kleine Klumpen oder größere blattartige Assemblies — und beeinflussen auch, wie LPS mit Proteinen im Blut interagiert.
Wie LPS das Gerinnungsenzym ergreift
Thrombin besitzt auf seiner Oberfläche zwei stark positiv geladene Bereiche, Exosite genannt, die ihm normalerweise helfen, natürliche Partner wie Fibrinogen und regulatorische Kofaktoren zu erkennen und zu positionieren. Da LPS stark negativ geladen ist, vermutete das Team, dass es sich an diese Regionen heftet. Mithilfe einer Kombination aus Bindungsassays und empfindlichen Fluoreszenzmessungen zeigten sie, dass LPS aus allen vier Bakterien tatsächlich an Thrombin binden kann. Allerdings lösten nur einige Chemotypen — insbesondere ein E.-coli-Stamm (O26:B6) und Klebsiella pneumoniae — deutliche strukturelle Veränderungen in Thrombin aus. Durch Blockade jedes Exosites mit kurzen DNA-basierten Sonden demonstrierten die Forschenden, dass LPS diese geladenen Flächen ansprechen muss, um seine Wirkung zu entfalten, und bestätigten damit, dass die Bindung an denselben Oberflächen erfolgt, die Thrombin für seine normale Funktion nutzt.
Wenn bakterielle Fragmente die Gerinnungsmaschine verlangsamen
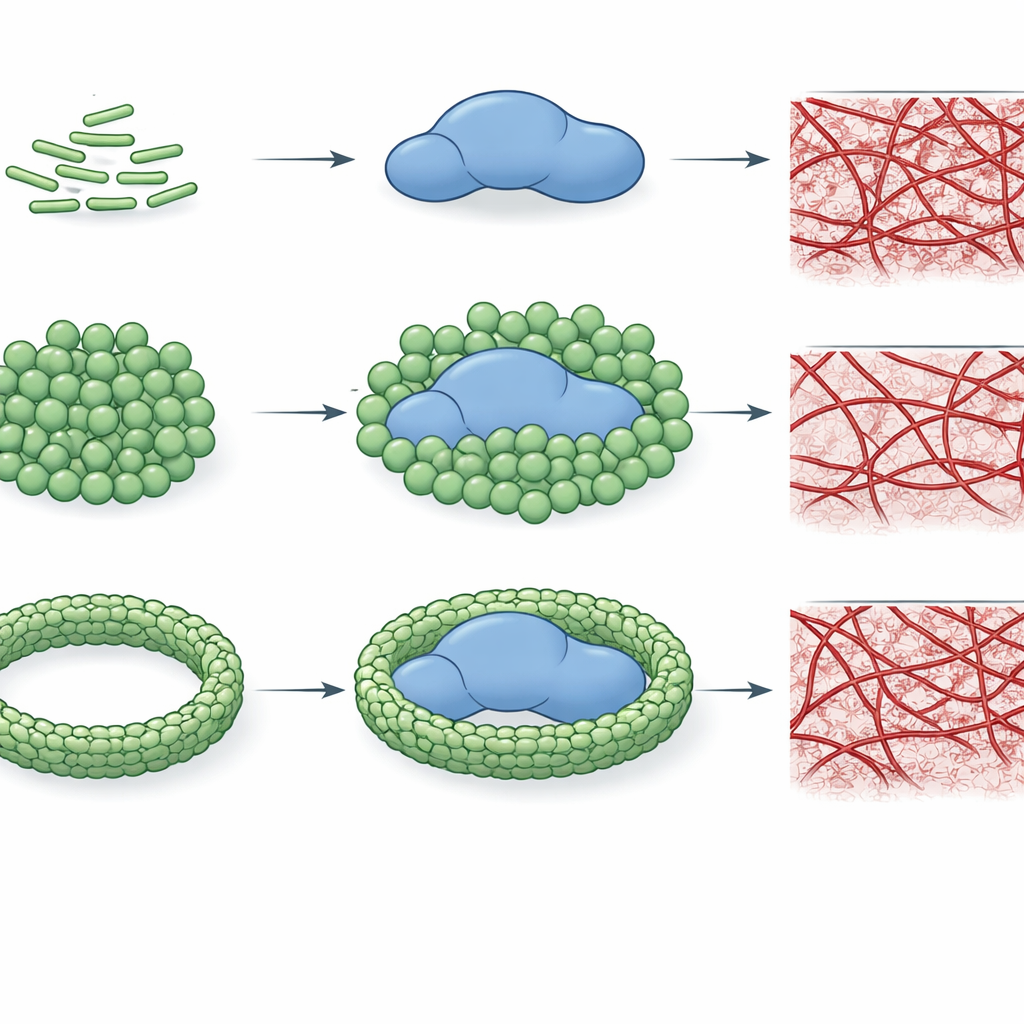
Um zu prüfen, ob diese Bindung tatsächlich die Leistung von Thrombin verändert, verfolgten die Autoren, wie schnell das Enzym ein kleines Modellsubstrat spaltet und wie effizient es Fibrinogen in ein Fibrinnetz umsetzt. Sie fanden heraus, dass spezifische LPS-Chemotypen, vor allem E. coli O26:B6 und Klebsiella pneumoniae, die katalytische Aktivität von Thrombin erheblich reduzieren können — mitunter um mehr als das Hundertfache. Diese Hemmung hängt nicht nur vom LPS-Typ, sondern auch von der Organisation der LPS-Moleküle ab. Wenn LPS als kleinere, stärker gekrümmte Cluster vorliegt, interagiert es enger mit Thrombin und hemmt es stark; wenn Calciumionen LPS in größere, geordnete Aggregate überführen, wird die Hemmung abgeschwächt oder geht bei manchen Chemotypen ganz verloren. Wichtig ist, dass sich diese Muster auch auf die Gerinnungsbildung übertragen: Bestimmte LPS-Formen können in gereinigten Systemen die Assemblierung eines Fibrinnetzes vollständig verhindern, während andere nur das Netzwerkwachstum verlangsamen oder sogar beschleunigen.
Unterschiedliche Bakterien, unterschiedliche Gerinnungsergebnisse
Die Situation wird in Plasma noch komplexer, wo viele weitere Proteine um Bindungsstellen konkurrieren. In dieser realistischeren Umgebung zeigen LPS-Chemotypen weiterhin unterschiedliche „Fingerabdrücke“. Bei niedrigen Konzentrationen verzögern mehrere Typen den Beginn der Gerinnung, bei höheren Konzentrationen schalten viele jedoch auf prokoagulative Verhaltensweisen um und verkürzen die Gerinnungszeiten. Ein E.-coli-Chemotyp, O26:B6, sticht hervor: Wenn sein LPS in calciumstabilisierte Aggregate überführt ist, verlangsamt es die Gerinnung selbst bei hohen Konzentrationen weiterhin, was darauf hindeutet, dass dieser spezielle Bakterienstamm eine anhaltende Neigung zu beeinträchtigter Blutgerinnung fördern könnte. Insgesamt zeigt die Arbeit, dass sowohl die feine Chemie des LPS als auch sein großmaßstäblicher Packungszustand bestimmen, ob Thrombin gehemmt, unbeeinträchtigt bleibt oder zu schnellerer Gerinnung gedrängt wird.
Was das für Sepsis und Blutgesundheit bedeutet
Die Autoren schließen daraus, dass bakterielles LPS nicht nur ein entfernter Entzündungs-Auslöser ist, sondern Thrombins Aktivität durch direkten physischen Kontakt feinsteuern kann — mit Effekten, die von Stamm zu Stamm variieren und davon abhängen, wie die Moleküle im Blut organisiert sind. Praktisch bedeutet dies, dass dieselbe allgemeine Infektionslast sehr unterschiedliche Gerinnungsmuster hervorrufen kann, abhängig von Mischung und Zustand des vorhandenen LPS. Durch die Kartierung dieser neuen Interaktionsschicht hilft die Studie zu erklären, warum Sepsis sowohl zu übermäßiger Gerinnung als auch zu beeinträchtigter Gerinnselbildung führen kann, und sie eröffnet Ansätze für Therapien, die die LPS–Thrombin-Bindung oder die Organisation von LPS gezielt adressieren, um das Gleichgewicht des Gerinnungssystems wiederherzustellen.
Zitation: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Schlüsselwörter: Sepsis, Thrombin, Lipopolysaccharid, Blutgerinnung, Gramnegative Bakterien