Clear Sky Science · fr
Base moléculaire de l’inhibition de l’activité de l’α-thrombine par les lipopolysaccharides bactériens
Pourquoi les toxines bactériennes comptent pour la coagulation
Les infections sévères causées par des bactéries à Gram négatif peuvent entraîner une spirale dangereuse où le sang se met à coaguler de manière incontrôlée, obstruant les petits vaisseaux et endommageant les organes. Cette étude pose une question apparemment simple mais aux grandes implications : lorsque des fragments de paroi bactérienne pénètrent dans la circulation, viennent-ils physiquement altérer la thrombine, l’enzyme clé de la formation des caillots ? En révélant comment des molécules bactériennes spécifiques interagissent avec la thrombine, ce travail éclaire pourquoi les troubles de la coagulation liés à la septicémie varient tant d’un patient à l’autre et peut indiquer de nouvelles façons de prédire ou même de contrôler ces événements potentiellement mortels.
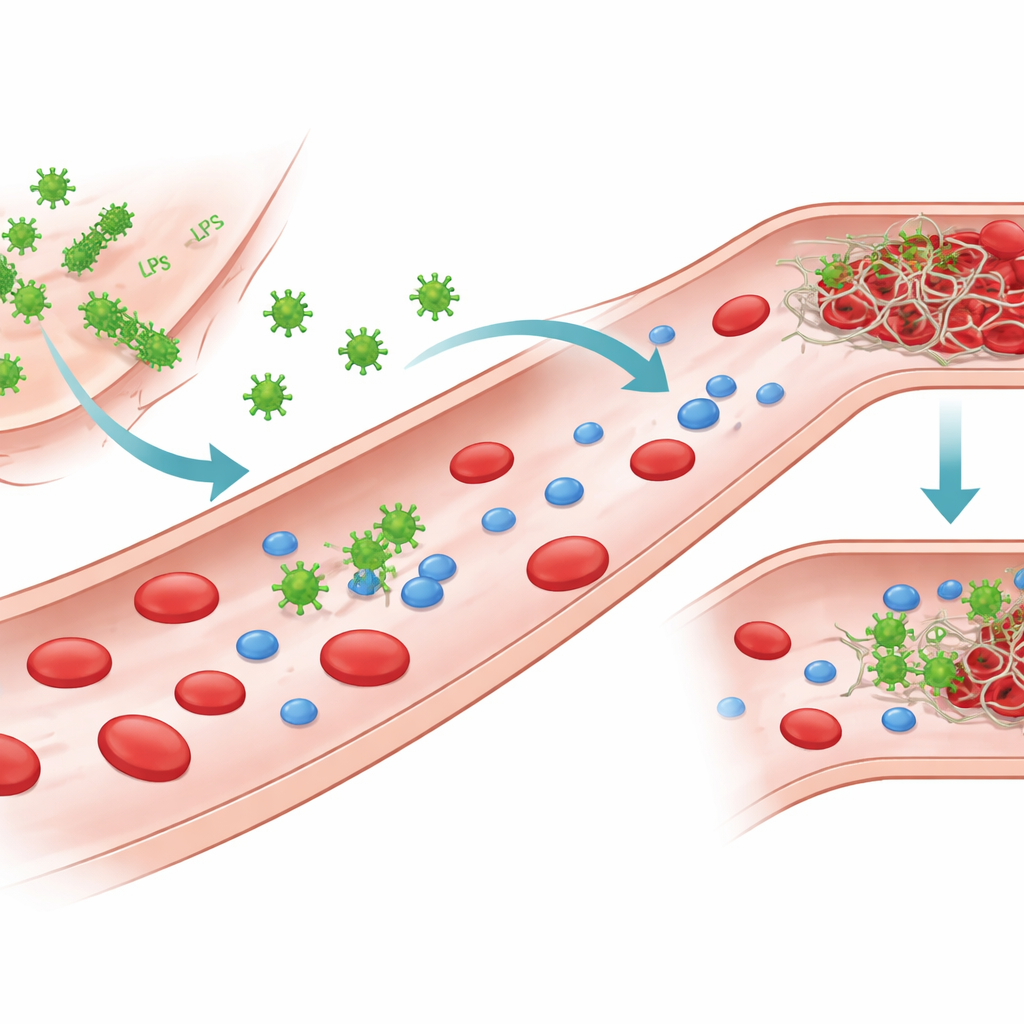
Fragments bactériens qui dialoguent avec le sang
Les bactéries à Gram négatif portent à leur surface externe une molécule puissante appelée lipopolysaccharide, ou LPS. Lorsque les bactéries sont endommagées ou détruites, le LPS peut se détacher et circuler dans le sang. Les auteurs se sont intéressés aux LPS de plusieurs agents pathogènes courants, notamment deux souches d’Escherichia coli, ainsi que Klebsiella pneumoniae et Pseudomonas aeruginosa. Bien qu’ils reposent tous sur le même échafaudage de base, leurs chaînes de sucres et leurs motifs de charge diffèrent, créant des « chiménotypes » distincts. Ces différences structurelles modifient la façon dont le LPS s’organise en solution aqueuse, formant des molécules isolées, de petits agrégats ou des assemblages en feuillets plus larges, et elles influent aussi sur les interactions du LPS avec les protéines sanguines.
Comment le LPS s’accroche à l’enzyme de la coagulation
La thrombine porte à sa surface deux zones fortement chargées positivement, appelées exosites, qui l’aident normalement à reconnaître et positionner ses partenaires naturels comme la fibrinogène et des cofacteurs régulateurs. Parce que le LPS est fortement chargé négativement, l’équipe a supposé qu’il pourrait se lier à ces régions. À l’aide d’un mélange d’essais de liaison et de mesures de fluorescence sensibles, ils ont montré que le LPS des quatre bactéries pouvait effectivement se lier à la thrombine. Cependant, seuls certains chiménotypes — en particulier une souche d’E. coli (O26:B6) et Klebsiella pneumoniae — induisaient des changements structuraux nets dans la thrombine. En bloquant chaque exosite avec de courtes sondes à base d’ADN, les chercheurs ont démontré que le LPS doit engager ces zones chargées pour produire ses effets, confirmant que la liaison se fait aux mêmes surfaces que celles utilisées par la thrombine pour sa fonction normale.
Quand des fragments bactériens ralentissent la machine à coaguler
Pour vérifier si cette liaison modifie réellement les performances de la thrombine, les auteurs ont suivi la vitesse à laquelle l’enzyme clive un petit substrat modèle et son efficacité à convertir la fibrinogène en un réseau de fibrine. Ils ont constaté que des chiménotypes de LPS spécifiques, notamment E. coli O26:B6 et Klebsiella pneumoniae, peuvent réduire considérablement le pouvoir catalytique de la thrombine, parfois de plus d’un centuple. Cette suppression dépend non seulement du type de LPS mais aussi de l’organisation des molécules de LPS. Quand le LPS existe sous forme de petits agrégats plus courbés, il interagit plus intimement avec la thrombine et l’inhibe fortement ; lorsque des ions calcium favorisent la formation d’agrégats plus grands et ordonnés, l’inhibition est affaiblie voire perdue pour certains chiménotypes. De façon importante, ces mêmes tendances se retrouvent au niveau de la formation du caillot : certaines formes de LPS peuvent empêcher complètement l’assemblage du réseau de fibrine dans des systèmes purifiés, tandis que d’autres ralentissent simplement ou, au contraire, accélèrent la croissance du caillot.
Des bactéries différentes, des conséquences de coagulation différentes
L’histoire devient encore plus riche dans le plasma, où de nombreuses autres protéines entrent en compétition. Dans cet environnement plus réaliste, les chiménotypes de LPS conservent des « empreintes » distinctes. À faibles concentrations, plusieurs types retardent le déclenchement de la coagulation, mais à des niveaux plus élevés beaucoup se comportent de manière pro-coagulante, raccourcissant les temps de coagulation. Un chiménotype d’E. coli, O26:B6, se distingue : lorsque son LPS est assemblé en agrégats stabilisés par le calcium, il continue de ralentir la coagulation même à forte concentration, laissant supposer que cette souche bactérienne particulière pourrait favoriser une tendance persistante à l’altération de la formation des caillots. Dans l’ensemble, le travail montre que la chimie détaillée du LPS et son état d’assemblage à grande échelle déterminent si la thrombine est inhibée, laissée intacte ou poussée vers une formation de caillot plus rapide.
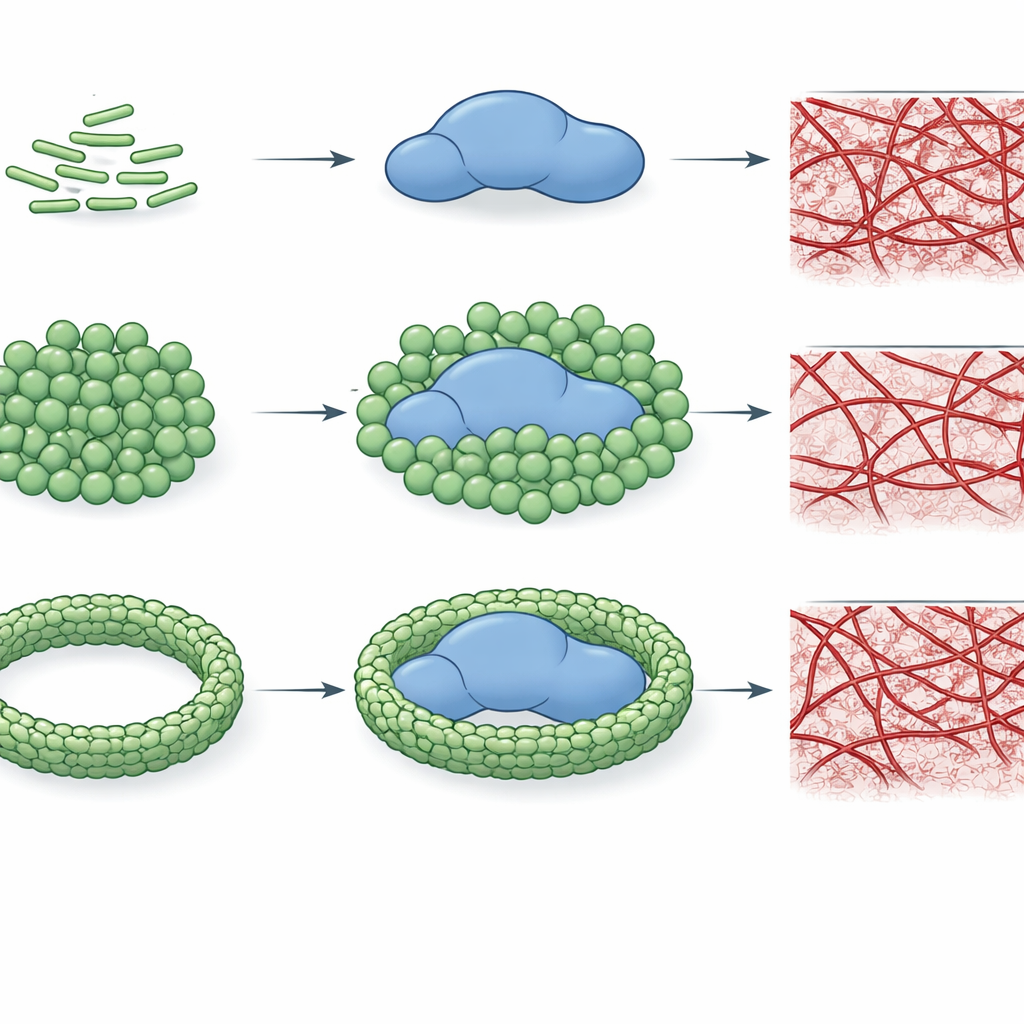
Ce que cela signifie pour la septicémie et la santé vasculaire
Les auteurs concluent que le LPS bactérien n’est pas seulement un déclencheur d’inflammation à distance mais peut modul er directement l’activité de la thrombine par contact physique, avec des effets qui varient selon la souche bactérienne et selon la manière dont ces molécules s’assemblent dans la circulation. En termes pratiques, cela signifie que la même charge infectieuse globale peut conduire à des profils de coagulation très différents selon le mélange et l’état du LPS présent. En cartographiant ce nouveau niveau d’interaction, l’étude aide à expliquer pourquoi la septicémie peut provoquer à la fois une coagulation excessive et une formation de caillots perturbée, et ouvre la voie à des thérapies visant la liaison LPS–thrombine ou l’organisation du LPS lui-même pour restaurer l’équilibre du système de coagulation.»}
Citation: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
Mots-clés: septicémie, thrombine, lipopolysaccharide, coagulation sanguine, bactéries à Gram négatif