Clear Sky Science · he
הבסיס המולקולרי לעיכוב פעילות α-תרומבין על ידי ליפופוליסכרידים חיידקיים
מדוע רעלנים חיידקיים חשובים לקליטת קרישים
זיהומים קשים הנגרמים על ידי חיידקים גרם-שליליים יכולים לדחוף את הגוף לסחרור מסוכן שבו הדם מתחיל לקרוש ללא שליטה, סותם כלי דם קטנים ופוגע באיברים. המחקר הזה שואל שאלה שנראית פשוטה אך בעלת השלכות רחבות: כאשר חלקים מדפנות תאים חיידקיות נכנסים למחזור הדם, האם הם משפיעים באופן פיזי על התרומבין — האנזים המרכזי היוצר קרישי דם? על ידי גילוי האופן שבו מולקולות חיידקיות ספציפיות מתקשרות עם התרומבין, העבודה מאירה מדוע בעיות קרישה הקשורות לספסיס שונות כל כך בין מטופל למטופל ועלולה להצביע על דרכים חדשות לחיזוי או אפילו לשליטה באירועים מסכני חיים אלו.
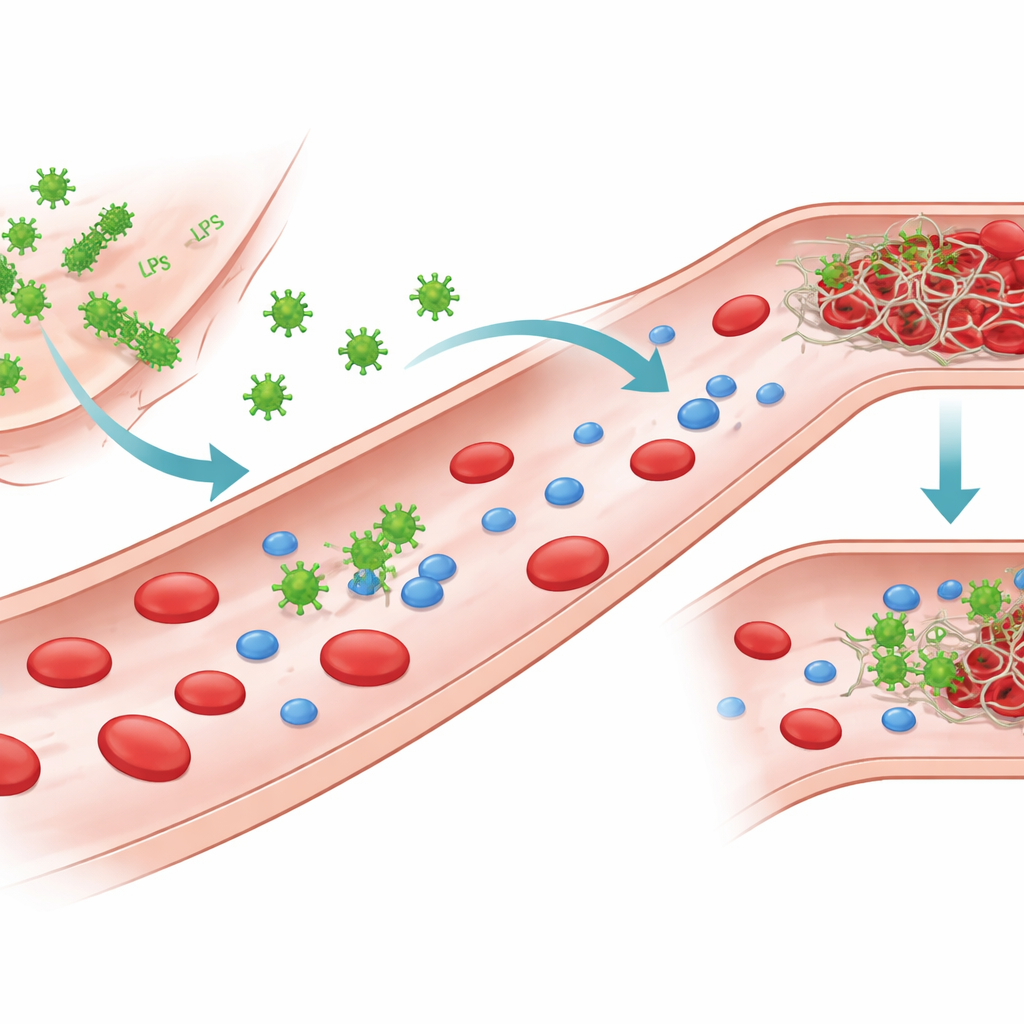
חתיכות חיידק שמתקשרות עם הדם
לחיידקים גרם-שליליים יש מולקולה עוצמתית הנקראת ליפופוליסכריד, או LPS, בחלק החיצוני שלהם. כאשר החיידקים ניזוקים או נהרסים, LPS יכול להשתחרר ולהסתובב בדם. החוקרים התמקדו ב‑LPS ממספר פתוגנים נפוצים, כולל שני זנים של Escherichia coli וכן Klebsiella pneumoniae ו‑Pseudomonas aeruginosa. אף שכולן בנויות על שלד בסיסי דומה, שרשראות הסוכר ודפוסי המטען שלהן שונים, ויוצרים "כימוטיפים" מובחנים. הבדלים מבניים אלה משנים את אופן הארגון של ה‑LPS במים, ויכולים ליצור מולקולות יחידות, צבירים קטנים או הרכבים משטחים גדולים יותר, וכן משפיעים על האינטראקציה של ה‑LPS עם חלבונים בדם.
איך LPS נצמד לאנזים הקרישה
לתרומבין יש שני אזורים בעלי מטען חיובי חזק על פניו, הנקראים אקסוסייטים, שבעזרתם הוא מזהה וממקם שותפים טבעיים כמו פיברינוגן וקופקטורים רגולטוריים. מכיוון שה‑LPS טעון שלילית מאוד, הצוות חשש שהוא עשוי להיצמד לאזורים אלה. באמצעות שילוב של בדיקות קשירה ומדידות פלואורסצנטיות רגישות, הם הראו כי LPS מכל ארבעת החיידקים יכול אכן לקשור את התרומבין. עם זאת, רק כמה כימוטיפים — בולט במיוחד זן אחד של E. coli (O26:B6) ו‑Klebsiella pneumoniae — גרמו לשינויים מבניים ברוריים בתרומבין. על ידי חסימת כל אקסוסייט עם פרובים קצרים מבוססי DNA, החוקרים הדגימו ש‑LPS חייב לתקשר עם הכתמים המטעיונים הללו כדי להפעיל את השפעותיו, ואישרו שהקשירה מתרחשת על פני השטח שבהן התרומבין עושה את עבודתו הרגילה.
מתי שברי חיידקים מעכבים את מכונת הקרישה
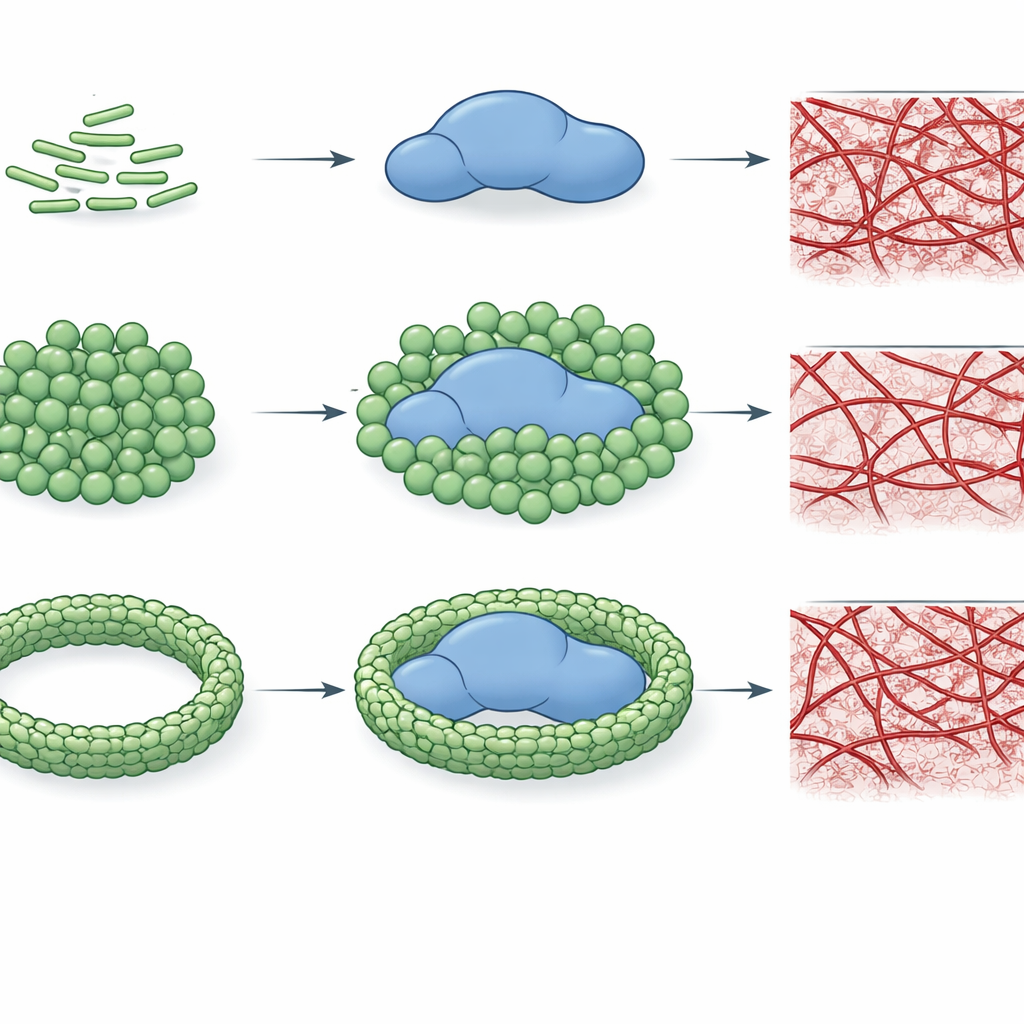
כדי לבחון האם קשירה זו באמת משנה את ביצועי התרומבין, המחברים עקבו אחרי המהירות בה האנזים חותך תת-סטרטג קטן וכמה יעיל הוא בהמרת פיברינוגן לרשת פיברין. הם מצאו שכימוטיפים מסוימים של LPS, במיוחד E. coli O26:B6 ו‑Klebsiella pneumoniae, יכולים להפחית באופן ניכר את הכוח הקטליטי של התרומבין, לפעמים ביותר ממאה פעמים. דיכוי זה תלוי לא רק בסוג ה‑LPS אלא גם באופן שבו מולקולות ה‑LPS מאורגנות. כאשר ה‑LPS קיים כצברים קטנים ומעוקלים יותר, הוא מתקשר ביתר אינטימיות עם התרומבין ומעכב אותו באופן חזק; כאשר יוני סידן דוחפים את ה‑LPS לצבירים גדולים ומסודרים יותר, העיכוב נחלש או אף נעלם עבור כמה כימוטיפים. חשובה מזה, דפוסים אלה משתקפים גם בהיווצרות קריש: צורות מסוימות של LPS יכולות למנוע לחלוטין הרכבת רשת הפיברין במערכות מטוהרות, בעוד אחרות רק מאטות או אפילו מאיצות את גדילת הקריש.
חיידקים שונים — תוצאות קרישה שונות
הסיפור נעשֶה עמוק עוד יותר בפלזמה, שבה חלבונים רבים נוספים מתחרים על תשומת הלב. בסביבה הריאליסטית יותר הזו כימוטיפים של LPS עדיין מציגים "טביעות אצבע" מובחנות. בריכוזים נמוכים, כמה סוגים מעכבים את תחילת הקרישה, אך ברמות גבוהות רבים מהם עוברים להתנהגות פרו-קרישתית, ומקצרים את זמני הקרישה. כימוטיפ אחד של E. coli, O26:B6, בולט: כאשר ה‑LPS שלו מארגן לצבירים המוצבים על ידי סידן, הוא ממשיך להאט את הקרישה אפילו בריכוזים גבוהים, מרמז שזן חיידקי זה עשוי לקדם נטייה מתמשכת להיווצרות קרישים פגומים. בסך הכול, העבודה מראה כי הן הכימיה המפורטת של ה‑LPS והן מצב הארגון שלו בקנה מידה גדול קובעים האם התרומבין מעוכב, נשאר ללא שינוי או נדחף לכיוון יצירת קרישים מהירה יותר.
מה המשמעות לכך בספסיס ובבריאות הדם
המחברים מסכמים כי LPS חיידקי אינו רק מפעיל דלקת מרחוק אלא יכול לכוונן ישירות את פעילות התרומבין באמצעות מגע פיזי, עם השפעות המשתנות מזן חיידקי אחד לאחר ותלויות באופן בו המולקולות מצטברות במחזור הדם. מבחינה מעשית, משמעות הדבר היא כי אותו עומס זיהומי כללי עלול להוביל לדפוסי קרישה שונים מאוד בהתאם לתערובת ולמצב ה‑LPS הנוכחי. על ידי מיפוי שכבה חדשה זו של אינטראקציה, המחקר מסייע להסביר מדוע הספסיס יכול לגרום גם לקרישה מופרזת וגם לפגמים ביצירת קריש, והוא פותח פתח לטיפולים המכוונים לקשירת LPS–תרומבין או לארגון ה‑LPS עצמו כדי לשחזר איזון במערכת הקרישה של הגוף.
ציטוט: Lira, A.L., Drew, K.C., Dantas, R.L.M. et al. Molecular basis for inhibition of α-thrombin activity by bacterial lipopolysaccharides. Sci Rep 16, 10851 (2026). https://doi.org/10.1038/s41598-026-46276-5
מילות מפתח: ספסיס, תרומבין, ליפופוליסכריד, קרישת דם, חיידקים גרם-שליליים