Clear Sky Science · zh
CRISPR/Cas9介导的人促红细胞生成素在β-酪蛋白位点的定点敲入在HC11乳腺上皮细胞中产生泌乳激素响应性表达
将乳汁细胞变成微型药物工厂
许多现代药物是我们体内自然产生的蛋白质,但在工厂规模化生产这些蛋白既昂贵又技术要求高。这项研究探索了一种巧妙的替代方法:重新编程产奶细胞,使其像在泌乳期自然开启乳蛋白那样,仅在激素触发时开启一种人源治疗蛋白。该工作展示了未来农场动物如何在其乳汁中安全、高效地生产复杂药物的可能性。
目标是安全、精确的药物生产
多年来,科学家尝试利用转基因动物生产诸如人促红细胞生成素(hEPO)等药物,hEPO是一种能促进红细胞生成的激素。早期尝试依赖将hEPO基因随机插入基因组,这常导致若干问题:基因可能在错误组织中表达、被沉默或引发动物疾病。本文作者试图通过将hEPO基因安置在基因组中一个非常特定、研究充分的位置来解决这些问题:该位置正是调控乳腺(产奶)细胞主要乳蛋白β-酪蛋白的区域。
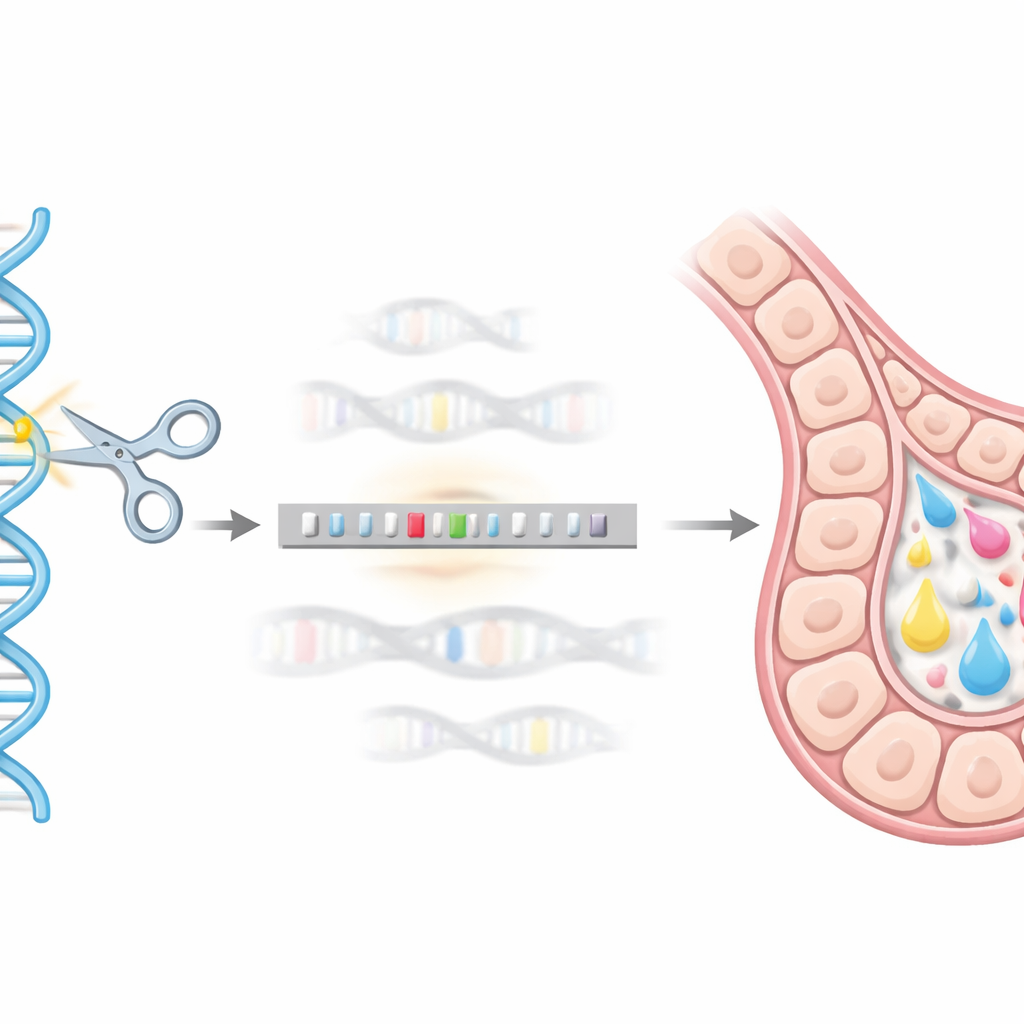
将基因编辑作为基因组“GPS”
为到达这一精确的基因组地址,研究团队将CRISPR/Cas9基因编辑系统用作一种分子定位与剪切工具。他们设计了携带与辅助标签(GST)融合的hEPO基因的DNA供体构建体,并在两侧加入与β-酪蛋白区段匹配的短同源序列。当CRISPR/Cas9在小鼠乳腺HC11细胞中切割目标位点时,细胞的自然修复机制可使用该供体构建体作为模板,将hEPO序列整齐地插入β-酪蛋白位点。通过一系列基因检测(基于PCR的方法),他们分离出单细胞克隆,其中一份β-酪蛋白拷贝已被hEPO构建体成功替代,生成了稳定的“敲入”细胞系。
激素开关模拟天然乳蛋白产生
研究者接着验证这一新的hEPO基因是否遵循与正常乳蛋白基因相同的开/关规则。HC11细胞可以通过加入“泌乳”激素被诱导进入类似泌乳的状态,类似于哺乳动物体内起作用的激素。在工程化的克隆细胞中,团队在激素处理前后测量了RNA和蛋白质水平。他们发现,加入激素后hEPO的RNA水平适度上升——约2到3倍,但培养基中的蛋白水平上升更为显著,约10到20倍。这一模式表明,插入的hEPO基因确实受乳腺特异性调控元件控制,并以激素依赖的方式分泌到周围液体中,模拟了天然乳蛋白的产生。
从分泌蛋白到可用药物
产生蛋白只是挑战的一半;还需要纯化和检测。由于hEPO与GST标签融合,研究人员可以利用结合GST的专用柱进行捕获,洗去杂质,然后用特定酶切去标签以释放更纯的hEPO产物。他们通过生化测定表明,纯化的蛋白保留了可测的生物活性——说明这些编辑细胞产生的激素不仅能被检测到,而且是功能性的。尽管总体产量和比活性低于工业细胞系(如CHO细胞)实现的水平,本实验旨在作为概念验证,而非经过充分优化的生产流程。
这对未来药物意味着什么
简而言之,这项研究证明可以将人源治疗基因直接置于乳腺细胞天然乳蛋白开关的控制之下,并用驱动泌乳的相同激素来开启该基因。由此产生的hEPO可被分泌、部分纯化并证明具有功能,且都来自一个单一且定义明确的基因组位点。尽管仍需进一步改进——例如产生双拷贝均被修改的动物、改进纯化工艺并仔细分析蛋白的精细结构——这种定点策略使利用乳腺作为复杂药物的安全、可控生物反应器的想法更接近现实。
引用: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
关键词: 促红细胞生成素, CRISPR 敲入, 乳腺生物反应器, 治疗性蛋白生产, β-酪蛋白位点