Clear Sky Science · nl
Gerichte CRISPR/Cas9-knock-in van humane erytropoëtine op het β-caseïne-locus leidt tot lactogene hormoon-afhankelijke expressie in HC11 melkepitheelcellen
Melkcellen omvormen tot kleine medicijnenfabriekjes
Veel moderne geneesmiddelen zijn eiwitten die ons lichaam van nature maakt, maar ze op industriële schaal produceren is duur en technisch complex. Deze studie onderzoekt een slimme alternatieve aanpak: het herschakelen van melkproducerende cellen zodat ze een menselijk therapeutisch eiwit alleen inschakelen wanneer hormonen daartoe aanzetten, vergelijkbaar met hoe ze tijdens de lactatie van nature melkproteïnen activeren. Het werk biedt een blik op hoe toekomstige boerderijdieren mogelijk veilig en efficiënt complexe geneesmiddelen in hun melk kunnen produceren.
Doel: veilige, precieze geneesmiddelenproductie
Jarenlang hebben wetenschappers geprobeerd transgene dieren te gebruiken om geneesmiddelen te produceren, zoals humane erytropoëtine (hEPO), een hormoon dat de aanmaak van rode bloedcellen stimuleert. Eerdere pogingen vertrouwden op willekeurige invoeging van het hEPO-gen in het genoom, wat vaak tot problemen leidde: het gen kon in de verkeerde weefsels actief worden, worden geïnactiveerd of ziekte bij het dier veroorzaken. De auteurs van dit artikel wilden deze problemen oplossen door het hEPO-gen op een zeer specifieke, goed begrepen plek in het genoom te plaatsen: het gebied dat normaal gesproken de aanmaak regelt van een belangrijk melkproteïne, beta-caseïne, in de melkkliercellen.
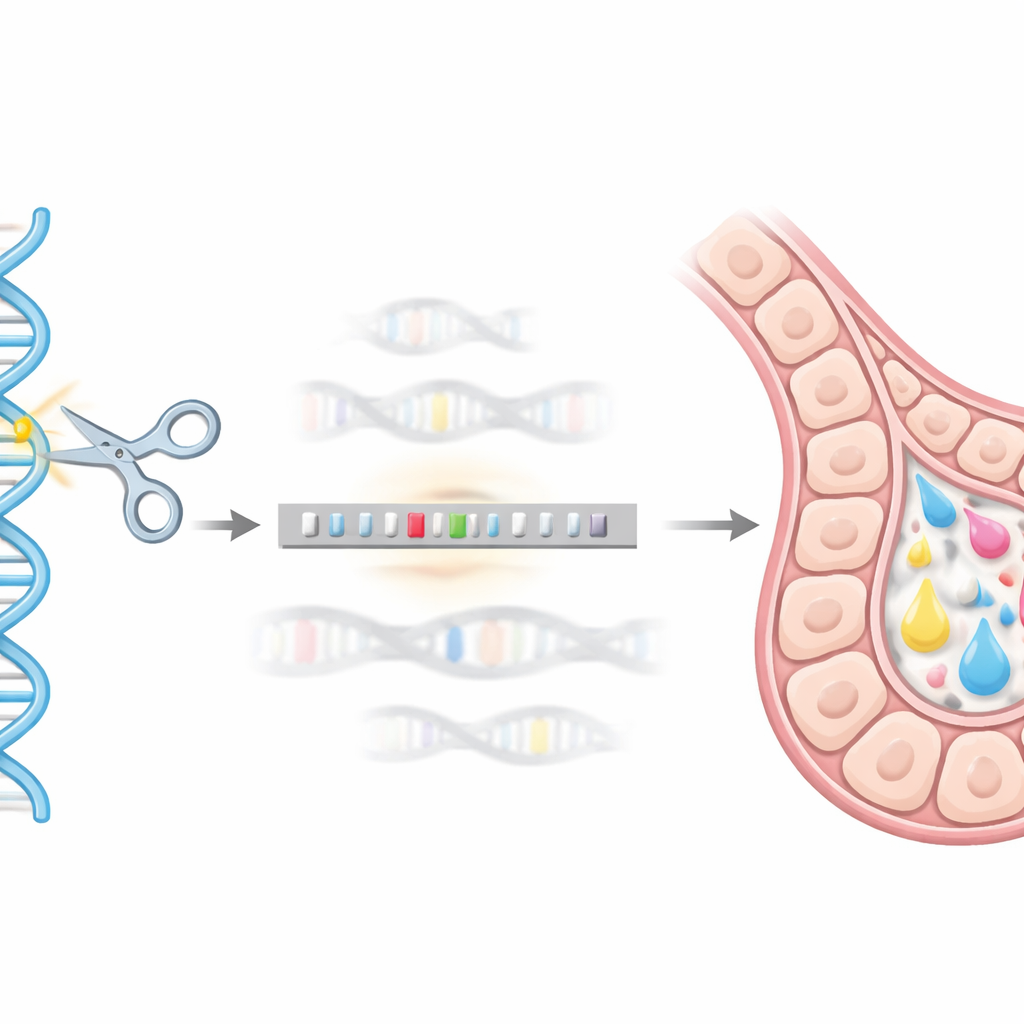
Geniereparatie als genomische "GPS"
Om dit precieze genomische adres te bereiken gebruikte het team het CRISPR/Cas9-gene-editingsysteem als een soort moleculaire GPS en schaar. Ze ontwierpen een DNA-donorconstruct dat het hEPO-gen bevatte, gekoppeld aan een hulp-tag (GST), en omringd door korte DNA-sequenties die overeenkomen met het beta-caseïne-gebied. Toen CRISPR/Cas9 de doellocatie in muismelk HC11-cellen doorsneed, kon het natuurlijke herstelmechanisme van de cel dit donorconstruct gebruiken als template en zo de hEPO-sequentie keurig in het beta-caseïne-locus invoegen. Met een reeks genetische tests (met PCR-gebaseerde methoden) isoleerden ze enkelcelligeklonen waarbij één kopie van het beta-caseïne-gen succesvol was vervangen door het hEPO-construct, waarmee stabiele “knock-in”-lijnen werden gecreëerd.
Hormoonschakelaar bootst natuurlijke melkproductie na
De onderzoekers vroegen zich vervolgens af of dit nieuwe hEPO-gen dezelfde aan/uit-regels zou volgen als het normale melkproteïnegen. HC11-cellen kunnen in een melkachtige staat worden gebracht door het toevoegen van "lactogene" hormonen, vergelijkbaar met die in een zogend dier. In de gemodificeerde klonen maten ze zowel RNA- als proteïneniveaus vóór en na hormoonbehandeling. Ze vonden dat hEPO-RNA-niveaus bescheiden stegen — ongeveer twee- tot driemaal — wanneer hormonen werden toegevoegd, maar dat de eiwitniveaus in het kweekmedium veel sterker toenamen, grofweg 10- tot 20-voudig. Dit patroon laat zien dat het ingevoegde hEPO-gen inderdaad onder controle staat van de mammary-specifieke regelende elementen en dat het, hormonaal afhankelijk, in de omliggende vloeistof wordt uitgescheiden, wat natuurlijke melkproteïneproductie nabootst.
Van uitgescheiden eiwit naar bruikbaar geneesmiddel
Een eiwit produceren is slechts de helft van de uitdaging; het moet ook gezuiverd en getest worden. Omdat het hEPO was gefuseerd aan een GST-tag, konden de onderzoekers het opvangen op een speciale kolom die GST bindt, verontreinigingen wegwassen en vervolgens een specifiek enzym gebruiken om de tag af te knippen en een schoner hEPO-product vrij te geven. Met biochemische assays lieten ze zien dat het gezuiverde eiwit meetbare biologische activiteit behield — wat aangeeft dat het hormoon gemaakt door deze gewijzigde cellen niet alleen aanwezig is, maar ook functioneel. Hoewel de totale opbrengst en de specifieke activiteit lager waren dan wat in industriële cellijnen zoals CHO-cellen wordt bereikt, was dit experiment bedoeld als proof of concept en niet als een volledig geoptimaliseerd productieproces.
Wat dit kan betekenen voor toekomstige geneesmiddelen
In eenvoudige bewoordingen toont deze studie aan dat het mogelijk is een menselijk therapeutisch gen direct onder controle te plaatsen van een natuurlijke melkproteïne-schakelaar in melkkliercellen en dat dat gen kan worden ingeschakeld met dezelfde hormonen die lactatie aansturen. Het resulterende hEPO kan worden uitgescheiden, gedeeltelijk gezuiverd en aangetoond functioneel te zijn, allemaal vanuit één goed gedefinieerde genomische locatie. Hoewel verdere verbeteringen nodig zijn — zoals het genereren van dieren met beide genkopieën aangepast, betere zuiveringsmethoden en een zorgvuldige analyse van de fijne structuur van het eiwit — brengt deze gerichte strategie het idee om de melkklier als een veilige, beheersbare bioreactor voor complexe geneesmiddelen te gebruiken dichterbij de realiteit.
Bronvermelding: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Trefwoorden: erytropoëtine, CRISPR knock-in, bioreactor in melkklier, productie van therapeutische eiwitten, beta-caseïne-locus