Clear Sky Science · ru
Целевая интеграция человеческого эритропоэтина с помощью CRISPR/Cas9 в локус бета-казеина приводит к гормонозависимой экспрессии в эпителиальных клетках молочной железы HC11
Превращение молочных клеток в крошечные фабрики лекарств
Многие современные лекарства представляют собой белки, которые наш организм естественно синтезирует, но их промышленное производство дорого и технологически сложно. В этом исследовании рассматривается изящная альтернатива: перепрограммирование клеток, продуцирующих молоко, так, чтобы они включали человеческий терапевтический белок только при гормональном сигнале, подобно тому, как они естественно активируют молочные белки во время лактации. Работа демонстрирует, как в будущем сельскохозяйственные животные могут безопасно и эффективно синтезировать сложные препараты в молоке.
Цель — безопасное и точное производство лекарств
В течение многих лет ученые пытались использовать трансгенных животных для получения лекарств, таких как человеческий эритропоэтин (hEPO) — гормон, стимулирующий образование эритроцитов. Ранние попытки опирались на случайную вставку гена hEPO в геном, что часто приводило к проблемам: ген мог экспрессироваться в неправильных тканях, быть заглушенным или вызывать заболевания у животного. Авторы этой работы решили устранить эти проблемы, поместив ген hEPO в очень конкретное, хорошо изученное место генома: регион, который обычно контролирует крупный молочный белок бета-казеин в эпителиальных клетках молочной железы.
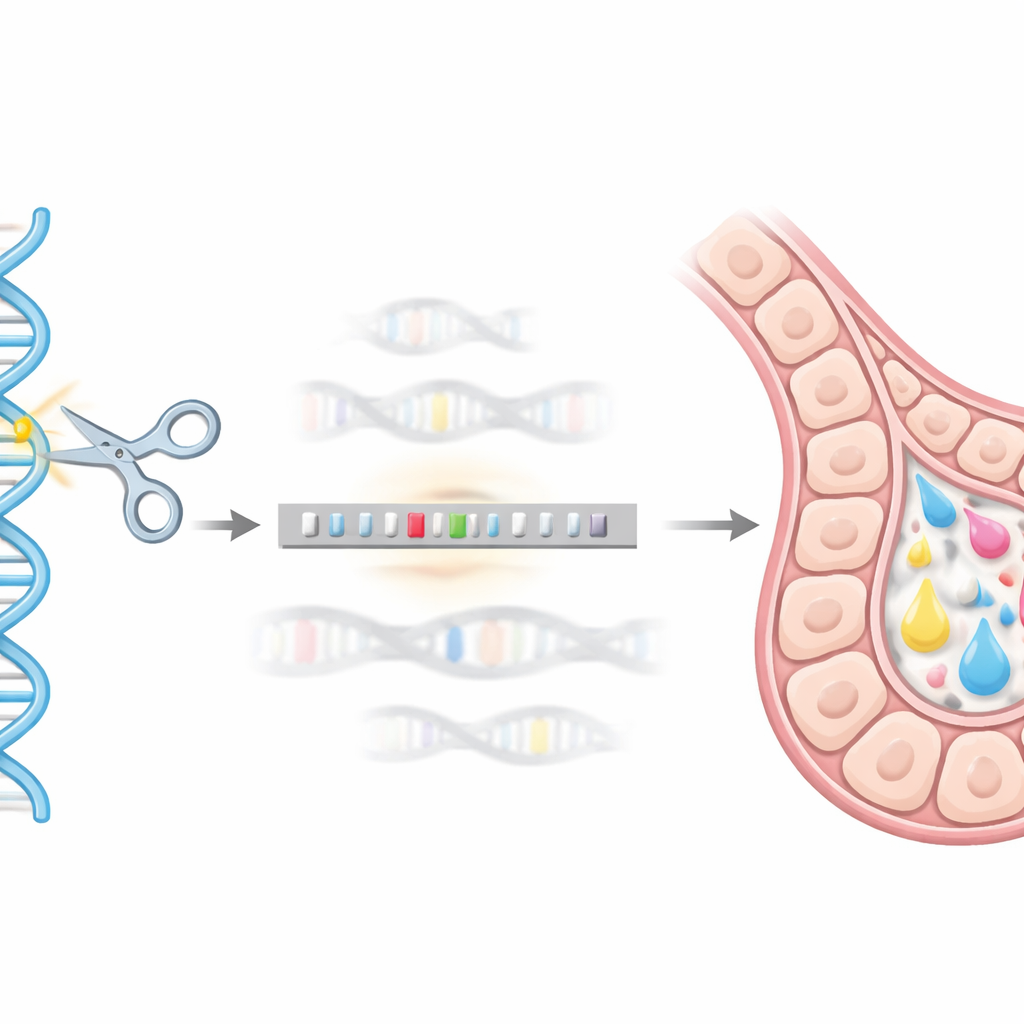
Геномный «GPS»: использование редактирования генов
Чтобы попасть в эту точную геномную «адресную» область, команда использовала систему редактирования CRISPR/Cas9 как молекулярный GPS и ножницы. Они сконструировали донорную ДНК, несущую ген hEPO, связанную с вспомогательным тегом (GST), и окружили её короткими участками ДНК, соответствующими региону бета-казеина. Когда CRISPR/Cas9 разрезал целевое место в клетках молочной железы мыши HC11, собственные репарационные механизмы клетки могли использовать этот донор как шаблон и аккуратно вставить последовательность hEPO в локус бета-казеина. Серией генетических тестов (на основе ПЦР) они выделили клоны из одной клетки, в которых одна копия гена бета-казеина была успешно заменена конструкцией hEPO, создав стабильные линии с «кик-ин» интеграцией.
Гормональный переключатель имитирует естественную продукцию молока
Затем исследователи проверили, будет ли новый ген hEPO подчиняться тем же правилам включения-выключения, что и нормальный ген молочного белка. Клетки HC11 можно «сдвинуть» в состояние, напоминающее лактацию, добавляя лактогенные гормоны, подобные тем, что действуют у кормящих животных. В созданных клонов команда измеряла уровни иРНК и белка до и после гормональной стимуляции. Они обнаружили, что уровни hEPO иРНК умеренно возрастали — примерно в 2–3 раза — при добавлении гормонов, тогда как концентрация белка в среде культуры увеличивалась значительно больше, примерно в 10–20 раз. Такая картина указывает, что вставленный ген hEPO действительно находится под контролем молярно-специфических регуляторных элементов и секретируется в окружную среду в гормонозависимом режиме, имитируя естественную продукцию молочных белков.
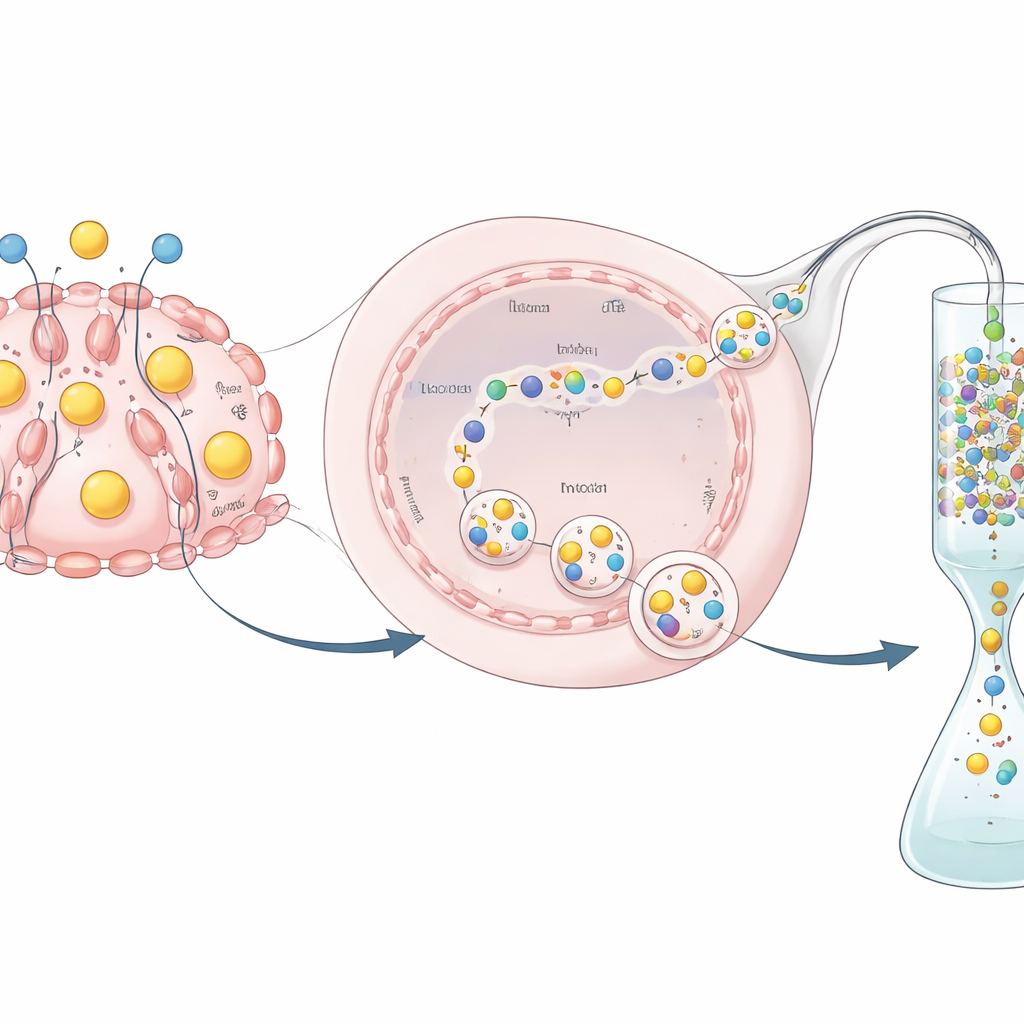
От секретируемого белка к пригодному лекарству
Производство белка — это лишь половина задачи; его нужно также очистить и протестировать. Поскольку hEPO был связан с GST-тегом, исследователи могли захватить его на специальной колонке, связывающей GST, смыть примеси и затем использовать специфический фермент, чтобы отрезать тег и получить более чистый продукт hEPO. С помощью биохимических тестов они показали, что очищенный белок сохраняет измеримую биологическую активность — то есть гормон, произведённый этими отредактированными клетками, не просто присутствует, но и функционален. Хотя общий выход и удельная активность были ниже, чем у промышленных клеточных линий, таких как клетки CHO, этот эксперимент задуман как доказательство концепции, а не как полностью отлаженный производственный процесс.
Что это может значить для будущих лекарств
Проще говоря, исследование демонстрирует возможность разместить человеческий терапевтический ген непосредственно под контролем природного молочного переключателя в клетках молочной железы и включать этот ген теми же гормонами, которые запускают лактацию. Получаемый hEPO может секретироваться, частично очищаться и демонстрировать активность, при этом всё происходит из одного, чётко определённого геномного места. Несмотря на то, что необходимы дальнейшие улучшения — например, получение животных с модифицированными обеими копиями гена, усовершенствование очистки и тщательное изучение тонкой структуры белка — такая целевая стратегия приближает идею использования молочной железы как безопасного и управляемого биореактора для сложных лекарственных препаратов к реализации.
Цитирование: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Ключевые слова: эритропоэтин, CRISPR-кированная интеграция, биореактор молочной железы, производство терапевтических белков, локус бета-казеина