Clear Sky Science · fr
Insertion ciblée médiée par CRISPR/Cas9 de l’érythropoïétine humaine au locus de la β-caseine aboutit à une expression répondant aux hormones lactogènes dans des cellules épithéliales mammaires HC11
Transformer des cellules lactées en petites usines à médicaments
Beaucoup de médicaments modernes sont des protéines que notre propre organisme produit naturellement, mais les fabriquer à grande échelle en usine est coûteux et techniquement exigeant. Cette étude explore une alternative ingénieuse : reprogrammer des cellules productrices de lait pour qu’elles activent une protéine thérapeutique humaine uniquement lorsqu’elles sont déclenchées par des hormones, de la même manière qu’elles activent naturellement les protéines du lait pendant la lactation. Le travail donne un aperçu de la façon dont de futurs animaux d’élevage pourraient produire des médicaments complexes dans leur lait de manière sûre et efficace.
Viser une production de médicaments sûre et précise
Pendant des années, les scientifiques ont tenté d’utiliser des animaux transgéniques pour produire des médicaments tels que l’érythropoïétine humaine (hEPO), une hormone qui aide l’organisme à fabriquer des globules rouges. Les tentatives antérieures reposaient sur l’insertion aléatoire du gène hEPO dans le génome, ce qui entraînait souvent plusieurs problèmes : le gène pouvait être exprimé dans des tissus inappropriés, être silencé ou provoquer des maladies chez l’animal. Les auteurs de cet article ont cherché à résoudre ces problèmes en plaçant le gène hEPO dans un emplacement très précis et bien caractérisé du génome : la région qui contrôle normalement une protéine majeure du lait appelée bêta-caseine dans les cellules mammaires (productrices de lait).
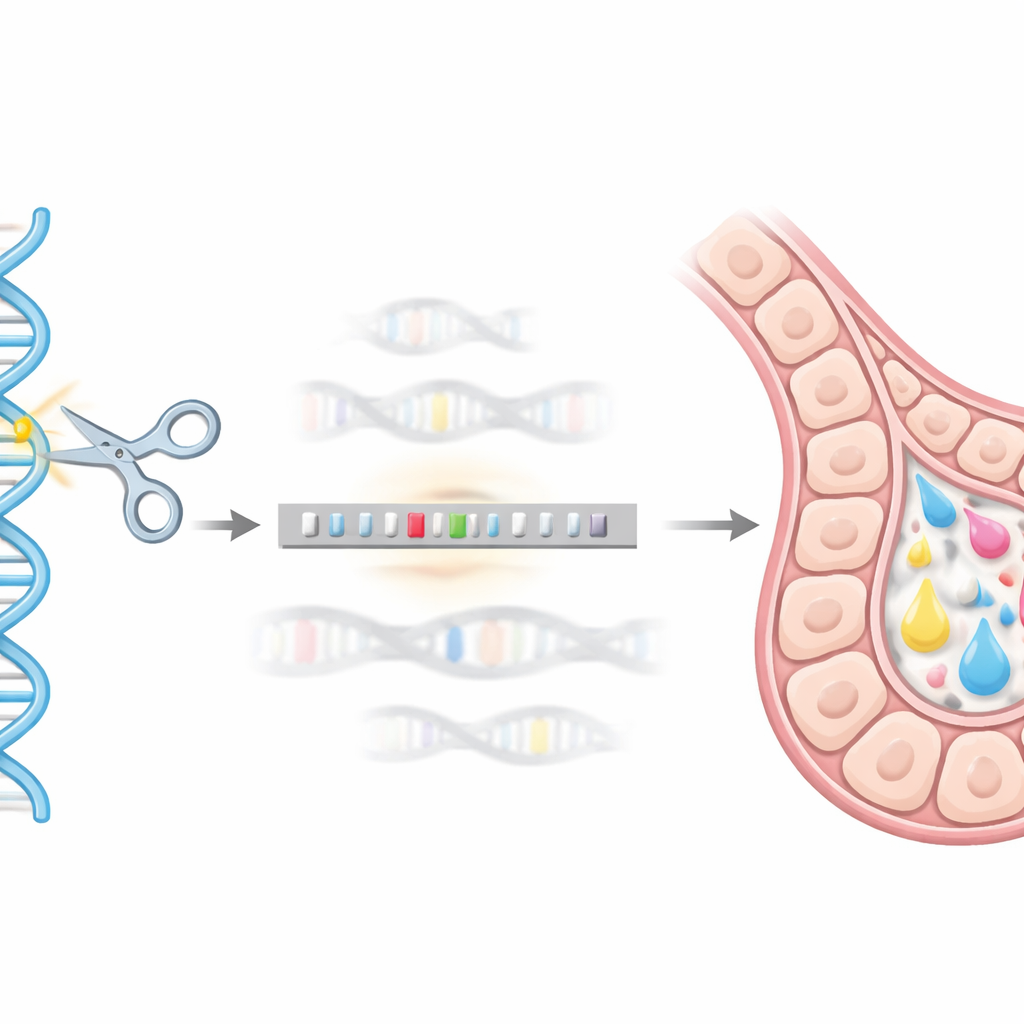
Utiliser l’édition génomique comme un « GPS » moléculaire
Pour atteindre cette adresse génomique précise, l’équipe a utilisé le système d’édition CRISPR/Cas9 comme une sorte de GPS moléculaire et de ciseaux. Ils ont conçu un donneur d’ADN portant le gène hEPO fusionné à une étiquette d’assistance (GST) et encadré par de courtes séquences d’ADN correspondant à la région de la bêta-caseine. Lorsque CRISPR/Cas9 a coupé le site cible dans des cellules mammaires de souris HC11, la machinerie de réparation naturelle de la cellule a pu utiliser ce donneur comme matrice, insérant proprement la séquence hEPO au locus de la bêta-caseine. Par une série de tests génétiques (méthodes basées sur la PCR), ils ont isolé des clones monocellulaires dans lesquels une copie du gène de la bêta-caseine avait été remplacée par succès par le construct hEPO, créant des lignées « knock-in » stables.
Un interrupteur hormonal qui mime la production naturelle de lait
Les chercheurs ont ensuite cherché à savoir si ce nouveau gène hEPO suivrait les mêmes règles d’activation/désactivation que le gène de la protéine du lait normale. Les cellules HC11 peuvent être poussées vers un état similaire à la production de lait en ajoutant des hormones « lactogènes », similaires à celles qui agissent chez un animal allaitant. Dans les clones modifiés, l’équipe a mesuré les niveaux d’ARN et de protéine avant et après le traitement hormonal. Ils ont constaté que les niveaux d’ARN de hEPO augmentaient modérément — d’environ deux à trois fois — lorsque les hormones étaient ajoutées, mais que les niveaux de protéine dans le milieu de culture augmentaient beaucoup plus fortement, d’environ 10 à 20 fois. Ce schéma montre que le gène hEPO inséré est bien sous le contrôle des éléments régulateurs spécifiques à la glande mammaire et qu’il est sécrété dans le fluide environnant de façon dépendante des hormones, imitant la production naturelle de protéines du lait.
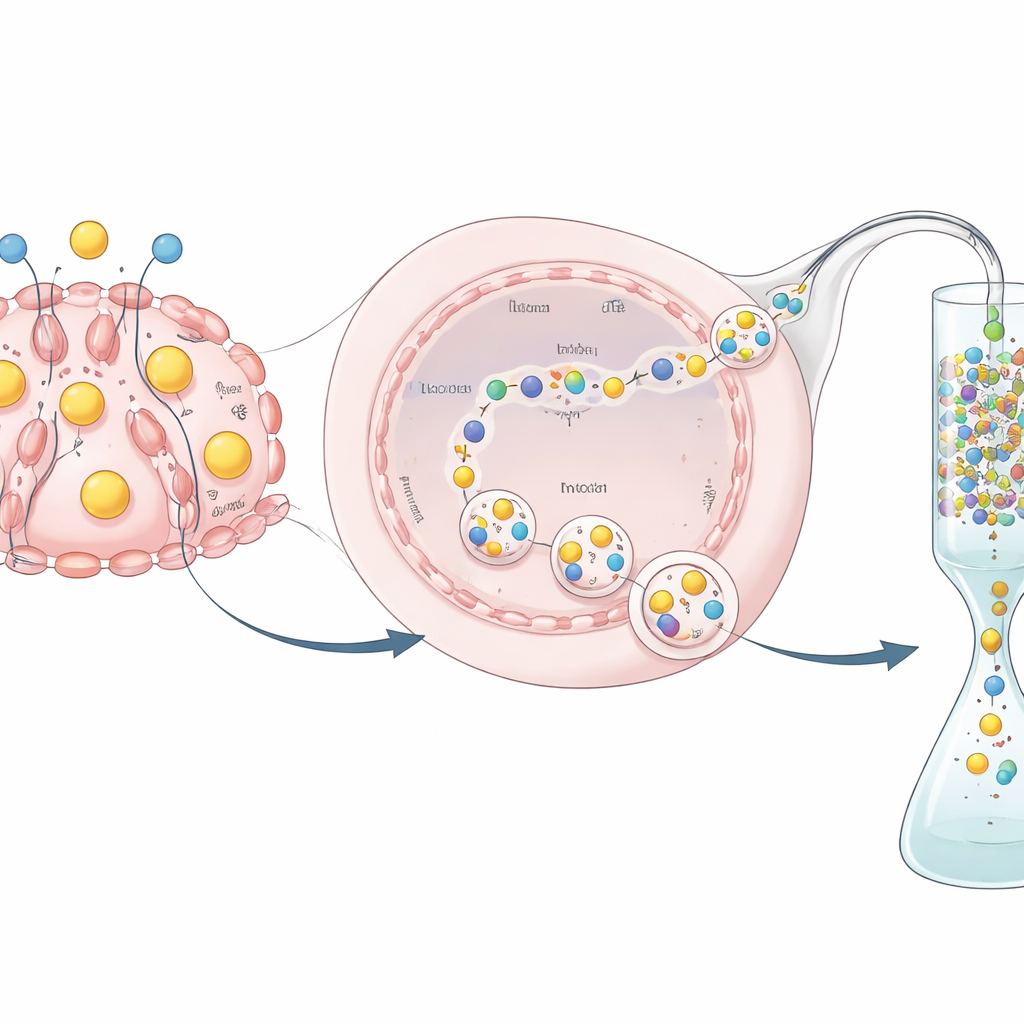
De la protéine sécrétée au médicament utilisable
Produire une protéine n’est qu’une partie du défi ; elle doit aussi être purifiée et testée. Comme le hEPO était fusionné à une étiquette GST, les chercheurs ont pu le capturer sur une colonne spécifique qui lie le GST, éliminer les impuretés par lavage, puis utiliser une enzyme spécifique pour couper l’étiquette et libérer un produit hEPO plus pur. Ils ont montré, à l’aide d’essais biochimiques, que la protéine purifiée conservait une activité biologique mesurable — indiquant que l’hormone produite par ces cellules modifiées est non seulement présente mais fonctionnelle. Bien que le rendement global et l’activité spécifique aient été inférieurs à ceux obtenus dans des lignées cellulaires industrielles telles que les cellules CHO, cette expérience était conçue comme une preuve de concept plutôt que comme un procédé de production entièrement optimisé.
Ce que cela pourrait signifier pour les médicaments de demain
En termes simples, cette étude démontre qu’il est possible de placer un gène thérapeutique humain directement sous le contrôle d’un interrupteur naturel de protéine du lait dans des cellules mammaires, et d’activer ce gène avec les mêmes hormones qui régulent la lactation. Le hEPO résultant peut être sécrété, partiellement purifié et montré comme actif, le tout à partir d’un emplacement génomique unique et bien défini. Bien que des améliorations supplémentaires soient nécessaires — comme générer des animaux avec les deux copies du gène modifiées, améliorer la purification et analyser soigneusement la structure fine de la protéine — cette stratégie ciblée rapproche l’idée d’utiliser la glande mammaire comme bioreacteur sûr et contrôlable pour des médicaments complexes d’une réalité potentielle.
Citation: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Mots-clés: érythropoïétine, insertion CRISPR, bioreacteur mammaire, production de protéines thérapeutiques, locus de la bêta-caseine