Clear Sky Science · it
Inserimento mirato mediato da CRISPR/Cas9 dell’eritropoietina umana nel locus della β-caseina determina un’espressione responsiva agli ormoni lattogenici nelle cellule epiteliali mammarie HC11
Trasformare le cellule del latte in piccole fabbriche di medicina
Molti farmaci moderni sono proteine che il nostro organismo produce naturalmente, ma produrle su scala industriale è costoso e tecnicamente complesso. Questo studio esplora un’alternativa intelligente: riprogrammare le cellule produttrici di latte in modo che attivino una proteina terapeutica umana solo quando stimolate da ormoni, proprio come fanno naturalmente con le proteine del latte durante la lattazione. Il lavoro offre uno sguardo su come, in futuro, gli animali da allevamento potrebbero produrre in modo sicuro ed efficiente farmaci complessi nel loro latte.
Obiettivo: produzione di farmaci sicura e precisa
Per anni i ricercatori hanno tentato di usare animali transgenici per produrre medicinali come l’eritropoietina umana (hEPO), un ormone che stimola la formazione dei globuli rossi. I tentativi precedenti si basavano sull’inserimento casuale del gene hEPO nel genoma, con problemi frequenti: il gene poteva attivarsi nei tessuti sbagliati, essere silenziato o causare patologie nell’animale. Gli autori di questo lavoro hanno cercato di superare questi limiti inserendo il gene hEPO in un punto molto preciso e ben caratterizzato del genoma: la regione che normalmente regola una proteina del latte principale chiamata beta-caseina nelle cellule mammarie (produttrici di latte).
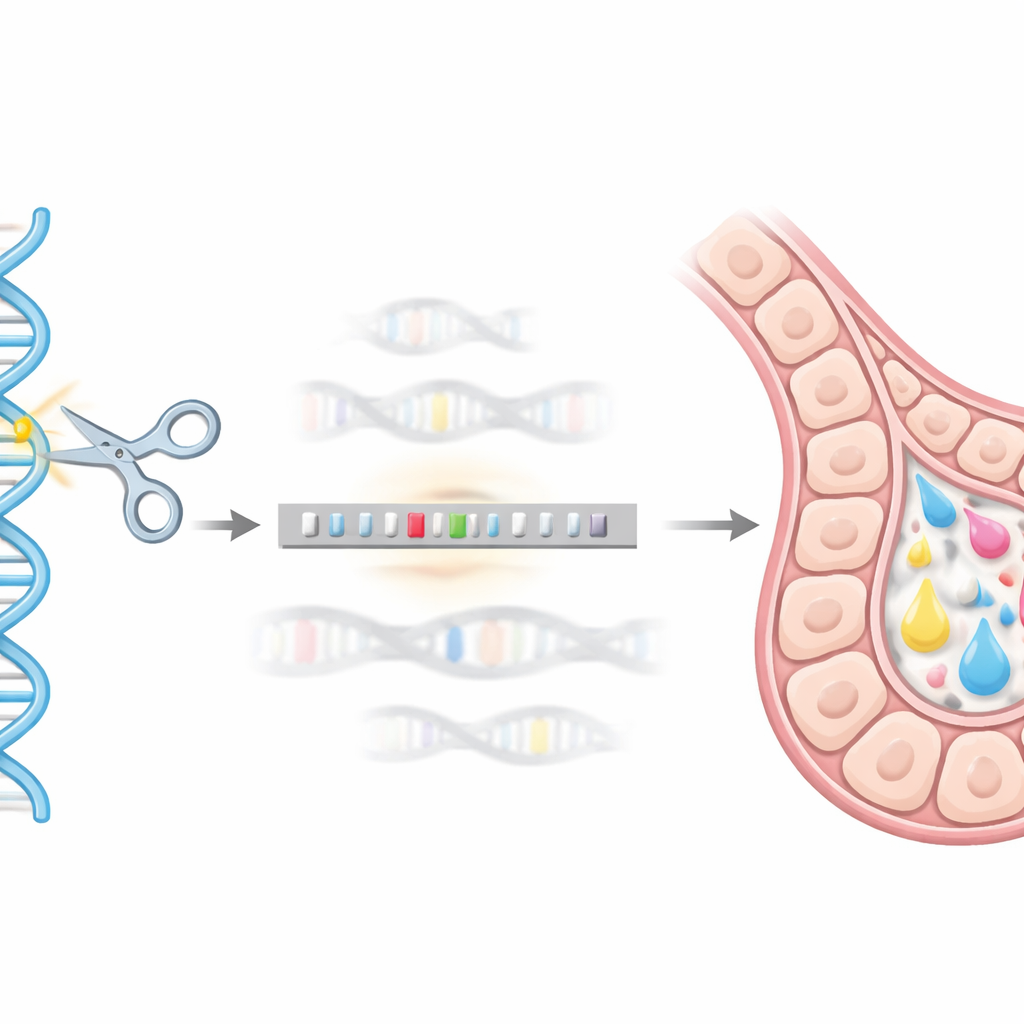
Usare l’editing genetico come un “GPS” genomico
Per raggiungere questo indirizzo genomico preciso, il team ha usato il sistema di editing CRISPR/Cas9 come una sorta di GPS molecolare e cesoie. Hanno progettato un costrutto donatore di DNA contenente il gene hEPO fuso a un tag ausiliario (GST) e lo hanno circondato con brevi sequenze di DNA corrispondenti alla regione della beta-caseina. Quando CRISPR/Cas9 ha tagliato il sito bersaglio nelle cellule mammarie murine HC11, la macchina riparativa naturale della cellula ha potuto usare questo costrutto donatore come stampo, inserendo ordinatamente la sequenza hEPO nel locus della beta-caseina. Tramite una serie di test genetici (basati su PCR), hanno isolato cloni derivati da singole cellule in cui una copia del gene beta-caseina era stata sostituita con successo dal costrutto hEPO, creando linee “knock-in” stabili.
Un interruttore ormonale che imita la produzione naturale di latte
I ricercatori hanno quindi verificato se questo nuovo gene hEPO rispettasse le stesse regole di accensione-spegnimento del gene delle proteine del latte. Le cellule HC11 possono essere spinte in uno stato simile al latte aggiungendo ormoni «lattogenici», simili a quelli che agiscono in un animale che allatta. Nei cloni ingegnerizzati, il team ha misurato i livelli di RNA e di proteina prima e dopo il trattamento ormonale. Hanno riscontrato che i livelli di RNA di hEPO aumentavano in modo moderato—circa due-tre volte—con l’aggiunta di ormoni, mentre i livelli proteici nel mezzo di coltura sono aumentati in modo molto più marcato, circa 10-20 volte. Questo schema indica che il gene hEPO inserito è effettivamente sotto il controllo degli elementi regolatori specifici della mammella ed è secreto nel fluido circostante in modo dipendente dagli ormoni, imitando la produzione naturale di proteine del latte.
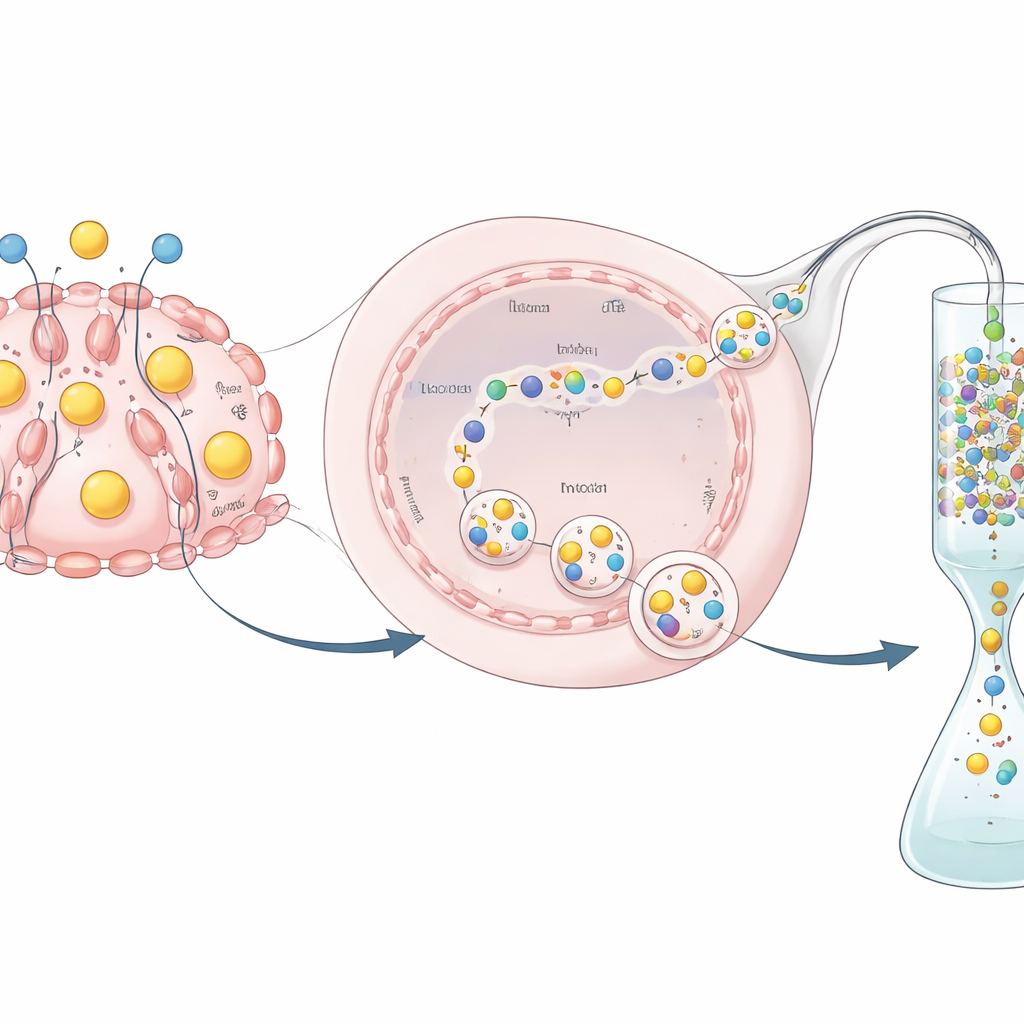
Dalla proteina secreta al medicinale utilizzabile
Produrre una proteina è solo metà della sfida; occorre anche purificarla e testarla. Poiché l’hEPO era fusa a un tag GST, i ricercatori hanno potuto catturarla su una colonna specifica che lega il GST, lavare via le impurità e poi usare un enzima specifico per rimuovere il tag e ottenere un prodotto hEPO più puro. Hanno dimostrato, mediante saggi biochimici, che la proteina purificata manteneva un’attività biologica misurabile—indicando che l’ormone prodotto da queste cellule editate non è solo presente ma funzionale. Sebbene la resa complessiva e l’attività specifica fossero inferiori rispetto a quelle ottenute in linee industriali come le cellule CHO, questo esperimento era pensato come prova di principio più che come un processo produttivo pienamente ottimizzato.
Implicazioni per i farmaci del futuro
In termini semplici, questo studio dimostra che è possibile collocare un gene terapeutico umano direttamente sotto il controllo di un interruttore naturale per le proteine del latte nelle cellule mammarie e attivare quel gene con gli stessi ormoni che regolano la lattazione. L’hEPO risultante può essere secreta, parzialmente purificata e dimostrata funzionante, il tutto da un singolo locus genomico ben definito. Pur richiedendo ulteriori miglioramenti—come ottenere animali con entrambe le copie del gene modificate, perfezionare la purificazione e analizzare attentamente la struttura fine della proteina—questa strategia mirata avvicina l’idea di usare la ghiandola mammaria come bioreattore sicuro e controllabile per farmaci complessi a una possibile applicazione pratica.
Citazione: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Parole chiave: eritropoietina, inserimento CRISPR, bioreattore ghiandolare mammario, produzione di proteine terapeutiche, locus della beta-caseina