Clear Sky Science · pt
Inserção direcionada mediada por CRISPR/Cas9 de eritropoietina humana no locus da β-caseína resulta em expressão responsiva a hormônios lactogênicos em células epiteliais mamárias HC11
Transformando células do leite em pequenas fábricas de remédios
Muitos medicamentos modernos são proteínas que nossos próprios corpos produzem naturalmente, mas fabricá-las em escala industrial é caro e exige grande complexidade técnica. Este estudo explora uma alternativa engenhosa: reprogramar células produtoras de leite para que elas ativem uma proteína terapêutica humana somente quando estimuladas por hormônios, tal como naturalmente ativam proteínas do leite durante a lactação. O trabalho oferece uma visão de como no futuro animais de criação poderiam produzir medicamentos complexos no leite de forma segura e eficiente.
Buscando produção de fármacos precisa e segura
Por anos, cientistas tentaram usar animais transgênicos para produzir medicamentos como a eritropoietina humana (hEPO), um hormônio que estimula a formação de glóbulos vermelhos. Tentativas anteriores dependiam da inserção aleatória do gene de hEPO no genoma, o que frequentemente causava problemas: o gene podia ser expresso em tecidos inadequados, ser silenciado ou ocasionar doenças no animal. Os autores deste artigo deram-se à tarefa de resolver essas questões colocando o gene de hEPO em um ponto muito específico e bem caracterizado do genoma: a região que normalmente controla uma proteína majoritária do leite chamada beta-caseína em células mamárias (produtoras de leite).
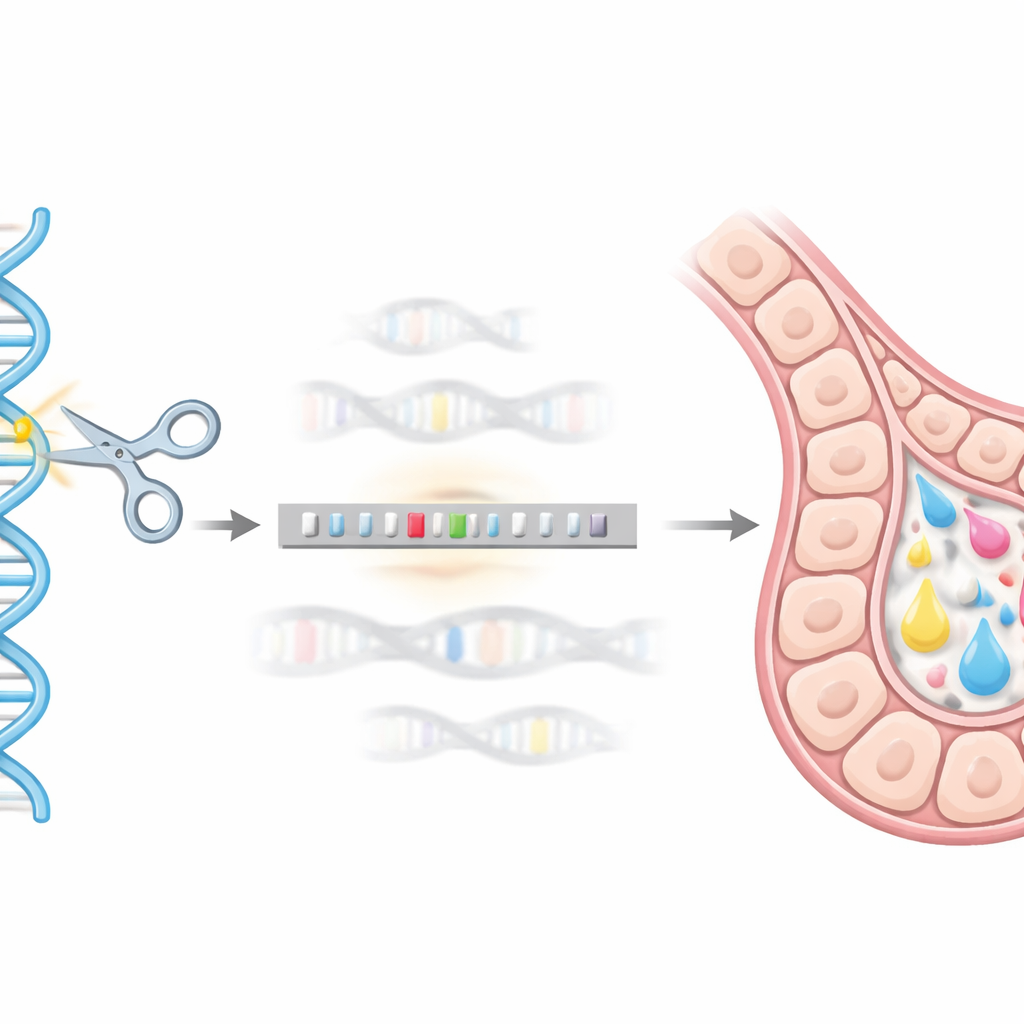
Usando edição gênica como um “GPS” genômico
Para atingir esse endereço genômico preciso, a equipe utilizou o sistema de edição gênica CRISPR/Cas9 como uma espécie de GPS molecular e tesoura. Projetaram um construto doador de DNA contendo o gene de hEPO fundido a uma etiqueta auxiliar (GST) e flanqueado por trechos curtos de DNA que correspondem à região da beta-caseína. Quando o CRISPR/Cas9 cortou o sítio alvo em células mamárias de camundongo HC11, a maquinaria natural de reparo da célula pôde usar esse construto doador como molde, inserindo ordenadamente a sequência de hEPO no locus da beta-caseína. Por meio de uma série de testes genéticos (usando métodos baseados em PCR), isolaram clones de célula única nos quais uma cópia do gene da beta-caseína foi substituída com sucesso pelo construto de hEPO, criando linhagens estáveis de “knock-in”.
Interruptor hormonal imita produção natural de leite
Os pesquisadores então perguntaram se esse novo gene de hEPO seguiria as mesmas regras de ligar/desligar do gene normal de proteína do leite. Células HC11 podem ser induzidas a um estado semelhante ao de produção de leite pela adição de hormônios “lactogênicos”, semelhantes aos que atuam em um animal em lactação. Nos clones editados, a equipe mediu níveis de RNA e proteína antes e depois do tratamento hormonal. Eles observaram que os níveis de RNA de hEPO aumentaram modestamente — cerca de duas a três vezes — quando os hormônios foram adicionados, mas os níveis de proteína no meio de cultura subiram de forma muito mais acentuada, aproximadamente de 10 a 20 vezes. Esse padrão indica que o gene de hEPO inserido está, de fato, sob o controle dos elementos regulatórios específicos da mama e é secretado para o fluido circundante de maneira dependente de hormônio, imitando a produção natural de proteínas do leite.
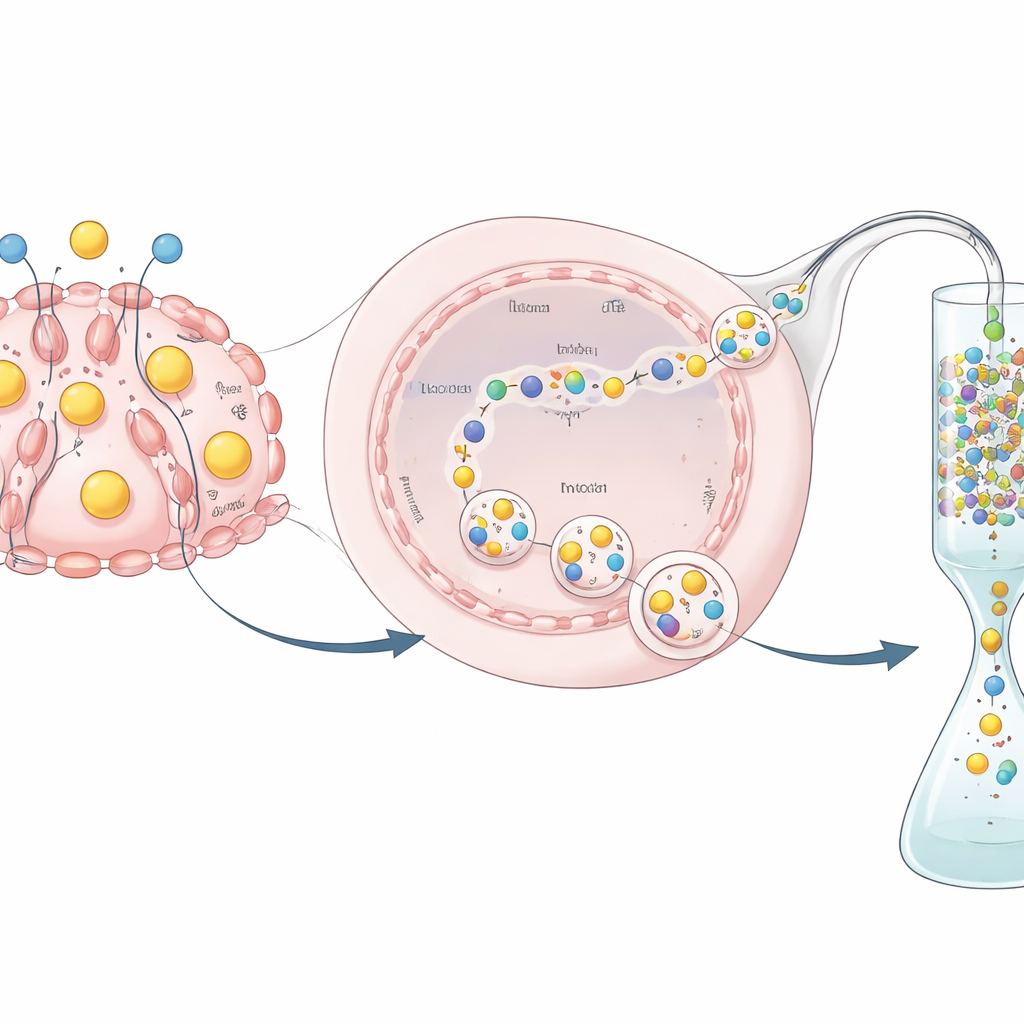
Da proteína secretada ao medicamento utilizável
Produzir uma proteína é apenas metade do desafio; ela também precisa ser purificada e testada. Como o hEPO foi fundido a uma etiqueta GST, os pesquisadores puderam capturá-lo em uma coluna especializada que liga GST, lavar as impurezas e então usar uma enzima específica para remover a etiqueta e liberar um produto de hEPO mais puro. Eles demonstraram, por ensaios bioquímicos, que a proteína purificada manteve atividade biológica mensurável — indicando que o hormônio produzido por essas células editadas não está apenas presente, mas funcional. Embora o rendimento geral e a atividade específica tenham sido menores do que os alcançados em linhas celulares industriais como células CHO, este experimento foi concebido como prova de conceito e não como um processo de produção totalmente otimizado.
O que isso pode significar para medicamentos futuros
Em termos simples, este estudo demonstra que é possível posicionar um gene terapêutico humano diretamente sob o controle de um interruptor natural de proteína do leite em células mamárias, e ativar esse gene com os mesmos hormônios que impulsionam a lactação. O hEPO resultante pode ser secretado, parcialmente purificado e demonstrado como funcional, tudo a partir de um único local genômico bem definido. Embora sejam necessárias melhorias adicionais — como gerar animais com ambas as cópias do gene modificadas, aperfeiçoar a purificação e analisar cuidadosamente a estrutura fina da proteína — essa estratégia direcionada aproxima a ideia de usar a glândula mamária como um biorreator seguro e controlável para medicamentos complexos da realidade.
Citação: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Palavras-chave: eritropoietina, inserção por CRISPR, biorreator de glândula mamária, produção de proteínas terapêuticas, locus da beta-caseína