Clear Sky Science · sv
CRISPR/Cas9-medierad riktad insättning av humant erytropoetin i β-casein-lokuset ger laktogen hormonresponsiv uttryck i HC11 bröstkörtelceller
Förvandla mjölkceller till små läkemedelsfabriker
Många moderna läkemedel är proteiner som våra kroppar naturligt framställer, men att producera dem i stor skala i fabriker är dyrt och tekniskt krävande. Denna studie utforskar ett smart alternativ: att omprogrammera mjölkproducerande celler så att de kan sätta på ett humant terapeutiskt protein först när de stimuleras av hormoner, på samma sätt som de naturligt aktiverar mjölkproteiner under laktation. Arbetet visar hur framtida lantbruksdjur på ett säkert och effektivt sätt skulle kunna tillverka komplexa läkemedel i sin mjölk.
Målsättning: säker och precis läkemedelsproduktion
I åratal har forskare försökt använda transgena djur för att producera läkemedel som humant erytropoetin (hEPO), ett hormon som hjälper kroppen att bilda röda blodkroppar. Tidigare försök förlitade sig på att slumpmässigt infoga hEPO-genen i genomet, vilket ofta ledde till problem: genen kunde aktiveras i fel vävnader, tystas ner eller orsaka sjukdom hos djuret. Författarna till denna artikel ville lösa dessa problem genom att placera hEPO-genen på en mycket specifik och välkänd plats i genomet: regionen som normalt styr ett stort mjölkprotein kallat beta-casein i bröstkörtelceller.
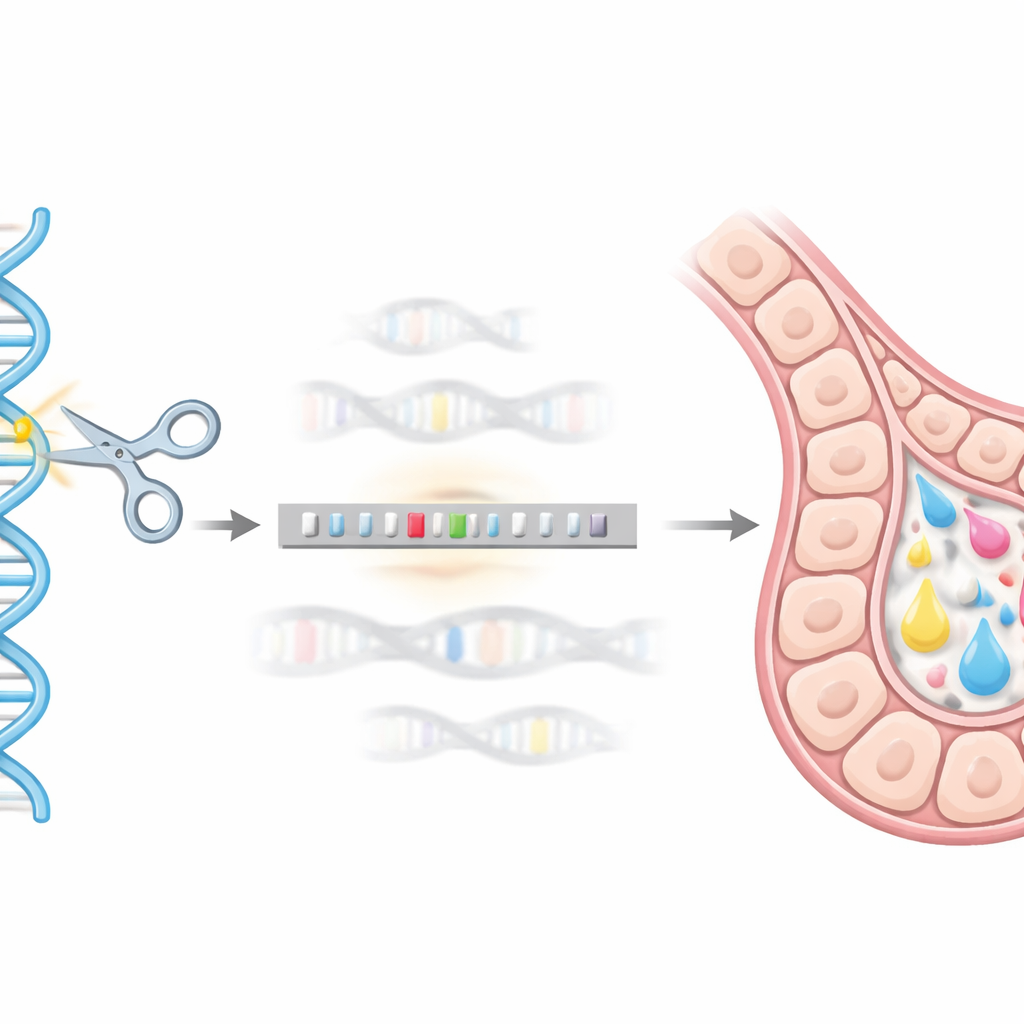
Använda genredigering som en genomisk ”GPS”
För att träffa denna precisa genomiska adress använde teamet CRISPR/Cas9-genredigeringssystemet som en slags molekylär GPS och sax. De designade en DNA-donorkonstruktion som bar hEPO-genen förenad med en hjälpmärkning (GST) och flankeras av korta DNA-sekvenser som matchar beta-casein-regionen. När CRISPR/Cas9 klippte målet i musens bröstkörtelceller (HC11) kunde cellens egna reparationsmaskineri använda denna donorkonstruktion som mall och på ett prydligt sätt infoga hEPO-sekvensen i beta-casein-lokuset. Genom en serie genetiska tester (med PCR-baserade metoder) isolerade de enkelcells-kloner där en kopia av beta-casein-genen framgångsrikt ersatts av hEPO-konstruktionen och skapade stabila ”knock-in”-linjer.
Hormonswitch som imiterar naturlig mjölkproduktion
Forskarna undersökte sedan om den nya hEPO-genen skulle följa samma av/på-regler som den normala mjölkproteingenen. HC11-celler kan pressas in i ett mjökliknande tillstånd genom att tillsätta ”laktogena” hormoner, liknande de som verkar i ett digivande djur. I de manipulerade klonerna mättes både RNA- och proteinnivåer före och efter hormonbehandling. De fann att hEPO-RNA ökade måttligt—ungefär två till tre gånger—efter hormontillsats, medan proteinnivåerna i odlingsmediet steg mycket mer dramatiskt, ungefär 10- till 20-faldigt. Detta mönster visar att den införda hEPO-genen verkligen står under kontroll av de bröstkörtelspecifika regulatoriska elementen och utsöndras i omgivande vätska på ett hormonberoende sätt, vilket imiterar naturlig mjölkproteinsproduktion.
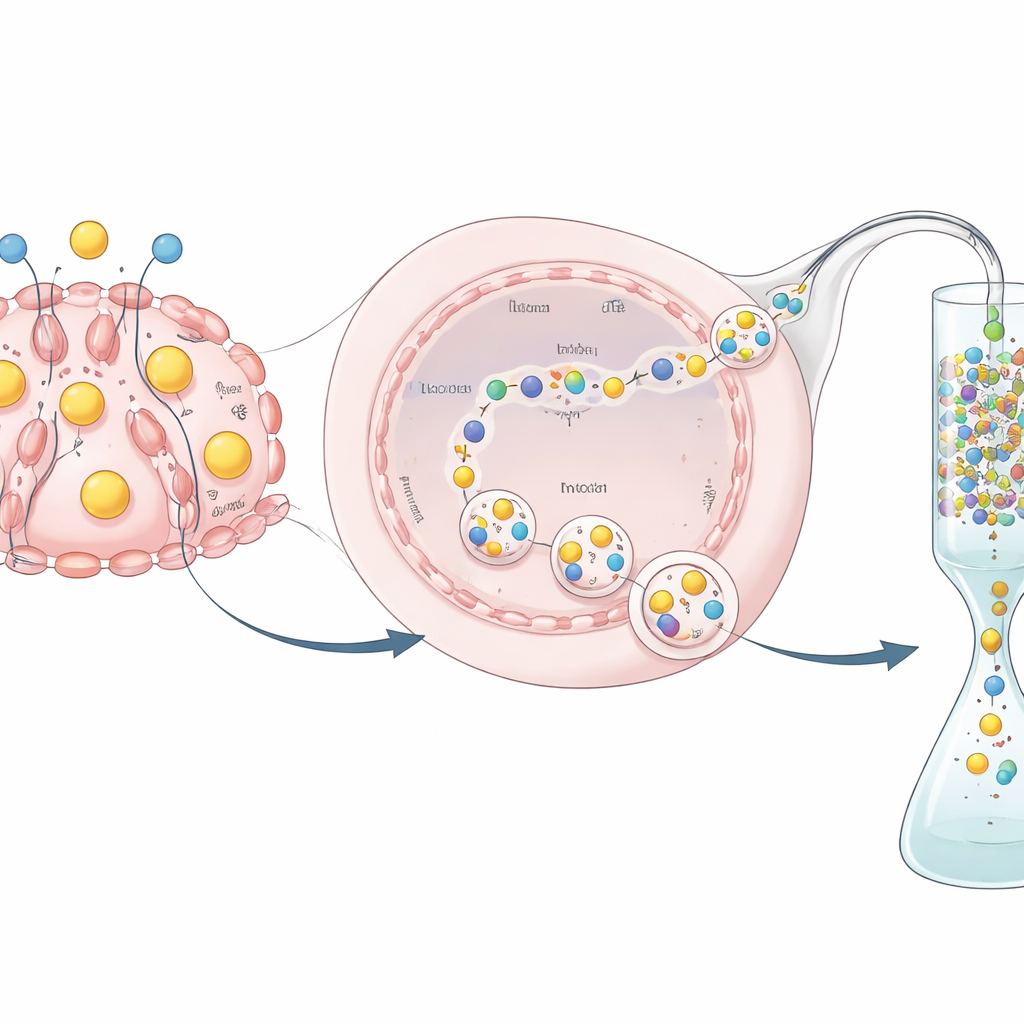
Från utsöndrat protein till användbart läkemedel
Att producera ett protein är bara halva utmaningen; det måste också renas och testas. Eftersom hEPO var förenat med en GST-tagg kunde forskarna fånga det på en specialkolonn som binder GST, tvätta bort föroreningar och sedan använda ett specifikt enzym för att klippa bort taggen och frigöra ett renare hEPO-produk. De visade, med biokemiska analyser, att det renade proteinet behöll mätbar biologisk aktivitet—vilket indikerar att hormonet framställt av dessa redigerade celler inte bara finns närvarande utan är funktionellt. Även om den totala avkastningen och den specifika aktiviteten var lägre än vad som uppnåtts i industriella cellinjer såsom CHO-celler, var detta experiment utformat som ett konceptbevis snarare än en fullt optimerad produktionsprocess.
Vad detta kan innebära för framtidens läkemedel
Enkelt uttryckt visar denna studie att det är möjligt att placera en human terapeutisk gen direkt under kontroll av en naturlig mjölkproteinswitch i bröstkörtelceller och att sätta på den genen med samma hormoner som driver laktation. Det resulterande hEPO kan utsöndras, delvis renas och visas vara verksamt—allt från en enda, väl definierad genomisk plats. Medan ytterligare förbättringar behövs—såsom att generera djur med båda genkopiorna modifierade, förbättrad rening och noggrann analys av proteinets detaljerade struktur—förflyttar denna riktade strategi idén att använda bröstkörteln som en säker, kontrollerbar bioreaktor för komplexa läkemedel närmare verklighet.
Citering: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Nyckelord: erytropoetin, CRISPR knock-in, mammälgsvarts bioreaktor, produktion av terapeutiska proteiner, beta-casein-lokus