Clear Sky Science · pl
Wstawienie ludzkiego erytropoetyny przy użyciu CRISPR/Cas9 w locusie β-kazeiny skutkuje ekspresją zależną od hormonów laktogennych w komórkach nabłonka gruczołu mlekowego HC11
Przekształcanie komórek mlecznych w maleńkie fabryki leków
Wiele współczesnych leków to białka, które nasze ciało naturalnie wytwarza, lecz ich produkcja na dużą skalę jest kosztowna i technicznie wymagająca. W tym badaniu zaproponowano sprytną alternatywę: przestrojenie komórek wytwarzających mleko tak, by uruchamiały ludzkie białko terapeutyczne tylko po aktywacji hormonami, podobnie jak naturalnie włączają białka mleka w okresie laktacji. Praca daje obraz, jak przyszłe zwierzęta hodowlane mogłyby bezpiecznie i wydajnie produkować złożone leki w mleku.
Celem: bezpieczna, precyzyjna produkcja leków
Przez lata naukowcy próbowali wykorzystać zwierzęta transgeniczne do produkcji leków, takich jak ludzka erytropoetyna (hEPO), hormon wspomagający powstawanie czerwonych krwinek. Wcześniejsze podejścia polegały na losowym wprowadzaniu genu hEPO do genomu, co często powodowało problemy: gen mógł być aktywowany w niewłaściwych tkankach, ulegać wyciszeniu lub szkodzić zwierzęciu. Autorzy tej pracy postanowili rozwiązać te problemy, umieszczając gen hEPO w bardzo konkretnym, dobrze poznanym miejscu genomu: w regionie, który normalnie kontroluje główne białko mleka, beta-kazeinę, w komórkach gruczołu mlekowego.
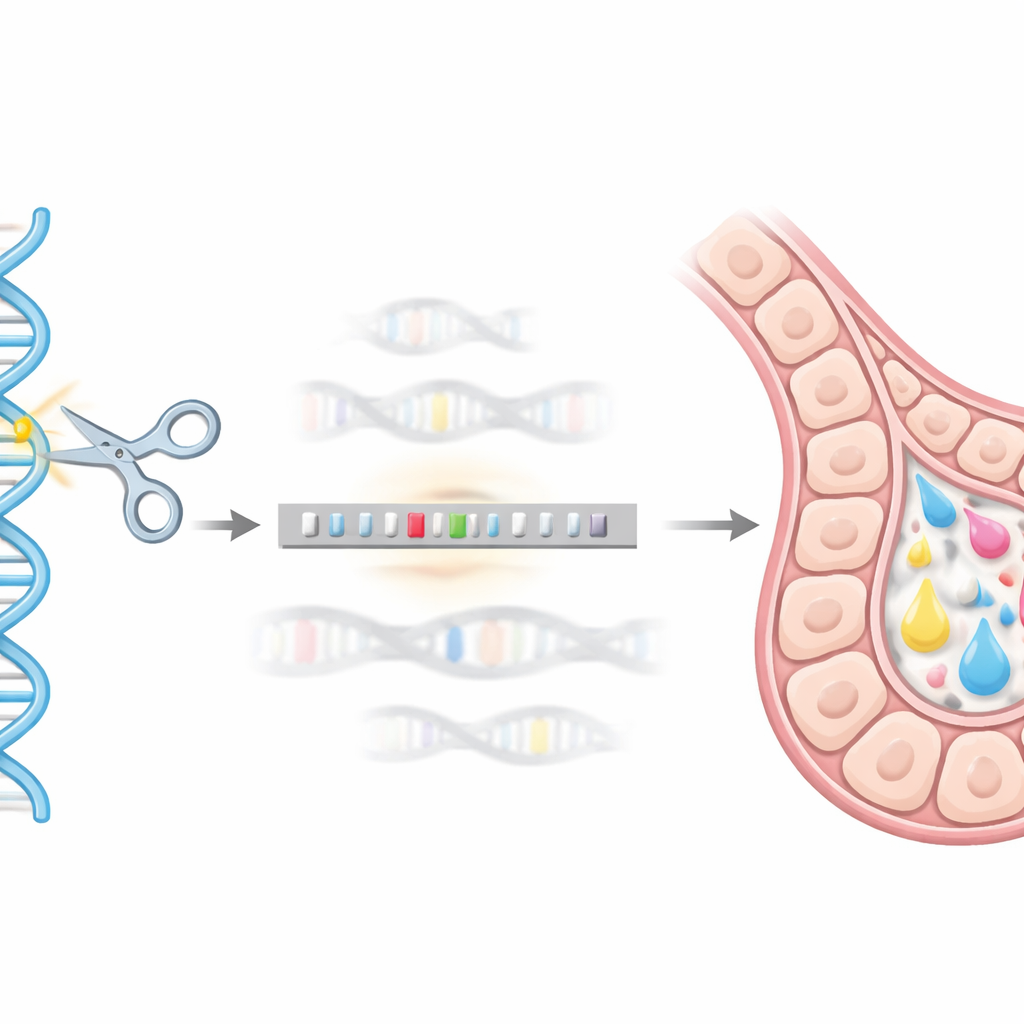
Edytowanie genu jako genomowy „GPS”
Aby trafić pod ten precyzyjny adres genetyczny, zespół użył systemu CRISPR/Cas9 jako swego rodzaju molekularnego GPS i nożyc. Zaprojektowali donorowy konstruktor DNA zawierający gen hEPO sprzężony z pomocniczą łatką (GST) i otoczony krótkimi odcinkami DNA odpowiadającymi regionowi beta-kazeiny. Kiedy CRISPR/Cas9 przeciął miejsce docelowe w mysich komórkach nabłonka gruczołu mlekowego HC11, naturalne mechanizmy naprawy komórkowej mogły wykorzystać ten konstruktor jako matrycę, starannie wstawiając sekwencję hEPO w locus beta-kazeiny. Poprzez serię badań genetycznych (metody oparte na PCR) wyizolowali klony z pojedynczych komórek, w których jedna kopia genu beta-kazeiny została pomyślnie zastąpiona konstruktem hEPO, tworząc stabilne linie „knock-in”.
Hormonowy przełącznik naśladuje naturalną produkcję mleka
Następnie badacze sprawdzili, czy nowy gen hEPO będzie podlegał tym samym regułom włączenia i wyłączenia co normalny gen białka mleka. Komórki HC11 można doprowadzić do stanu podobnego do laktacji przez dodanie hormonów „laktogennych”, podobnych do tych działających u ssącego zwierzęcia. W zmodyfikowanych klonach zespół zmierzył poziomy RNA i białka przed i po leczeniu hormonami. Stwierdzili, że poziom RNA hEPO wzrastał umiarkowanie — około 2–3-krotnie — po dodaniu hormonów, ale stężenie białka w płynie hodowlanym wzrosło znacznie bardziej, w przybliżeniu 10–20-krotnie. Ten wzorzec pokazuje, że wstawiony gen hEPO rzeczywiście znajduje się pod kontrolą elementów regulacyjnych specyficznych dla gruczołu mlekowego i jest wydzielany do otaczającego płynu w sposób zależny od hormonów, naśladując naturalną produkcję białek mleka.
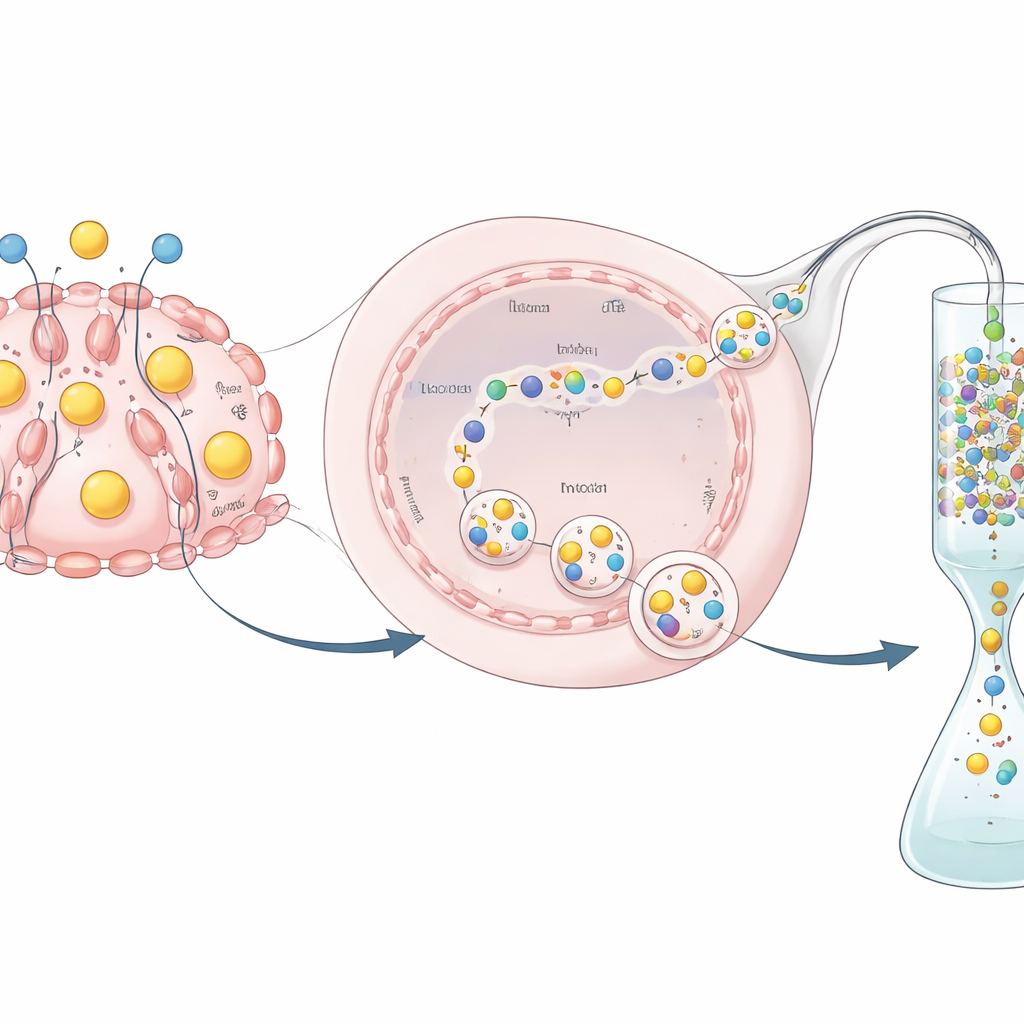
Od białka wydzielonego do użytecznego leku
Wyprodukowanie białka to tylko połowa wyzwania; trzeba je także oczyścić i przetestować. Ponieważ hEPO został sprzężony z łatką GST, badacze mogli wychwycić je na specjalnej kolumnie wiążącej GST, wypłukać zanieczyszczenia, a następnie użyć specyficznego enzymu do odcięcia łatki i uzyskania czystszego produktu hEPO. Wykazali, przy użyciu analiz biochemicznych, że oczyszczone białko zachowało mierzalną aktywność biologiczną — co wskazuje, że hormon wytworzony przez te zmodyfikowane komórki jest nie tylko obecny, ale i funkcjonalny. Chociaż całkowity uzysk i aktywność właściwa były niższe niż w przemysłowych liniach komórkowych, takich jak komórki CHO, eksperyment miał charakter dowodu koncepcji, a nie w pełni zoptymalizowanego procesu produkcyjnego.
Co to może znaczyć dla przyszłych leków
Mówiąc prościej, badanie dowodzi, że możliwe jest umieszczenie ludzkiego genu terapeutycznego bezpośrednio pod kontrolą naturalnego przełącznika białka mleka w komórkach gruczołu mlekowego i uruchamianie tego genu tymi samymi hormonami, które wywołują laktację. Powstała hEPO może być wydzielana, częściowo oczyszczana i wykazywać aktywność, wszystko z jednego, dobrze zdefiniowanego miejsca w genomie. Choć wymagane są dalsze udoskonalenia — takie jak uzyskanie zwierząt z modyfikacją obu kopii genu, poprawa metod oczyszczania i dokładna analiza struktury białka — ta celowana strategia przybliża ideę wykorzystania gruczołu mlekowego jako bezpiecznego, kontrolowanego bioreaktora do produkcji złożonych leków.
Cytowanie: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Słowa kluczowe: erytropoetyna, CRISPR knock-in, bioreaktor gruczołu mlekowego, produkcja białek terapeutycznych, locus beta-kazeiny