Clear Sky Science · tr
CRISPR/Cas9 aracılığıyla hedeflenen insan eritropoietin yerleştirmesi: β-kazein lokusunda HC11 meme epitel hücrelerinde laktogen hormonlara yanıt veren ifade
Süt Hücrelerini Küçük İlaç Fabrikalarına Dönüştürmek
Günümüzün birçok ilaçı vücudumuzun doğal olarak ürettiği proteinlerdir, ancak bunları fabrikalarda ölçekli olarak üretmek hem pahalı hem de teknik olarak zorludur. Bu çalışma zekice bir alternatif sunuyor: süt üreten hücrelerin, laktasyon sırasında doğal olarak süt proteinlerini açtıkları gibi, hormonlarla tetiklendiğinde insan terapötik bir proteini aktive edecek şekilde yeniden kablolanması. Çalışma, gelecekte çiftlik hayvanlarının sütlerinde karmaşık ilaçları güvenli ve verimli biçimde üretebileceğine dair bir önizleme sunuyor.
Güvenli, Hassas İlaç Üretimini Hedeflemek
Yıllardır bilim insanları insan eritropoietin (hEPO) gibi ilaçları üretmek için transgenik hayvanları kullanmayı denediler. hEPO, vücudun kırmızı kan hücresi üretimine yardımcı olan bir hormondur. Önceki girişimler genin genomda rastgele yerlere eklenmesine dayanıyordu; bu da genin yanlış dokularda açılmasına, susturulmasına veya hayvanda hastalığa yol açmasına neden olabiliyordu. Bu makalenin yazarları, bu sorunları çözmek amacıyla hEPO genini genomda çok özel ve iyi anlaşılan bir yere yerleştirmeyi amaçladılar: meme (süt üreten) hücrelerinde ana süt proteini olan beta-kazeini kontrol eden bölgeye.
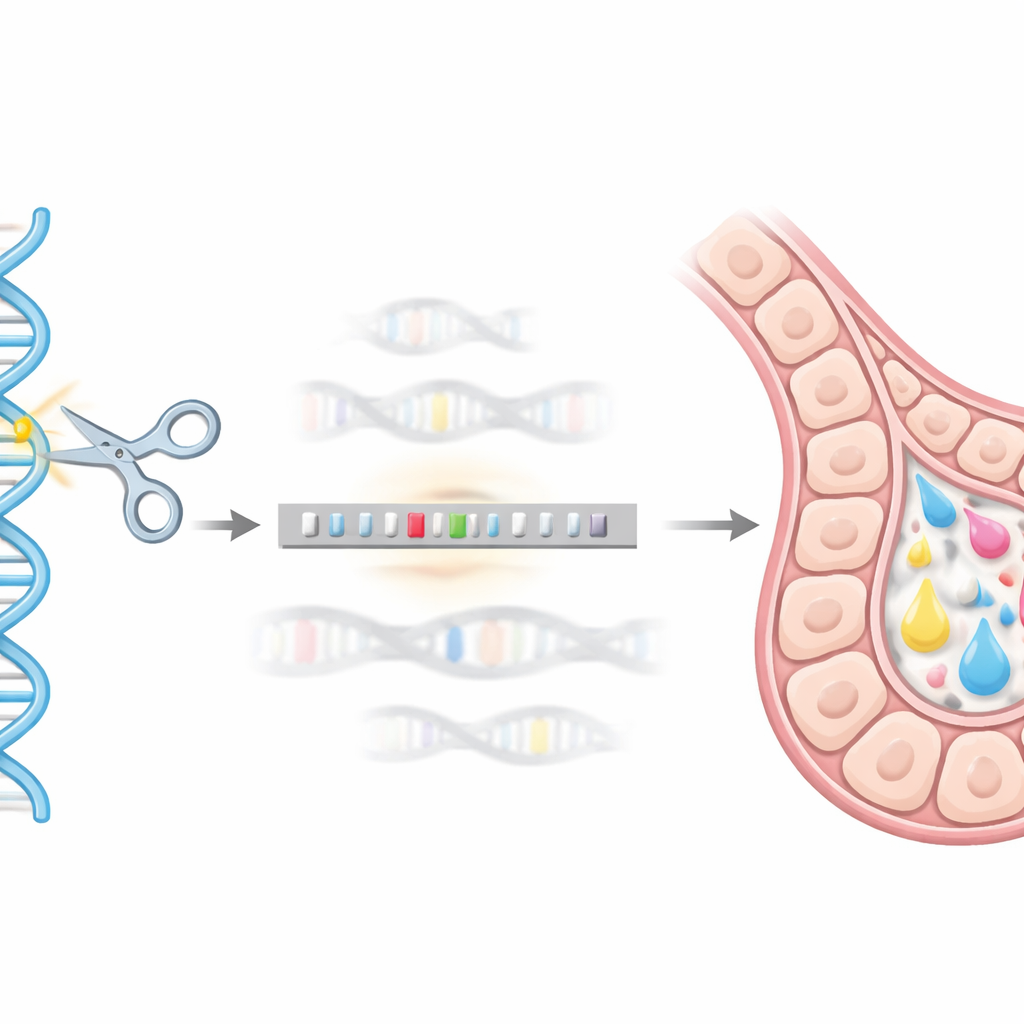
Genomik "GPS" olarak Gen Düzenleme Kullanmak
Bu hassas genomik adrese ulaşmak için ekip, CRISPR/Cas9 gen düzenleme sistemini bir tür moleküler GPS ve makas gibi kullandı. hEPO genini GST yardımcı etiketiyle füzyona uğratıp beta-kazein bölgesiyle eşleşen kısa DNA dizileriyle çevreledikleri bir DNA bağışçı kılıfı tasarladılar. CRISPR/Cas9 hedef bölgeyi mouse meme HC11 hücrelerinde kestiğinde, hücrenin doğal onarım mekanizması bu bağışçı kılıfı bir şablon olarak kullanıp hEPO dizisini beta-kazein lokusuna düzgünce yerleştirebildi. Bir dizi genetik test (PCR tabanlı yöntemler kullanılarak) ile beta-kazein geninin bir kopyasının başarıyla hEPO kılıfı ile değiştirildiği tek hücre klonları izole edilerek stabil “knock-in” hatları oluşturuldu.
Hormon Anahtarı Doğal Süt Üretimini Taklit Ediyor
Araştırmacılar, bu yeni hEPO geninin normal süt-proteini geninin açık-kapalı kurallarına uyup uymayacağını sorguladılar. HC11 hücreleri, emziren hayvanda işe yarayanlara benzer “laktogen” hormonlar eklenerek süt-benzeri bir duruma itilebilir. Mühendislik yapılan klonlarda ekip hormon tedavisinden önce ve sonra hem RNA hem de protein seviyelerini ölçtü. hEPO RNA seviyelerinin hormon eklenince 2–3 kat kadar ılımlı bir artış gösterdiğini, fakat kültür ortamındaki protein düzeylerinin çok daha dramatik biçimde—yaklaşık 10–20 kat—yükseldiğini buldular. Bu desen, yerleştirilen hEPO geninin gerçekten meme özgü düzenleyici öğelerin kontrolü altında olduğunu ve hormon bağımlı olarak çevreleyen sıvıya salgılandığını, yani doğal süt proteini üretimini taklit ettiğini gösteriyor.
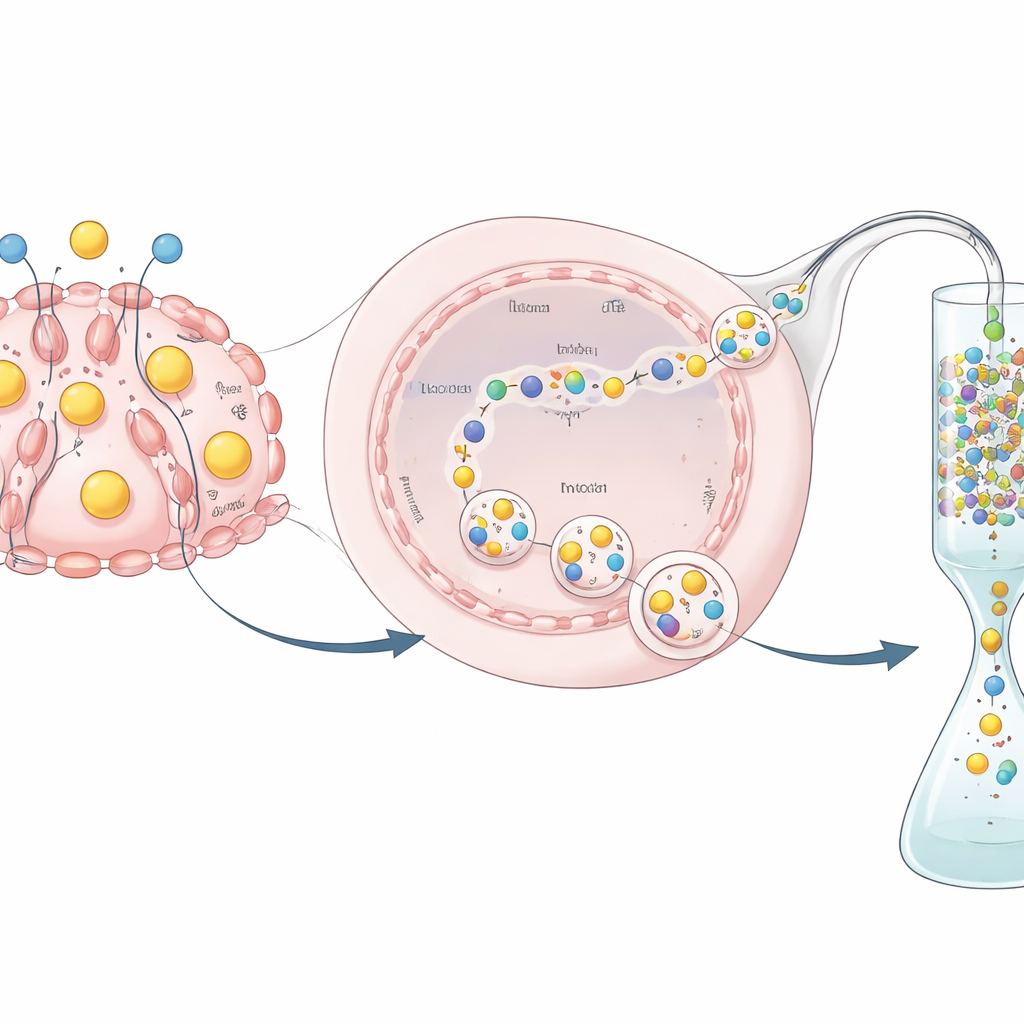
Salgılanan Proteinden Kullanılabilir İlaca
Bir proteini üretmek zorluğun yalnızca yarısıdır; ayrıca saflaştırılmalı ve test edilmelidir. hEPO GST etiketiyle füzyonlandığı için araştırmacılar GST bağlayan özel bir kolonda proteini tutup kirleri yıkayabilir ve ardından etiketi kesmek için spesifik bir enzim kullanarak daha temiz bir hEPO ürünü elde edebildiler. Biyokimyasal testlerle, saflaştırılmış proteinin ölçülebilir biyolojik aktiviteyi koruduğunu gösterdiler—bu da düzenlenmiş hücrelerin ürettiği hormonun sadece var olmadığını, aynı zamanda işlevsel olduğunu işaret ediyor. Genel verim ve özgül aktivite, CHO hücreleri gibi endüstriyel hücre hatlarında elde edilenlerin altında olsa da, bu deney tam anlamıyla optimize edilmiş bir üretim sürecinden ziyade bir kavram kanıtı olarak tasarlanmıştı.
Geleceğin İlaçları İçin Ne Anlam İfade Edebilir
Basitçe söylemek gerekirse, bu çalışma insan terapötik bir genin meme hücrelerinde doğal bir süt-proteini anahtarı altına doğrudan yerleştirilebileceğini ve bu genin laktasyonu yönlendiren aynı hormonlarla açılabileceğini gösteriyor. Ortaya çıkan hEPO salgılanabilir, kısmen saflaştırılabilir ve tek, iyi tanımlanmış bir genomik konumdan işlevsel olduğu gösterilebilir. Her iki gen kopyasının da değiştirilmesi, saflaştırmanın iyileştirilmesi ve proteinin ince yapısının dikkatle analiz edilmesi gibi daha fazla geliştirme gereksinimleri bulunsa da, bu hedeflenmiş strateji meme bezini karmaşık ilaçlar için güvenli ve kontrol edilebilir bir biyoreaktör olarak kullanma fikrini gerçeğe bir adım daha yaklaştırıyor.
Atıf: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Anahtar kelimeler: eritropoietin, CRISPR knock-in, meme bezi biyoreaktörü, terapötik protein üretimi, beta-kazein lokusu