Clear Sky Science · de
CRISPR/Cas9-vermittelte gezielte Einschleusung von humanem Erythropoietin in das β-Casein-Lokus führt zu laktogenhormon-responsiver Expression in HC11-Mammärepithelzellen
Milchzellen als winzige Medizinfabriken
Viele moderne Medikamente sind Proteine, die unser Körper natürlicherweise herstellt, doch ihre großtechnische Produktion ist teuer und technisch anspruchsvoll. Diese Studie untersucht eine clevere Alternative: Milchbildende Zellen so umzuschalten, dass sie ein humanes Therapeutikum nur dann aktivieren, wenn Hormone es auslösen — ähnlich wie sie bei der Laktation natürlich Milchproteine einschalten. Die Arbeit zeigt, wie künftige Nutztiere möglicherweise sicher und effizient komplexe Wirkstoffe in ihrer Milch produzieren könnten.
Auf sichere, präzise Arzneimittelproduktion ausgerichtet
Jahrelang versuchten Forschende, transgene Tiere zur Produktion von Medikamenten wie humanem Erythropoietin (hEPO) zu nutzen, einem Hormon, das die Bildung roter Blutkörperchen fördert. Frühere Ansätze setzten auf zufällige Einfügungen des hEPO-Gens ins Genom, was häufig Probleme verursachte: das Gen konnte in falschen Geweben aktiviert werden, stillgelegt werden oder Krankheiten beim Tier auslösen. Die Autorinnen und Autoren dieser Arbeit wollten diese Probleme lösen, indem sie das hEPO-Gen an einen sehr spezifischen, gut charakterisierten Ort im Genom setzen: in die Region, die normalerweise ein wichtiges Milchprotein namens Beta-Casein in den Milchdrüsenzellen kontrolliert.
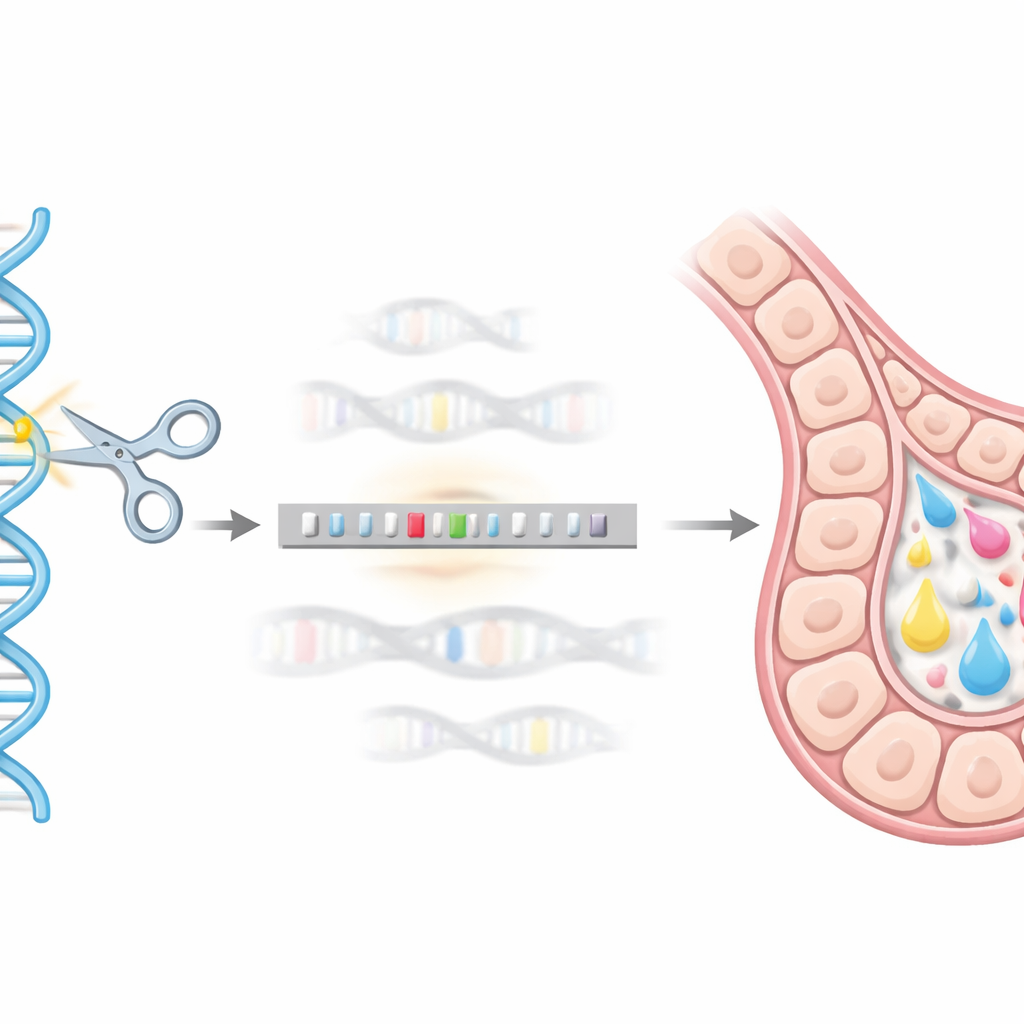
Geneditierung als genomisches „GPS“
Um diese präzise genomische Adresse zu erreichen, verwendete das Team das CRISPR/Cas9-Geneditierungssystem als eine Art molekulares GPS und Schere. Sie entwarfen ein DNA-Spenderkonstrukt, das das hEPO-Gen an ein Hilfs-Tag (GST) gekoppelt trägt und mit kurzen DNA-Sequenzen flankiert ist, die zum Beta-Casein-Bereich passen. Wenn CRISPR/Cas9 die Zielstelle in Maus-Mammariazellen (HC11) durchschnitt, konnte die zelluläre Reparaturmaschinerie dieses Spenderkonstrukt als Vorlage nutzen und die hEPO-Sequenz sauber in das Beta-Casein-Lokus einfügen. Mithilfe einer Reihe genetischer Tests (unter Verwendung PCR-basierter Methoden) isolierten sie Einzelzellklone, in denen eine Kopie des Beta-Casein-Gens erfolgreich durch das hEPO-Konstrukt ersetzt worden war und stabile „Knock-in“-Linien entstanden.
Hormon-Schalter imitiert natürliche Milchproduktion
Die Forschenden prüften anschließend, ob das neue hEPO-Gen denselben Ein-/Ausschaltregeln folgt wie das normale Milchprotein-Gen. HC11-Zellen lassen sich durch Zugabe von „laktogenen“ Hormonen in einen milchähnlichen Zustand versetzen, ähnlich den Hormonen, die in laktierenden Tieren wirken. In den modifizierten Klonen maßen sie sowohl RNA- als auch Proteinniveaus vor und nach der Hormonbehandlung. Sie fanden heraus, dass die hEPO-RNA-Spiegel moderat anstiegen — etwa um das Zwei- bis Dreifache — wenn Hormone hinzugefügt wurden, die Proteinmengen im Kulturmedium jedoch deutlich stärker zunahmen, nämlich ungefähr um das 10- bis 20-Fache. Dieses Muster zeigt, dass das eingebrachte hEPO-Gen tatsächlich unter der Kontrolle der mammären, spezifischen Regulations-Elemente steht und hormonabhängig in das umgebende Medium sezerniert wird, ähnlich der natürlichen Milchproteinsynthese.
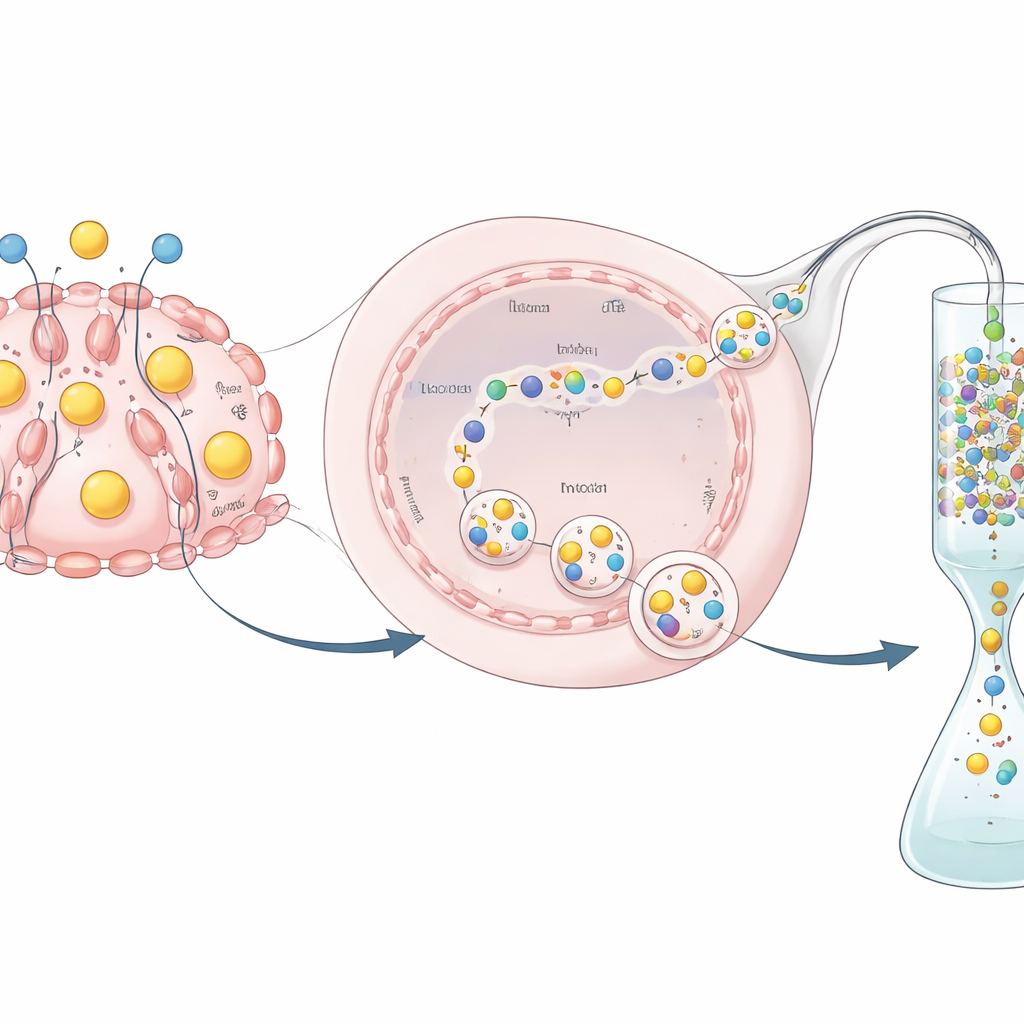
Von sekretierter Substanz zum verwendbaren Arzneimittel
Die Produktion eines Proteins ist nur die halbe Herausforderung; es muss auch gereinigt und getestet werden. Da das hEPO mit einem GST-Tag fusioniert war, konnten die Forschenden es auf einer speziellen Säule auffangen, die GST bindet, Verunreinigungen abspülen und dann ein spezifisches Enzym nutzen, um das Tag abzuschneiden und ein saubereres hEPO-Produkt freizusetzen. Sie zeigten mit biochemischen Tests, dass das gereinigte Protein messbare biologische Aktivität behielt — was darauf hinweist, dass das von den editierten Zellen produzierte Hormon nicht nur vorhanden, sondern funktional ist. Obwohl Ausbeute und spezifische Aktivität geringer waren als bei industriellen Zelllinien wie CHO-Zellen, diente dieses Experiment als Proof-of-Concept und nicht als vollständig optimierter Produktionsprozess.
Was das für künftige Medikamente bedeuten könnte
Kurz gesagt demonstriert diese Studie, dass es möglich ist, ein humanes Therapeutikum direkt unter die Kontrolle eines natürlichen Milchprotein-Schalters in Mammariazellen zu platzieren und dieses Gen mit denselben Hormonen zu aktivieren, die die Laktation steuern. Das resultierende hEPO kann sezerniert, teilweise aufgereinigt und als wirksam nachgewiesen werden — alles von einem einzigen, klar definierten genomischen Ort aus. Obwohl weitere Verbesserungen nötig sind — etwa die Erzeugung von Tieren mit beiden Genkopien verändert, bessere Reinigungsverfahren und eine sorgfältige Analyse der Feinstruktur des Proteins — rückt diese zielgerichtete Strategie die Idee, die Brustdrüse als sicheren, steuerbaren Bioreaktor für komplexe Medikamente zu nutzen, näher an die Realität.
Zitation: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Schlüsselwörter: Erythropoietin, CRISPR-Knock-in, Brustdrüsen-Bioreaktor, Produktion therapeutischer Proteine, Beta-Casein-Lokus