Clear Sky Science · he
החדרת CRISPR/Cas9 המכוונת של אריתרופואטין אנושי למקום ה-β-קזאין מובילה לביטוי רגיש להורמוני להנקה בתאי אפיתל שדיים HC11
להפוך תאי חלב למפעלים זעירים לתרופות
תרופות מודרניות רבות הן חלבונים שהגוף שלנו מייצר באופן טבעי, אך ייצור בקנה מידה תעשייתי יקר ומורכב טכנית. המחקר הזה בוחן אלטרנטיבה חכמה: לכוון מחדש תאים המייצרים חלב כך שיוכלו להפעיל חלבון טיפולי אנושי רק כאשר הם מופרעים על־ידי הורמונים, בדומה להפעלת חלבוני החלב במהלך ההנקה. העבודה מציעה הצצה לאופן שבו בעלי חיים חקלאיים עתידיים עשויים לייצר תרופות מורכבות בחלבם בצורה בטוחה ויעילה.
שאיפה לייצור תרופות מדויק ובטוח
שנים רבות מדענים ניסו להשתמש בבעלי חיים טרנסגניים כדי לייצר תרופות כמו אריתרופואטין אנושי (hEPO), הורמון המסייע לייצור תאי דם אדומים. ניסיונות מוקדמים התבססו על החדרה אקראית של גן ה-hEPO לגנום, מה שהוביל לעתים קרובות לבעיות כגון הפעלה לא במקומה, שתקה של הגן או גרימת מחלות בבעלי החיים. המחברים של מאמר זה שאפו לפתור בעיות אלה על ידי הצבת גן ה-hEPO במיקום ספציפי ומובן בגנום: האזור שמווסת בדרך כלל חלבון חלב מרכזי הנקרא בטא-קזאין בתאי השד (תאי ייצור החלב).
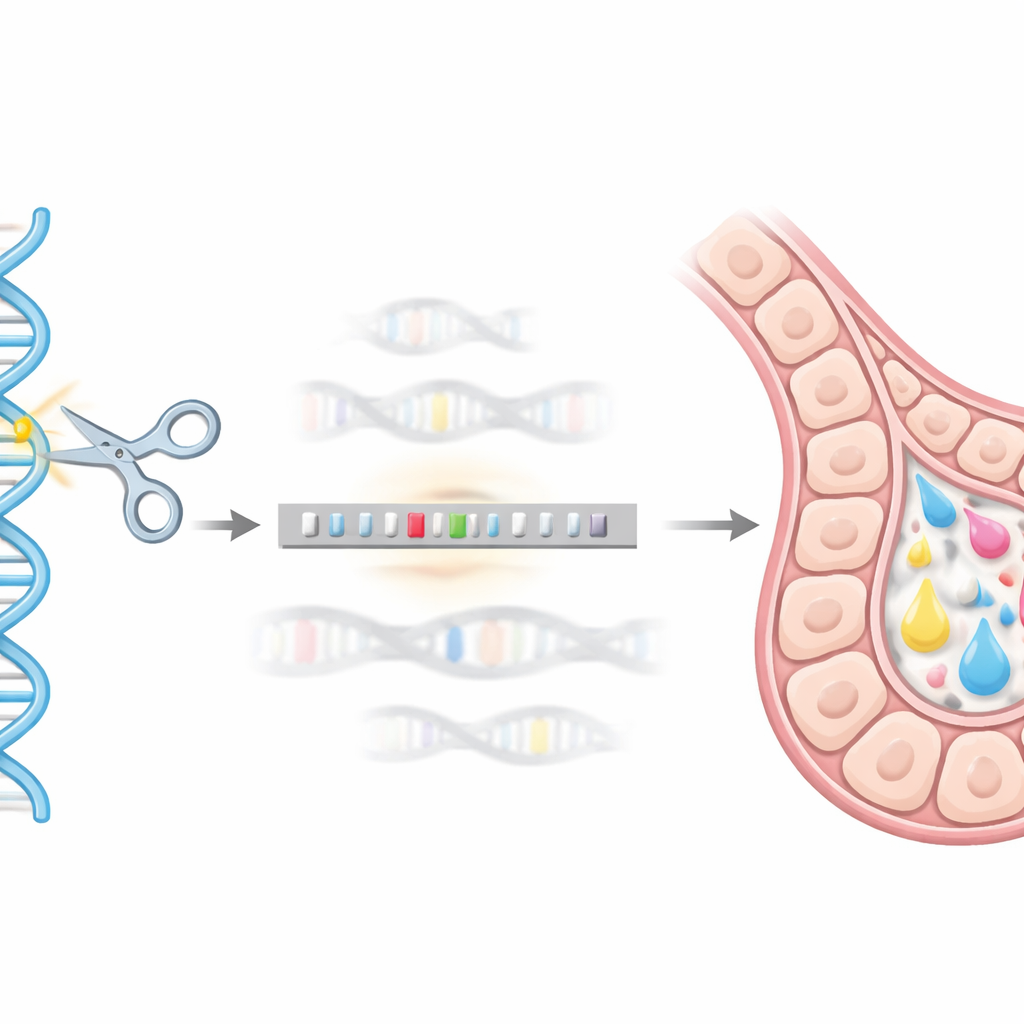
שימוש בעריכת גנים כ"GPS" גנומי
כדי להגיע לכתובת הגנומית המדויקת הזו, הצוות השתמש במערכת העריכה CRISPR/Cas9 כסוג של GPS ומספריים מולקולריים. הם תכננו תבנית דנ״א תורמת שנושאת את גן ה-hEPO מחובר לתג עזר (GST) וסגרו אותו בקצוות בקצרי רצפי דנ״א התואמים לאזור הבטא-קזאין. כאשר CRISPR/Cas9 חתר את אתר היעד בתאי השד של עכבר HC11, מנגנוני התיקון הטבעיים של התא יכלו להשתמש בתבנית התורמת כתבנית, ולהחדיר בצורה נקייה את רצף ה-hEPO ללוקוס של בטא-קזאין. באמצעות סדרת בדיקות גנטיות (שימוש בשיטות מבוססות PCR) הם בודדו שורות של קלונות מתא יחיד שבהן עותק אחד של גן הבטא-קזאין הוחלף בהצלחה על־ידי קונסטרוקט ה-hEPO, ויצרו שורות "נוק-אין" יציבות.
מתג הורמונלי המדמה ייצור חלב טבעי
החוקרים לאחר מכן שאלו האם הגן החדש של ה-hEPO יתנהג לפי כללי ההפעלה והכיבוי של גן חלב רגיל. ניתן לדחוף תאי HC11 למצב דמוי חלב על־ידי הוספת הורמונים "לקטוגניים", דומים לאלו הפועלים בחיה מניקה. בקלונות המהונדסים מדדו הצוות רמות RNA וחלבון לפני ואחרי טיפול הורמונלי. הם מצאו שרמות ה-RNA של hEPO עלו באופן צנוע — בערך פי שניים עד שלושה — כאשר הוספו הורמונים, אך רמות החלבון בתווך התרביתי עלו בצורה דרמטית הרבה יותר, בכ-10 עד 20 פעמים. תבנית זו מצביעה על כך שהגן המוחדר נמצא אכן תחת שליטה של מרכיבים ויסותיים הספציפיים לבלוטת החלב ומופרש לנוזל הסובב באופן תלוי הורמונים, המדמה את ייצור חלבון החלב הטבעי.
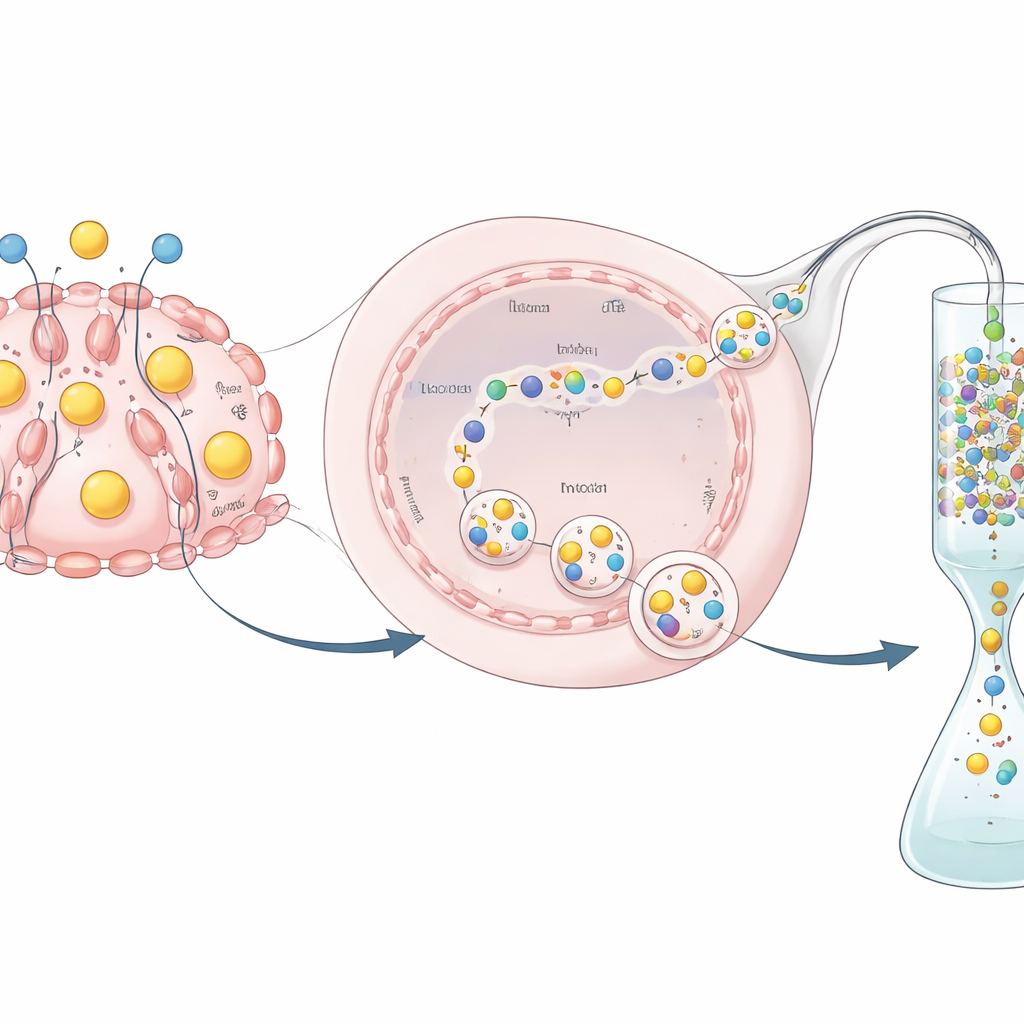
מחלבון מופרש לתרופה שניתן להשתמש בה
ייצור החלבון הוא רק חצי מהאתגר; יש גם לטהר אותו ולבחון אותו. מאחר ש-hEPO חובר לתג GST, החוקרים יכלו ללכוד אותו על עמודה מיוחדת הקושרת GST, לשטוף זיהומים, ואז להשתמש באנזים ספציפי כדי לחתוך את התג ולשחרר מוצר hEPO נקי יותר. הם הראו באמצעות ניסויים ביוכימיים שהחלבון המטוהר שמר על פעילות ביולוגית נמדדת — מה שמעיד שההורמון שנוצר על־ידי התאים הערוכים אינו רק קיים אלא גם פונקציונלי. אף על פי שהתשואה הכוללת והפעילות הספציפית היו נמוכות מאלו שהושגו בקווי תאים תעשייתיים כגון תאי CHO, הניסוי עוצב כהוכחת עיקרון ולא כהליך ייצור משוכלל וממוטב.
מה זה עשוי להגיד על תרופות בעתיד
במונחים פשוטים, המחקר מראה שאפשר לשים גן טיפולי אנושי ישירות תחת שליטת מתג טבעי של חלב בחלל הגנומי של תאי השד, ולהפעיל את הגן הזה באותם הורמונים שמניעים הנקה. ה-hEPO המתקבל יכול להיות מופרש, מטוהר חלקית ומופגנת כפעיל, וכל זאת ממיקום גנומי יחיד ומוגדר היטב. בעוד שדרושים שיפורים נוספים — כגון יצירת בעלי חיים עם שני העותקים של הגן מותאמים, שיפור הטיהור וניתוח מדוקדק של המבנה העדין של החלבון — האסטרטגיה הממוקדת הזו מקרבת את רעיון השימוש בבלוטת החלב כביוריאקטור בטוח ומוצג לשליטה לתרופות מורכבות למציאות.
ציטוט: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
מילות מפתח: אריתרופואטין, החדרת CRISPR, ביוריאקטור של בלוטת החלב, ייצור חלבונים טיפוליים, לוקוס בטא-קזאין