Clear Sky Science · es
Inserción dirigida mediada por CRISPR/Cas9 de eritropoyetina humana en el locus de la β-caseína da como resultado una expresión sensible a hormonas lactogénicas en células epiteliales mamarias HC11
Convertir células lácteas en pequeñas fábricas de medicinas
Muchos medicamentos modernos son proteínas que nuestro propio cuerpo fabrica de forma natural, pero producirlas a escala en fábricas es caro y técnicamente complejo. Este estudio explora una alternativa ingeniosa: reconectar las células productoras de leche para que activen una proteína terapéutica humana solo cuando lo ordenen las hormonas, de forma análoga a cómo en la lactación se encienden naturalmente las proteínas de la leche. El trabajo ofrece una visión de cómo animales de granja podrían, en el futuro, fabricar de manera segura y eficiente fármacos complejos en su leche.
Apuntando a una producción de fármacos segura y precisa
Durante años, los científicos han intentado usar animales transgénicos para producir medicamentos como la eritropoyetina humana (hEPO), una hormona que ayuda al organismo a producir glóbulos rojos. Intentos anteriores dependían de insertar el gen de hEPO al azar en el genoma, lo que con frecuencia provocaba varios problemas: el gen podía activarse en tejidos inapropiados, silenciarse o causar enfermedad en el animal. Los autores de este trabajo se propusieron resolver esos problemas ubicando el gen de hEPO en un sitio muy específico y bien caracterizado del genoma: la región que normalmente controla una proteína principal de la leche denominada beta-caseína en células mamarias (productoras de leche).
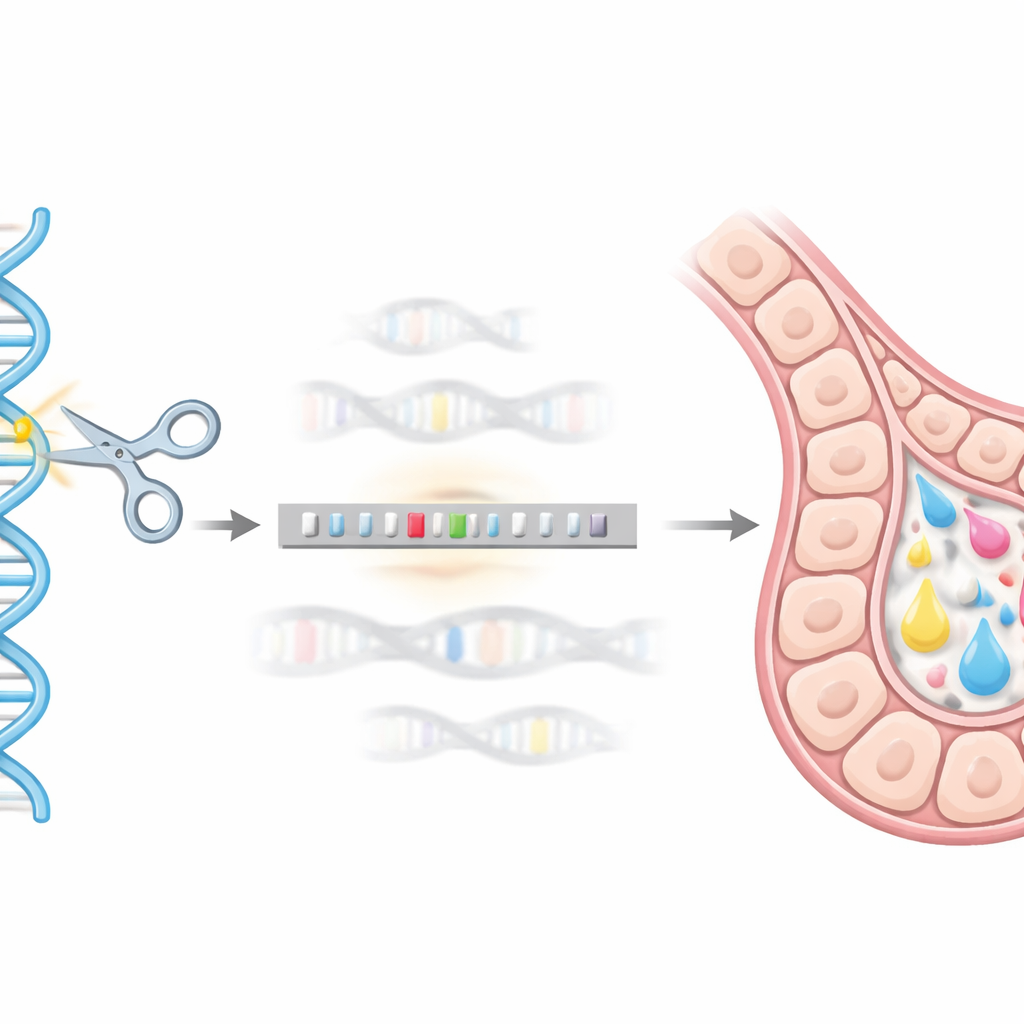
Usar la edición genética como un “GPS” genómico
Para alcanzar esta dirección genómica precisa, el equipo usó el sistema de edición CRISPR/Cas9 como una suerte de GPS molecular y tijeras. Diseñaron un donante de ADN que llevaba el gen hEPO fusionado a una etiqueta auxiliar (GST) y lo flanquearon con cortos tramos de ADN coincidentes con la región de la beta-caseína. Cuando CRISPR/Cas9 cortó el sitio objetivo en células mamarias murinas HC11, la maquinaria de reparación natural de la célula pudo usar ese donante como plantilla, insertando limpiamente la secuencia de hEPO en el locus de beta-caseína. Mediante una serie de pruebas genéticas (con métodos basados en PCR), aislaron clones de una sola célula en los que una copia del gen de beta-caseína había sido reemplazada con éxito por el constructo hEPO, creando líneas estables de “knock-in”.
El interruptor hormonal imita la producción natural de leche
Los investigadores se preguntaron entonces si este nuevo gen hEPO seguiría las mismas reglas de encendido y apagado que el gen normal de proteína de la leche. Las células HC11 pueden inducirse a un estado similar al de la leche añadiendo hormonas “lactogénicas”, similares a las que actúan en un animal lactante. En los clones modificados, el equipo midió niveles de ARN y proteína antes y después del tratamiento hormonal. Encontraron que los niveles de ARN de hEPO aumentaron modestamente—aproximadamente de dos a tres veces—cuando se añadieron hormonas, pero los niveles de proteína en el medio de cultivo subieron con mucha más intensidad, en torno a 10-20 veces. Este patrón indica que el gen hEPO insertado está, efectivamente, bajo el control de los elementos reguladores específicos de la glándula mamaria y se secreta al fluido circundante de forma dependiente de hormonas, imitando la producción natural de proteínas de la leche.
De proteína secretada a medicamento utilizable
Producir una proteína es solo la mitad del desafío; también debe purificarse y evaluarse. Como la hEPO estaba fusionada a una etiqueta GST, los investigadores pudieron capturarla en una columna especial que une GST, lavar las impurezas y luego usar una enzima específica para cortar la etiqueta y liberar un producto hEPO más limpio. Demostraron, mediante ensayos bioquímicos, que la proteína purificada conservaba actividad biológica medible—lo que indica que la hormona producida por estas células editadas no solo está presente sino que es funcional. Aunque el rendimiento global y la actividad específica fueron inferiores a los logrados en líneas celulares industriales como las CHO, este experimento fue diseñado como una prueba de concepto más que como un proceso de producción completamente optimizado.
Qué podría significar esto para los medicamentos del futuro
En términos sencillos, este estudio demuestra que es posible ubicar un gen terapéutico humano directamente bajo el control de un interruptor natural de proteína de la leche en células mamarias, y activar ese gen con las mismas hormonas que impulsan la lactación. La hEPO resultante puede secretarse, purificarse parcialmente y mostrarse funcional, todo desde una única ubicación genómica bien definida. Aunque se necesitan mejoras adicionales—como generar animales con ambas copias del gen modificadas, optimizar la purificación y analizar con detalle la estructura fina de la proteína—esta estrategia dirigida acerca la idea de usar la glándula mamaria como un biorreactor seguro y controlable para medicamentos complejos a una realidad más tangible.
Cita: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
Palabras clave: eritropoyetina, inserción CRISPR, biorreactor de glándula mamaria, producción de proteínas terapéuticas, locus de beta-caseína