Clear Sky Science · ar
الدمج المستهدف بواسطة CRISPR/Cas9 لجين الإريثروبويتين البشري في موقع بيتا-كازين يؤدي إلى تعبير مستجيب للهرمونات اللبنية في خلايا الظهارة الثديية HC11
تحويل خلايا الحليب إلى مصانع صغيرة للأدوية
العديد من الأدوية الحديثة هي بروتينات يصنعها جسمنا طبيعياً، لكن إنتاجها على نطاق واسع في المصانع مكلف ويتطلب مهارات تقنية عالية. تستكشف هذه الدراسة بديلًا ذكيًا: إعادة برمجة خلايا إنتاج الحليب بحيث تقوم بتشغيل بروتين علاجي بشري فقط عند تحفيزها بالهرمونات، على غرار تشغيلها الطبيعي لبروتينات الحليب أثناء الإرضاع. يقدم العمل لمحة عن كيف يمكن أن تنتج الحيوانات المستقبلية الأدوية المعقدة في حليبها بأمان وكفاءة.
السعي لإنتاج دوائي دقيق وآمن
لسنوات، حاول العلماء استخدام حيوانات متحولة وراثيًا لإنتاج أدوية مثل الإريثروبويتين البشري (hEPO)، وهو هرمون يساعد الجسم في تكوين خلايا الدم الحمراء. اعتمدت المحاولات السابقة على إدخال عشوائي لجين hEPO في الجينوم، ما أدى غالبًا إلى مشاكل مثل تشغيل الجين في أنسجة خاطئة، أو كبت تعبيره، أو التسبب بمرض للحيوان. سعى مؤلفو هذه الورقة إلى حل هذه المشاكل بوضع جين hEPO في موقع محدد ومعروف جيدًا في الجينوم: المنطقة التي تتحكم عادةً في بروتين الحليب الرئيسي المسمى بيتا-كازين في خلايا الثدي (الخلايا المنتجة للحليب).
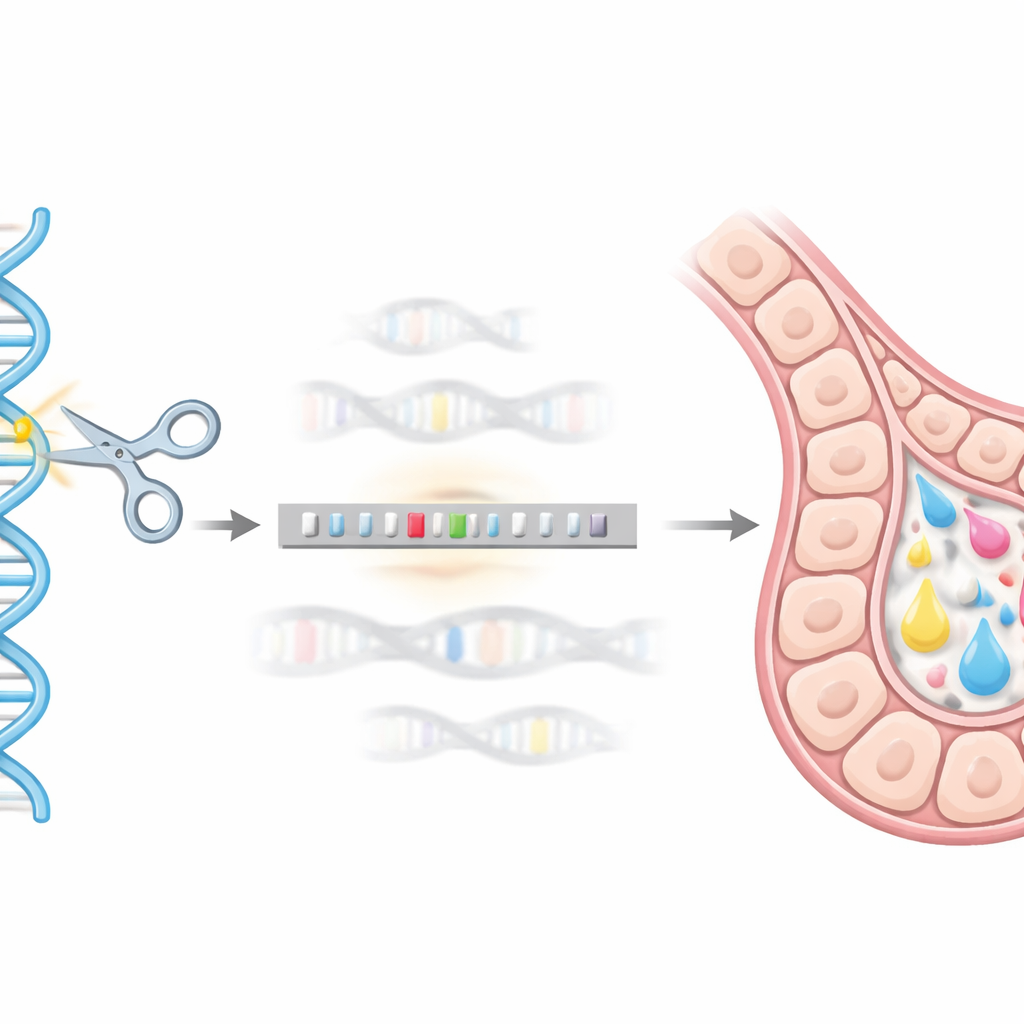
استخدام تحرير الجينات كـ "نظام تحديد مواقع" جيني
لوصولهم إلى هذا العنوان الجينومي الدقيق، استخدم الفريق نظام تحرير الجينات CRISPR/Cas9 كنوع من نظام تحديد المواقع والجِرَاح الجزيئي. صمموا قطعة مرسِل DNA تحمل جين hEPO مدموجًا بعلامة مساعدة (GST) ومحاطة بمقاطع قصيرة من الحمض النووي المطابقة لمنطقة بيتا-كازين. عندما قطع CRISPR/Cas9 الموقع المستهدف في خلايا الثدي الفأرية HC11، استغلّت آلية الإصلاح الطبيعية للخلية هذا الناقل كقالب، فأدخلت تسلسل hEPO في موقع بيتا-كازين. ومن خلال سلسلة من الاختبارات الجينية (باستخدام طرق تعتمد على PCR)، عزلوا كلونات أحادية الخلية استبدل فيها نسخة واحدة من جين بيتا-كازين بنجاح ببناء hEPO، مكونين خطوطًا ثابتة من "الادخال الجيني" (knock-in).
مفتاح هرمي يحاكي إنتاج الحليب الطبيعي
سأل الباحثون بعد ذلك ما إذا كان جين hEPO الجديد سيتبع نفس قواعد التشغيل والإيقاف التي يخضع لها جين بروتين الحليب الطبيعي. يمكن دفع خلايا HC11 إلى حالة شبيهة بالحليب بإضافة هرمونات "لبنية" تشبه تلك الفعالة في حيوانات المرضعة. في الكلونات المعدلة، قاس الفريق مستويات كل من الحمض النووي الريبي والبروتين قبل وبعد علاج الهرمونات. وجدوا أن مستويات RNA لـ hEPO ارتفعت بشكل متواضع — بنحو مرتين إلى ثلاث مرات — عند إضافة الهرمونات، لكن مستويات البروتين في وسط الزرع ارتفعت بدرجة أكبر بكثير، نحو 10 إلى 20 ضعفًا تقريبًا. يظهر هذا النمط أن جين hEPO المدرج يخضع فعلاً لعناصر التنظيم الخاصة بالغدة الثديية ويُفرَز إلى السائل المحيط بطريقة تعتمد على الهرمونات، محاكيًا إنتاج بروتينات الحليب الطبيعي.
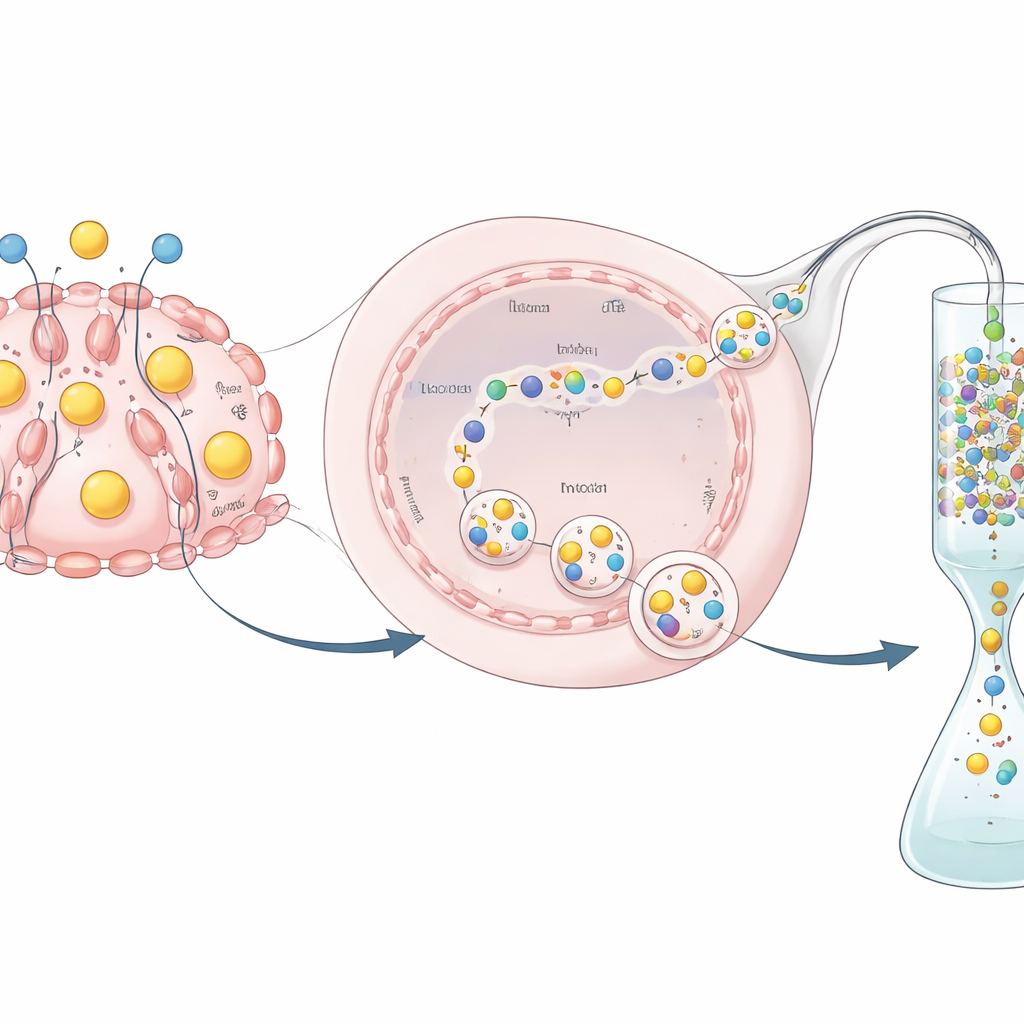
من بروتين مُفرَز إلى دواء قابل للاستخدام
إنتاج البروتين هو نصف التحدي فقط؛ إذ يجب أيضًا تنقيته واختباره. وبما أن hEPO كان مدموجًا بعلامة GST، تمكّن الباحثون من صيده على عمود خاص يرتبط بـ GST، وغسل الشوائب، ثم استخدام إنزيم محدد لقطع العلامة وإطلاق منتج hEPO أنقى. أظهروا، باستخدام تجارب بيوكيميائية، أن البروتين المنقّى احتفظ بنشاط بيولوجي قابل للقياس — ما يدل على أن الهرمون المنتج من هذه الخلايا المعدلة ليس مجرد وجودي بل فعال. وعلى الرغم من أن العائد الكلي والنشاط النوعي كانا أقل مما يُحقق عادة في خطوط خلوية صناعية مثل خلايا CHO، فصُمم هذا التجربة لإثبات المفهوم وليس كعملية إنتاج مُحسّنة بالكامل.
ماذا يعني هذا للأدوية المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أنه من الممكن وضع جين علاجي بشري مباشرةً تحت سيطرة مفتاح طبيعي لبروتين الحليب في خلايا الثدي، وأن يتم تشغيل هذا الجين بنفس الهرمونات التي تحفز الإدرار اللبني. يمكن أن يُفرَز hEPO الناتج، ويُنقّى جزئيًا، ويُثبت عمله، وكل ذلك من موقع جينومي واحد محدد جيدًا. وبينما هناك حاجة إلى تحسينات إضافية — مثل إنشاء حيوانات مُعدَّلة على نسختي الجين معًا، وتحسين عمليات التنقية، وتحليل البنية الدقيقة للبروتين بعناية — تقرّب هذه الاستراتيجية المستهدفة فكرة استخدام الغدة الثديية كمفاعل حيوي آمن وقابل للتحكم لإنتاج أدوية معقدة من الواقع.
الاستشهاد: You, HJ., Kim, GY. & Kang, MJ. CRISPR/Cas9-mediated targeted knock-in of human erythropoietin at the β-casein locus results in lactogenic hormone-responsive expression in HC11 mammary epithelial cells. Sci Rep 16, 14606 (2026). https://doi.org/10.1038/s41598-026-45234-5
الكلمات المفتاحية: الإريثروبويتين, إدخال جيني بواسطة CRISPR, مفاعل حيوي للغدة الثديية, إنتاج البروتينات العلاجية, موقع بيتا-كازين